Содержание
- 2. Содержание урока 1. Понятие : гидролиз Классификация гидролиза 2. Гидролиз органических веществ 3. Гидролиз солей 4.
- 3. Гидролиз – это реакция обменного разложения веществ водой Частицы растворенного вещества в воде окружены гидратной оболочкой.
- 4. Классификация гидролиза
- 5. гидролиз
- 6. Гидролиз органических веществ Гидролиз галагеналканов Гидролиз сложных эфиров (жиров) Гидролиз углеводов Гидролиз белков Гидролиз АТФ (аденозинтрифосфорная
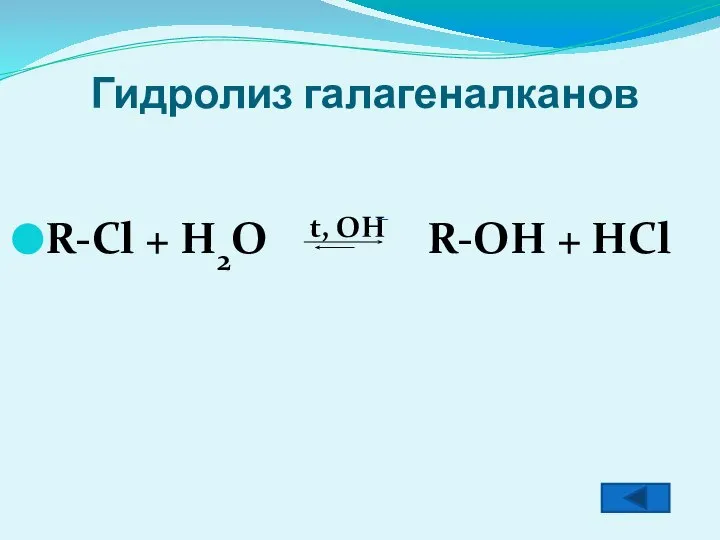
- 7. Гидролиз галагеналканов R-Cl + H2O t, OH R-OH + HCl
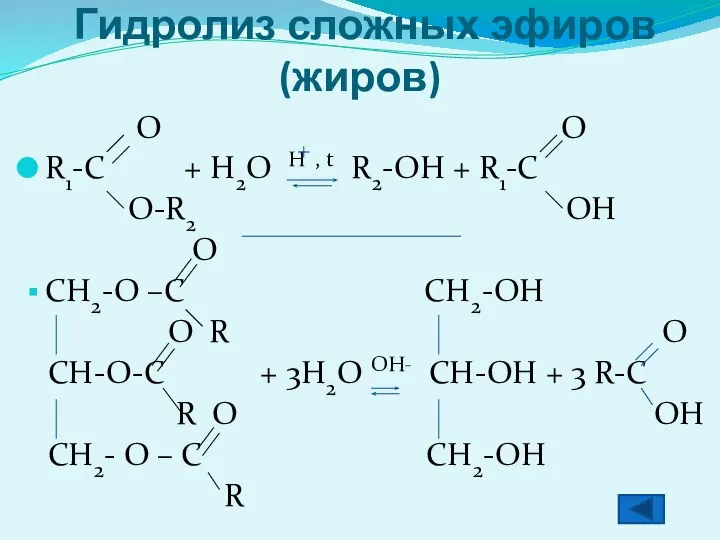
- 8. Гидролиз сложных эфиров (жиров) O O R1-C + H2O H , t R2-OH + R1-C O-R2
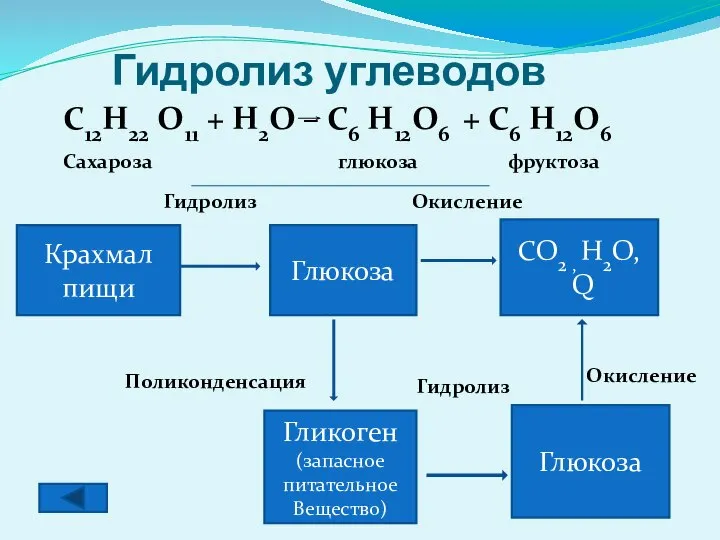
- 9. Гидролиз углеводов Крахмал пищи Глюкоза CO2 , H2O, Q Гликоген (запасное питательное Вещество) Глюкоза Гидролиз Окисление
- 10. Гидролиз белков O H O H H2N – CH2 – C – N – CH –
- 11. Гидролиз АТФ (аденозинтрифосфорная кислота) АТФ + Н2О Н3РО4 + АДФ + энергия
- 12. Гидролиз солей Сущность гидролиза сводится к обменному химическому взаимодействию катионов или анионов соли с молекулами воды.
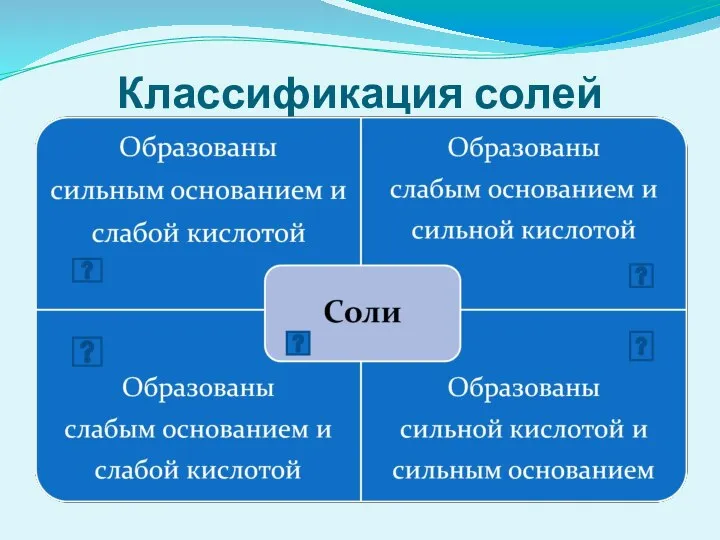
- 13. Классификация солей
- 14. Слабые кислоты: HCOOH, CH3COOH, HCN, H2S, HF, H2CO3, H2 SO3, H3PO4 , HNO2 ; Слабые основания:
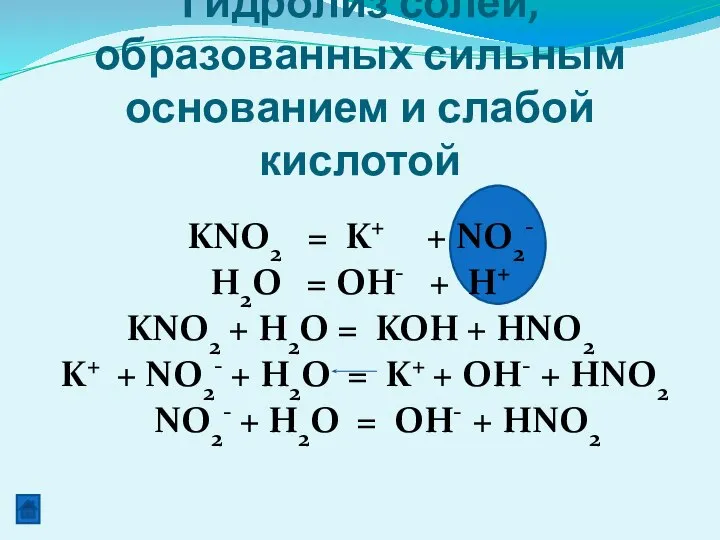
- 15. KNO2 = K+ + NO2- H2O = OH- + H+ KNO2 + H2O = KOH +
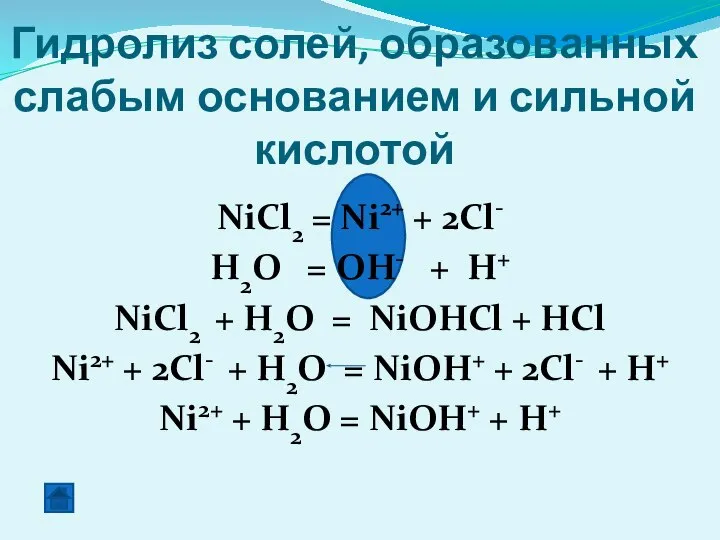
- 16. Гидролиз солей, образованных слабым основанием и сильной кислотой NiCl2 = Ni2+ + 2Cl- H2O = OH-
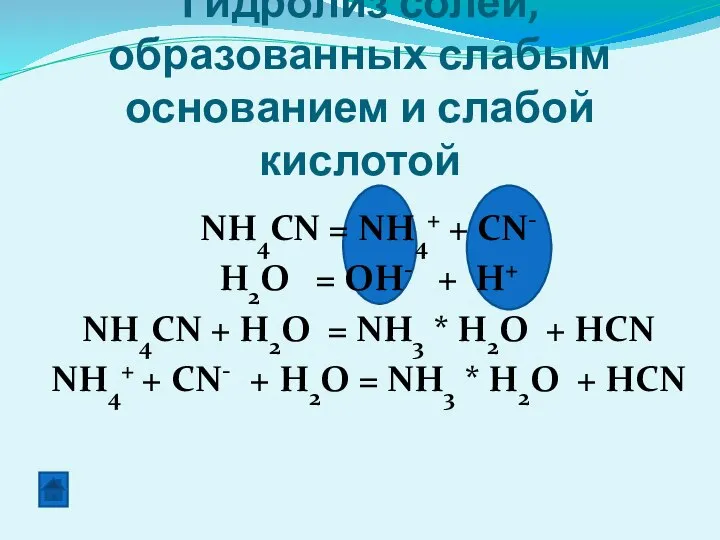
- 17. Гидролиз солей, образованных слабым основанием и слабой кислотой NH4CN = NH4+ + CN- H2O = OH-
- 18. Гидролиз солей, образованных сильным основанием и сильной кислотой KCl = K+ + Cl- H2O = OH-
- 19. Гидролиз солей
- 20. Гидролиз неорганических соединений Полному и необратимому гидролизу в водном растворе подвергаются некоторые бинарные соединения: карбиды; галогениды;
- 21. Гидролиз карбидов CaC2 + 2H2O = Ca(OH)2 +C2 H2 Карбид кальция ацетилен Al4C3 + 12 H2O
- 23. Скачать презентацию











 Н2O Матвієнко А. 10-а
Н2O Матвієнко А. 10-а  Зола. Свойства щёлока
Зола. Свойства щёлока Химические свойства металлов. (9 класс)
Химические свойства металлов. (9 класс) Ди- және полисахаридтер
Ди- және полисахаридтер История спички Выполнил ученик 9 б класса МОУ Навлинская СОШ №1 Фролов Кирилл
История спички Выполнил ученик 9 б класса МОУ Навлинская СОШ №1 Фролов Кирилл Химия в быту
Химия в быту Investigation of the conditions for the synthesis of a silver - containing composite
Investigation of the conditions for the synthesis of a silver - containing composite ПИЩЕВЫЕ ДОБАВКИ-Е Выполнила ученица 10 класса Цатурова Аида Арташевна
ПИЩЕВЫЕ ДОБАВКИ-Е Выполнила ученица 10 класса Цатурова Аида Арташевна Тема урока: Силикатная промышленность
Тема урока: Силикатная промышленность Периодический закон Менделеева в действии
Периодический закон Менделеева в действии Презентация Предельные углеводороды
Презентация Предельные углеводороды  Электродные процессы
Электродные процессы Уксусная кислота (эта́новая кислота)
Уксусная кислота (эта́новая кислота) Вредны или полезны сладкие газированные напитки
Вредны или полезны сладкие газированные напитки Качественный анализ и его методы
Качественный анализ и его методы Образование растворов ВМС
Образование растворов ВМС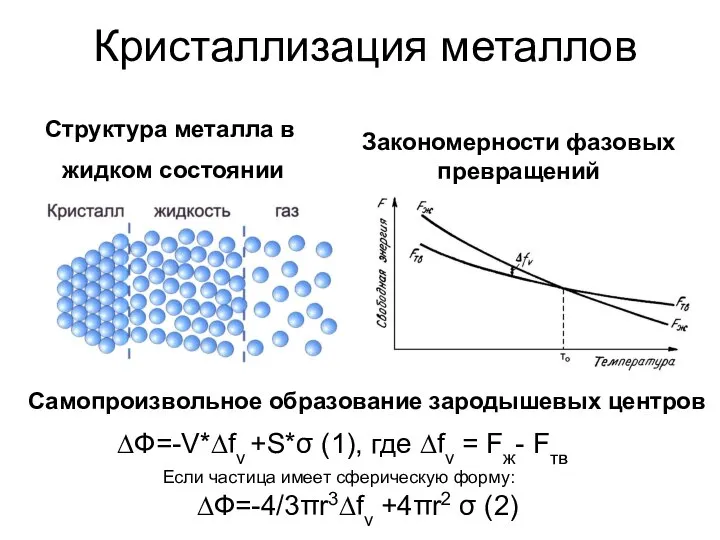 Закономерности фазовых превращений
Закономерности фазовых превращений Химические элементы космоса.
Химические элементы космоса. Шлюмберже Бұрғылау жабдығы және жөндеу (БЖ жәнеЖ) Джалал Каримов Атырау 2 шілде, 2013
Шлюмберже Бұрғылау жабдығы және жөндеу (БЖ жәнеЖ) Джалал Каримов Атырау 2 шілде, 2013 Соли
Соли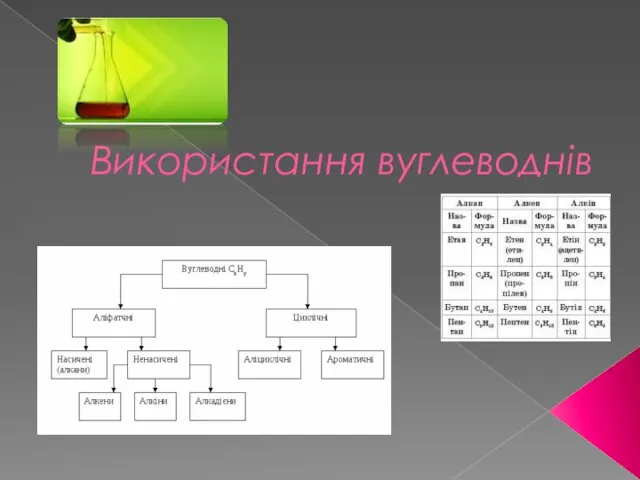 Використання вуглеводнів
Використання вуглеводнів Должностные обязанности Инструкции по ТБ и ОТ Реактивы Паспорт кабинета химии
Должностные обязанности Инструкции по ТБ и ОТ Реактивы Паспорт кабинета химии Полісахариди харчових продуктів і їх властивості. Лекція 4
Полісахариди харчових продуктів і їх властивості. Лекція 4 Технологии создания и обработки кристаллических материалов
Технологии создания и обработки кристаллических материалов Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Исследование воздействия плазмы метана на свойства оксида графена
Исследование воздействия плазмы метана на свойства оксида графена Термодинамика химических процессов
Термодинамика химических процессов History of radioactivity
History of radioactivity