Содержание
- 2. Ацетилен — органическое соединение, непредельный углеводород C2H2. Имеет тройную связь между атомами углерода, принадлежит к классу
- 3. Физические свойства При нормальных условиях — бесцветный газ, легче воздуха. Чистый 100 % ацетилен не обладает
- 4. Химические свойства цетилен с водой, в присутствии солей ртути и других катализаторов, образует уксусный альдегид (реакция
- 5. Применение Ацетилен используют: для газовой сварки и резки металлов, как источник очень яркого, белого света в
- 6. Получение
- 8. Скачать презентацию
Слайд 2
Ацетилен — органическое соединение, непредельный углеводород C2H2. Имеет тройную связь между
Ацетилен — органическое соединение, непредельный углеводород C2H2. Имеет тройную связь между
атомами углерода, принадлежит к классу алкинов. При нормальных условиях — бесцветный газ.
Слайд 3
Физические свойства
При нормальных условиях — бесцветный газ, легче воздуха. Чистый 100
Физические свойства
При нормальных условиях — бесцветный газ, легче воздуха. Чистый 100
% ацетилен не обладает запахом, однако технический ацетилен содержит примеси, которые придают ему резкий запах[5]. Малорастворим в воде, хорошо растворяется в ацетоне. Температура кипения −83,6 °C[6]. Тройная точка −80,55 °C при давлении 961,5 мм рт. ст., критическая точка 35,18 °C при давлении 61,1 атм[7].
Ацетилен требует большой осторожности при обращении. Может взрываться от удара, при нагреве до 500 °C или при сжатии выше 0,2 МПа[8] при комнатной температуре. Струя ацетилена, выпущенная на открытый воздух, может загореться от малейшей искры, в том числе от разряда статического электричества с пальца руки. Для хранения ацетилена используются специальные баллоны, заполненные пористым материалом, пропитанным ацетоном[9].
Ацетилен обнаружен на Уране и Нептуне.
Ацетилен требует большой осторожности при обращении. Может взрываться от удара, при нагреве до 500 °C или при сжатии выше 0,2 МПа[8] при комнатной температуре. Струя ацетилена, выпущенная на открытый воздух, может загореться от малейшей искры, в том числе от разряда статического электричества с пальца руки. Для хранения ацетилена используются специальные баллоны, заполненные пористым материалом, пропитанным ацетоном[9].
Ацетилен обнаружен на Уране и Нептуне.
Слайд 4
Химические свойства
цетилен с водой, в присутствии солей ртути и других катализаторов,
Химические свойства
цетилен с водой, в присутствии солей ртути и других катализаторов,
образует уксусный альдегид (реакция Кучерова). В силу наличия тройной связи, молекула высокоэнергетична и обладает большой удельной теплотой сгорания — 14000 ккал/м³ (50,4 МДж/кг). При сгорании в кислороде температура пламени достигает 3150 °C. Ацетилен может полимеризироваться в бензол и другие органические соединения (полиацетилен, винилацетилен). Для полимеризации в бензол необходим графит и температура в ~500 °C. В присутствии катализаторов, например, трикарбонил(трифенилфосфин)никеля, температуру реакции циклизации можно снизить до 60-70 °C.
Кроме того, атомы водорода ацетилена относительно легко отщепляются в виде протонов, то есть он проявляет кислотные свойства. Так, ацетилен вытесняет метан из эфирного раствора метилмагнийбромида (образуется содержащий ацетиленид-ион раствор), образует нерастворимые взрывчатые осадки с солями серебра и одновалентной меди.
Кроме того, атомы водорода ацетилена относительно легко отщепляются в виде протонов, то есть он проявляет кислотные свойства. Так, ацетилен вытесняет метан из эфирного раствора метилмагнийбромида (образуется содержащий ацетиленид-ион раствор), образует нерастворимые взрывчатые осадки с солями серебра и одновалентной меди.
Слайд 5
Применение
Ацетилен используют:
для газовой сварки и резки металлов,
как источник очень яркого,
Применение
Ацетилен используют:
для газовой сварки и резки металлов,
как источник очень яркого,
белого света в автономных светильниках, где он получается реакцией карбида кальция и воды (см. карбидная лампа),
в производстве взрывчатых веществ (см. ацетилениды),
для получения уксусной кислоты, этилового спирта, растворителей, пластических масс, каучука, ароматических углеводородов.
для получения технического углерода
в атомно-абсорбционной спектрофотометрии при пламенной атомизации
в ракетных двигателях (вместе с аммиаком)
в производстве взрывчатых веществ (см. ацетилениды),
для получения уксусной кислоты, этилового спирта, растворителей, пластических масс, каучука, ароматических углеводородов.
для получения технического углерода
в атомно-абсорбционной спектрофотометрии при пламенной атомизации
в ракетных двигателях (вместе с аммиаком)
Слайд 6
Получение
Получение
- Предыдущая
Спряжение глаголовСледующая -
Рынок, как система экономических отношений




 Презентация по Химии "Моносахариды" - скачать смотреть
Презентация по Химии "Моносахариды" - скачать смотреть  Алмаз. Внутренняя структура алмаза
Алмаз. Внутренняя структура алмаза Основы химической термодинамики
Основы химической термодинамики Основы теории смазывания и стандарты качества моторных масел
Основы теории смазывания и стандарты качества моторных масел Химический практикум для олимпиадной команды. Количественный анализ
Химический практикум для олимпиадной команды. Количественный анализ Қызықты химия
Қызықты химия Занимательная химия на кухне
Занимательная химия на кухне Мәктәптә-химия атналыгы
Мәктәптә-химия атналыгы Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями
Кристалічна ґрадка. Встановити взаємозв’язок між будовою речовин та їх фізичними властивостями Полимеры
Полимеры Биохимия соединительной ткани
Биохимия соединительной ткани Тема : Спирты Презентация по химии Ученицы 11 «Б» класса ЗОШ №41 Зануды Татьяны
Тема : Спирты Презентация по химии Ученицы 11 «Б» класса ЗОШ №41 Зануды Татьяны  Ионообменная хроматография
Ионообменная хроматография Материаловедение. Химические волокна (7 класс)
Материаловедение. Химические волокна (7 класс) Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Жевательная резинка польза или вред
Жевательная резинка польза или вред КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Взаимосвязь
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ Лекция по теме: «Взаимосвязь Современные химические технологии
Современные химические технологии ТЕМА УРОКА:
ТЕМА УРОКА: Природні і супутні нафтові гази Виконала учениця 4-Б курсу Слободяник Єлизавета
Природні і супутні нафтові гази Виконала учениця 4-Б курсу Слободяник Єлизавета  Углеводороды. Химический диктант
Углеводороды. Химический диктант Липиды. Содержание липидов в клетках
Липиды. Содержание липидов в клетках Распределение электронов в атомах. Энергетические уровни
Распределение электронов в атомах. Энергетические уровни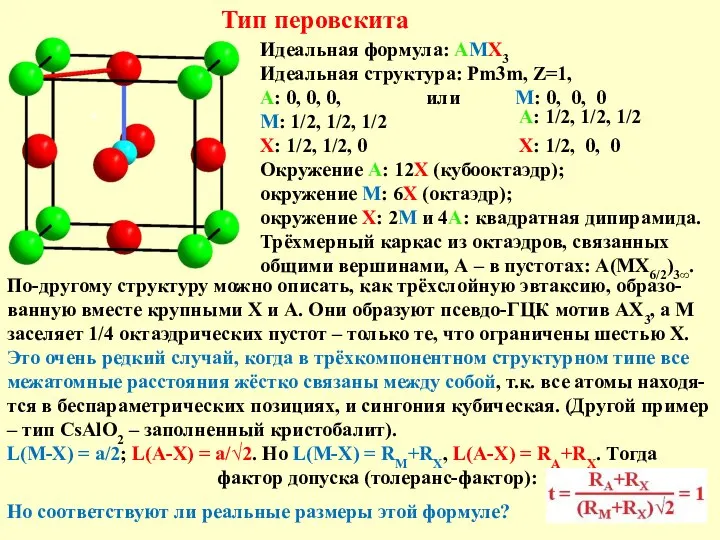 Тип перовскита
Тип перовскита Нитрид индия – новый материал для оптоэлектроники
Нитрид индия – новый материал для оптоэлектроники Мыло и мыловарение
Мыло и мыловарение Алкены. Строение, номенклатура, изомерия, физические и химические свойства алкенов
Алкены. Строение, номенклатура, изомерия, физические и химические свойства алкенов Качественное и количественное определение содержания аскорбиновой кислоты в продуктах питания
Качественное и количественное определение содержания аскорбиновой кислоты в продуктах питания