Содержание
- 2. Цель урока: Продолжить формирование представлений учащихся об изомерии и номенклатуре органических веществ, умений составлять структурные формулы
- 3. Задачи: Обучающие:- обобщение и систематизация знаний по теме «Алкины»;- выявление уровня усвоения основных понятий, правил; проверка
- 4. Сегодня на уроке вы узнаете: Понятие о непредельных углеводородах. Характеристика тройной связи. Изомерия и номенклатура алкинов.
- 5. Понятие об алкинах Алкины – углеводороды, содержащие в молекуле одну тройную связь между атомами углерода, а
- 6. Характеристика тройной связи Вид гибридизации – sp Валентный угол – 180 Длина связи С = С
- 7. Схема образования sp -гибридных орбиталей
- 8. Схема образования sp -гибридных орбиталей
- 9. Номенклатура алкинов. (Согласно международной номенклатуре названия ацетиленовых углеводородов производят от соответствующего алкана с заменой суффикса –ан
- 10. Гомологический ряд алкинов C2H2 C3H4 C4H6 C5H8 C6H10 C7H12 Этин Пропин Бутин Пентин Гексин Гептин
- 11. Изомерия алкинов Структурная изомерия 1. Изомерия положения тройной связи (начиная с С4Н6): СН ≡С−СН2−СН3 СН3−С≡С−СН3 бутин-1
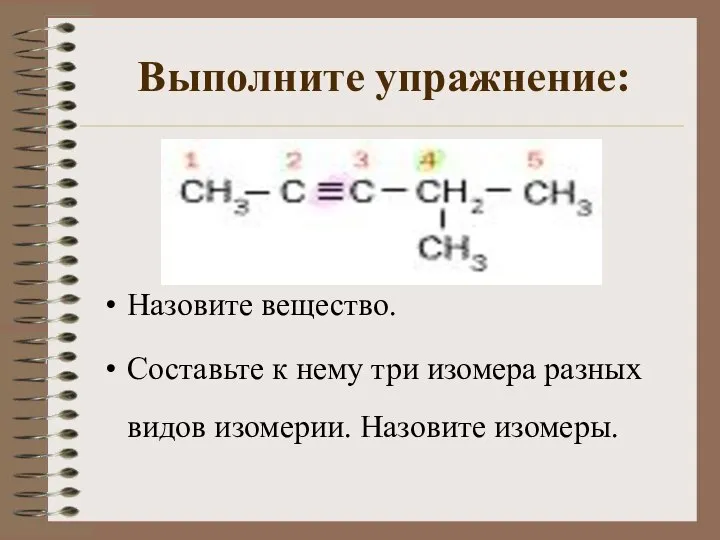
- 12. Выполните упражнение: Назовите вещество. Составьте к нему три изомера разных видов изомерии. Назовите изомеры.
- 13. Реакции присоединения 1. Галогенирование Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды
- 15. Скачать презентацию











 Физико-химия поверхностных явлений. Основы адсорбционной терапии
Физико-химия поверхностных явлений. Основы адсорбционной терапии Класифікація неорганічних сполук
Класифікація неорганічних сполук Уроки зельеварения. Задача 6
Уроки зельеварения. Задача 6 Предмет, задачи, понятия, законы химии
Предмет, задачи, понятия, законы химии Термодинамические свойства газов
Термодинамические свойства газов Химическое равновесие. Необратимые и обратимые реакции
Химическое равновесие. Необратимые и обратимые реакции Морфология тел полезных ископаемых
Морфология тел полезных ископаемых Презентация по Химии "Белки" - скачать смотреть бесплатно_
Презентация по Химии "Белки" - скачать смотреть бесплатно_ Применение аммиака и солей аммония
Применение аммиака и солей аммония Кислотно-основные равновесия
Кислотно-основные равновесия Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Презентация по химии на тему: «Применение кислорода»
Презентация по химии на тему: «Применение кислорода» Перманганат калия
Перманганат калия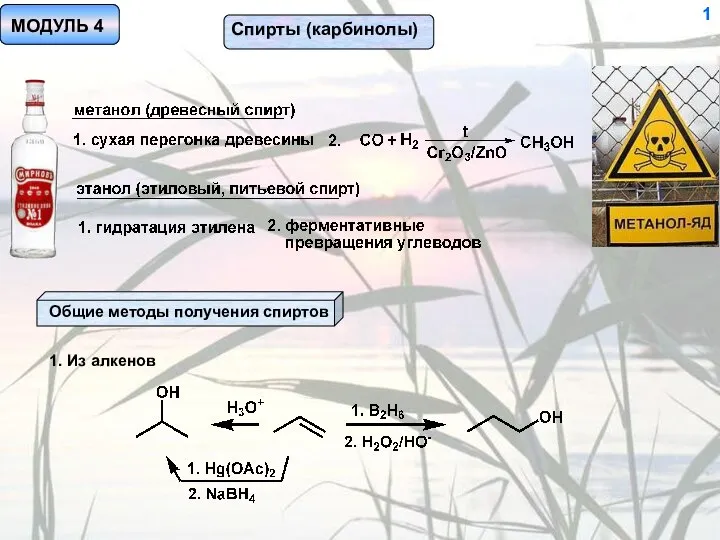 Спирты (карбинолы)
Спирты (карбинолы) Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования
Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования Отраслевые стандарты качества лекарственных средств: GMP, GLP, GSP, GDP, GPP, GCP и другие
Отраслевые стандарты качества лекарственных средств: GMP, GLP, GSP, GDP, GPP, GCP и другие Обмен веществ. Метаболизм и его функции
Обмен веществ. Метаболизм и его функции Идентификация органических веществ
Идентификация органических веществ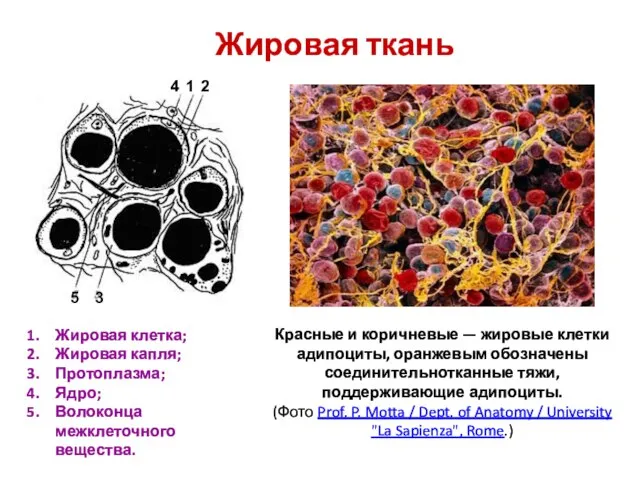 Жировая ткань
Жировая ткань Презентация по Химии "Анализ тенденций развития химии" - скачать смотреть
Презентация по Химии "Анализ тенденций развития химии" - скачать смотреть  Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық
Ауылшаруашылық дақылдарының тұқымдарын фунгецидтермен улау және химиялық қорғау тәсілдерінің биологиялық Кольорові метали
Кольорові метали 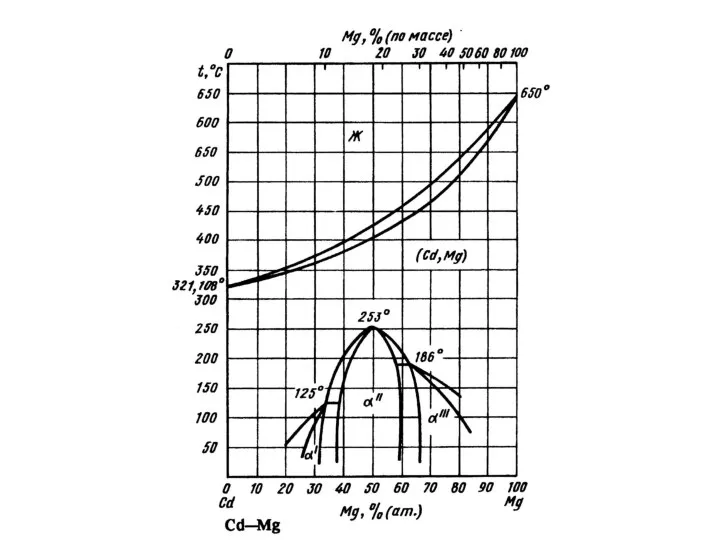 Промежуточные фазы
Промежуточные фазы Смеси и растворы
Смеси и растворы Липидтердің метаболизмі
Липидтердің метаболизмі Аттестационная работа. Образовательная программа элективного курса Химия вокруг нас
Аттестационная работа. Образовательная программа элективного курса Химия вокруг нас В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми
В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми  ЕГЭ по химии
ЕГЭ по химии