Содержание
- 2. Историческая справка Еще в древности арабские алхимики из оазиса Амон, находившегося посредине ливийской пустыни, получали бесцветные
- 3. Тема урока «Можно не любить химию, но прожить без неё сегодня и завтра нельзя» О.М.Нефёдов Аммиак
- 4. Состав вещества Строение Свойства Применение Получение аммиак
- 5. Цель урока: - изучить строение аммиака , -доказать как строение отражается на его свойствах, -разобрать способы
- 6. NH3 молекулярная формула N электронная формула структурная формула H H H
- 7. Строение Есть возможность образовать связь по донорно – акцепторному механизму Вид связи - ковалентная полярная N
- 8. Форма молекулы аммиака
- 10. Как строение молекулы отражается на свойствах?
- 11. Свойства физические Строение Легче воздуха Хорошо растворим в воде H2O NH3 Молекулярная кристаллическая решетка
- 12. В растворе аммиака фенофталеин - малиновый
- 14. Свойства химические Строение Допишите уравнения реакции, составьте электронный баланс, укажите окислитель и восстановитель. Запишите уравнения реакции
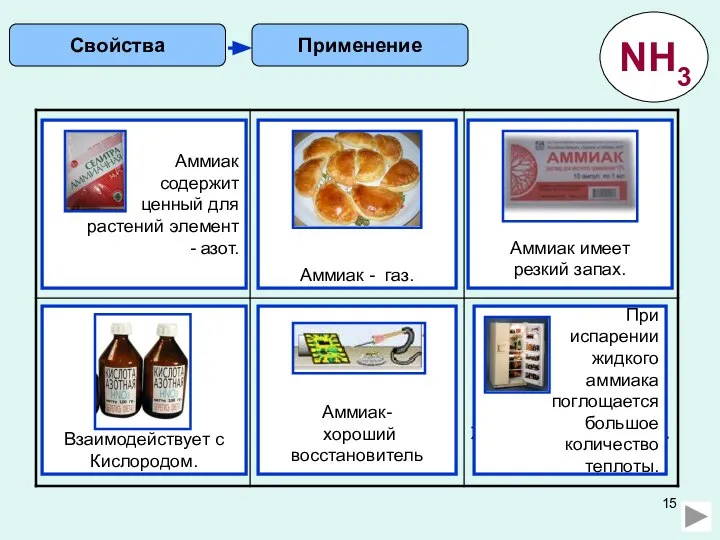
- 15. Применение Свойства
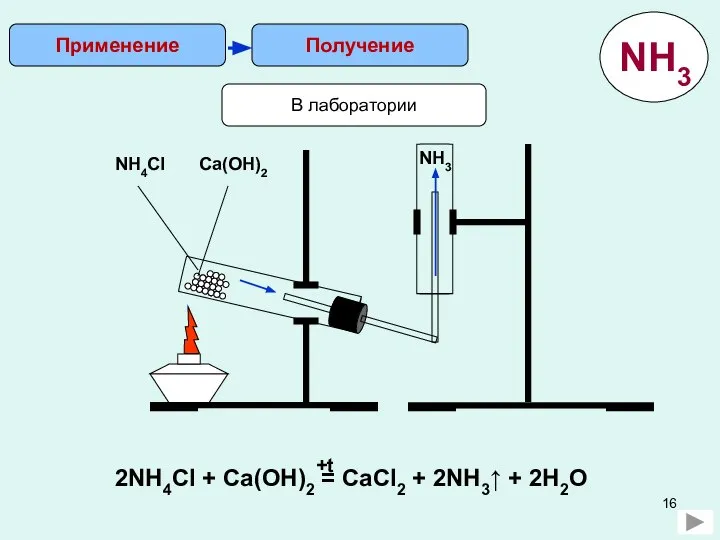
- 16. Получение Применение В лаборатории NH4Cl Ca(OH)2 NH3
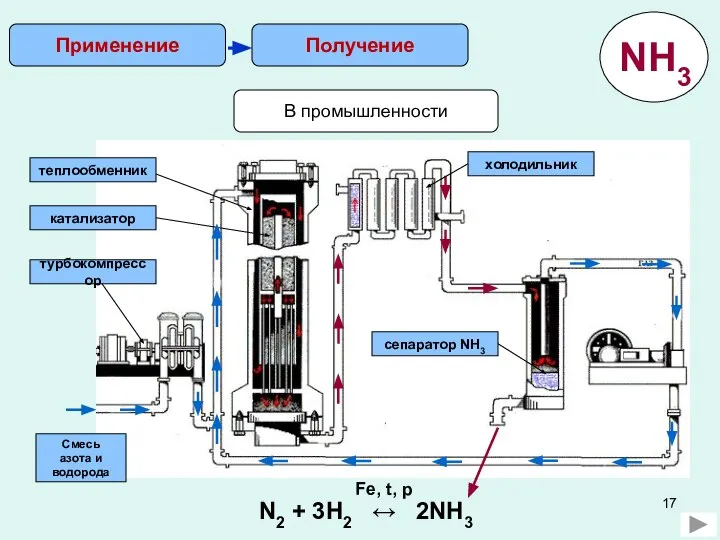
- 17. В промышленности Получение Применение Смесь азота и водорода турбокомпрессор катализатор теплообменник холодильник сепаратор NH3
- 18. Подведем итоги. 1.АММИАК – легкий газ с резким запахом. 2. АММИАК – слабое неорганическое основание. Причина
- 20. Скачать презентацию














 Ion exchange
Ion exchange Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск
Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск Презентація на тему: “Поняття про полімери на прикладі поліетилену”
Презентація на тему: “Поняття про полімери на прикладі поліетилену”  Соли и классы химических веществ
Соли и классы химических веществ Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Строение углеводородов
Строение углеводородов Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов
Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов Водород
Водород  Валентність
Валентність  Ферроцен. Свойства, получение и применение
Ферроцен. Свойства, получение и применение Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу
Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу Изотермический распад переохлажденного аустенита
Изотермический распад переохлажденного аустенита Презентация по Химии "«Химические волокна»" - скачать смотреть
Презентация по Химии "«Химические волокна»" - скачать смотреть  Три кити нанохімії
Три кити нанохімії Гiдроксикислоти. Номенклатура
Гiдроксикислоти. Номенклатура Комплексные соединения
Комплексные соединения Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха
Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха Конструкция ферментатора
Конструкция ферментатора Электролитическая диссоциация. Устойчивость комплексных соединений
Электролитическая диссоциация. Устойчивость комплексных соединений Щелочные металлы
Щелочные металлы Низкомолекулярные биорегуляторы терпены
Низкомолекулярные биорегуляторы терпены Серная кислота H2SO4
Серная кислота H2SO4 Хроматографические методы анализа
Хроматографические методы анализа Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия
Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость
Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость