Содержание
- 2. Анодные реакции электрохимической коррозии чрезвычайно многообразны и сложны. Однако. можно выделить 7 направлений анодной реакции коррозионного
- 3. 1. гидратированные катионы металла: Me – 2e + mH2O→ [Me (H2Om)]+2 2. адсорбционную плёнку кислорода: Me
- 4. Сложность анодных процессов состоит том, что анодная реакция может протекать одновременно по двум направлениям, которые в
- 5. Каждая из перечисленных реакций протекает стадийно, в отдельных стадиях участвуют ионы коррозионной среды. Количество стадий и
- 6. Анализируя вид получающихся продуктов, можно сделать вывод, что они могут быть растворимыми и нерастворимыми в коррозионной
- 7. Состояние повышенной коррозионной стойкости металла, вызванное торможением анодного процесса за счет образования адсорбционных пленок кислорода или
- 8. Явление пассивности впервые было отмечено еще Ломоносовым, но широко изучать его начали только в 30 годы
- 9. Анодная поляризационная кривая пассивирующегося металла Модуль 5. Анодные процессы электрохимической коррозия Лекция 5.1
- 10. На анодной поляризационной кривой выделяют следующие участки: Участок АВ – область активного растворения металла с образованием
- 11. Участок ЕР – область пассивации. Растворение металла происходит с небольшой скоростью, при этом на металле протекают
- 12. При потенциалах положительнее потенциала Епереп (потенциал перепассиваци) металл начинает растворяться с образованием сложных анионов металла: Me
- 13. Ход кривой с пассивацией во многом зависит от присутствия в электролите ионов хлора. При их наличии
- 14. До 70 годов прошлого века интенсивно шла дискуссия какие продукты ответственны за пассивность, вызванную кислород содержащими
- 15. Долговременное существование двух теорий объясняется тем, что ни одна из теорий не могла объяснить всю совокупность
- 16. Адсорбционная теория пассивности Хорошо объясняет влияние хлор-иона на пассивацию. Пассивацию в две ступени. Экспериментальные данные по
- 17. Явление пассивации с успехом используется в практике защиты металлов от коррозии. ( Al, Cu, Zn при
- 18. Чтобы проанализировать коррозионную ситуацию и оценить опасность коррозии необходимо выяснить: По какому пути идёт анодная реакция
- 19. 1 3 5 7 9 11 13 2 12 10 8 4 6 +0.2 +0.8 -1.0
- 20. 1. рН Два окислителя Н+ и О2 , продукты коррозии Fe+2 (растворимые). Коррозия очень опасна. 2.
- 21. 11,5 Окислитель О2 , продукты коррозии Fe(ОН)2 Fe(ОН)3 (нерастворимые, и упорядоченные), коррозия не опасна, железо пассивируется.
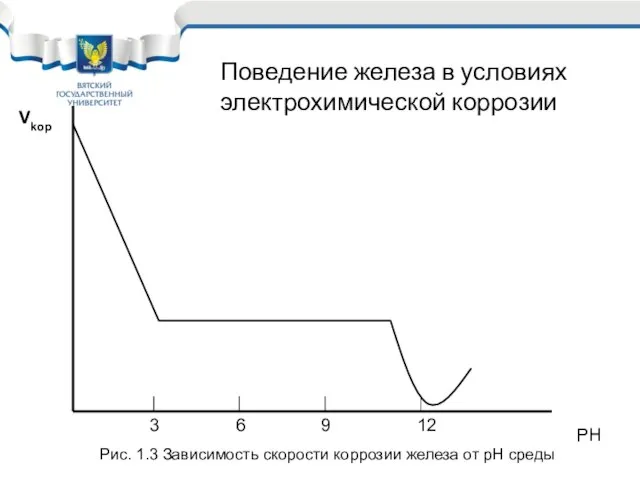
- 22. Vkop PH 3 6 9 12 Рис. 1.3 Зависимость скорости коррозии железа от рН среды Поведение
- 23. Железо, углеродистые и низколегированные стали в условиях электрохимической коррозии необходимо защищать во всех средах, кроме слабощелочных
- 24. Влияние внешних и внутренних факторов на электрохимическую коррозию
- 25. Протекторная защита Протекторная защита основана на особенностях коррозии двух металлов в контакте. Согласно теории контактной коррозии,
- 26. Анодная защита Анодная защита применяется только для металлов, склонных к пассивации в коррозионной среде. Она сводится
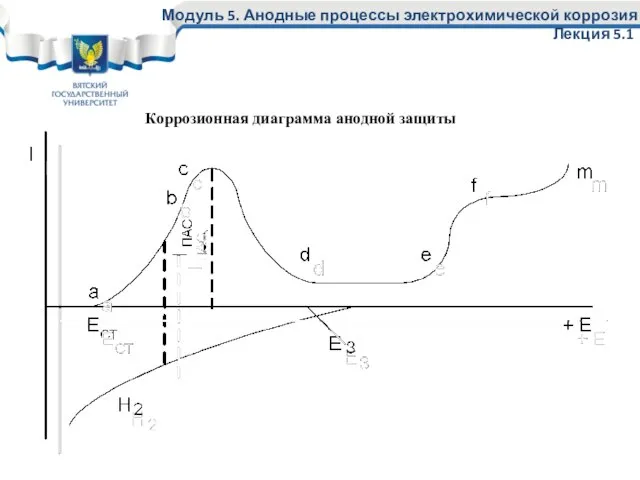
- 27. Коррозионная диаграмма анодной защиты Модуль 5. Анодные процессы электрохимической коррозия Лекция 5.1
- 28. Модуль 5. Анодные процессы электрохимической коррозия Лекция 5.1
- 29. Модуль 5. Анодные процессы электрохимической коррозия Лекция 5.1
- 31. Скачать презентацию

![1. гидратированные катионы металла: Me – 2e + mH2O→ [Me (H2Om)]+2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/561256/slide-2.jpg)























 Осадочные горные породы
Осадочные горные породы Фізичні та хімічні властивості солей
Фізичні та хімічні властивості солей  Комплексные соединения
Комплексные соединения Total Syntheses of Trichorabdal A and Maoecrystal Z
Total Syntheses of Trichorabdal A and Maoecrystal Z Презентация по Химии "Кто хочет стать отличником" - скачать смотреть
Презентация по Химии "Кто хочет стать отличником" - скачать смотреть  Каталитический синтез нуклеозидов и других пребиотических производных формамида при протонном облучении метеоритов
Каталитический синтез нуклеозидов и других пребиотических производных формамида при протонном облучении метеоритов Тема урока "Основания" - презентация_
Тема урока "Основания" - презентация_ Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Урок по химии в 10 классе по теме Каучуки
Урок по химии в 10 классе по теме Каучуки Презентация по Химии "Основы" - скачать смотреть бесплатно
Презентация по Химии "Основы" - скачать смотреть бесплатно Органічні сполуки: ліпіди
Органічні сполуки: ліпіди Алкадиены. Состав и строение
Алкадиены. Состав и строение Химики на службе у дорог
Химики на службе у дорог Серная кислота и её свойства
Серная кислота и её свойства Презентация по Химии "РЕАКЦИИ АЛЬДЕГИДНОЙ ГРУППЫ" - скачать смотреть бесплатно
Презентация по Химии "РЕАКЦИИ АЛЬДЕГИДНОЙ ГРУППЫ" - скачать смотреть бесплатно Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Роль ионов в неживой природе и в жизни людей
Роль ионов в неживой природе и в жизни людей ФКХ-Л2 2016
ФКХ-Л2 2016 Вода: фізичні та хімічні властивості. Поширеність в природі
Вода: фізичні та хімічні властивості. Поширеність в природі Соли «Na2SO4»
Соли «Na2SO4» Химическая реакция
Химическая реакция Атомы, молекулы и ионы
Атомы, молекулы и ионы Вещества по их способности проводить электрический ток в растворах
Вещества по их способности проводить электрический ток в растворах Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Исследование воздействия плазмы метана на свойства оксида графена
Исследование воздействия плазмы метана на свойства оксида графена Значення хімії у повсякденному житті Значення хімії у побуті
Значення хімії у повсякденному житті Значення хімії у побуті  Липиды. Классификация
Липиды. Классификация ХИМИЧЕСКОЕ РАВНОВЕСИЕ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯ.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯ.