Содержание
- 2. На уроке мы: -продолжим изучать соединения азота -подробно рассмотрим свойства HNO3 -будем совершенствовать навыки написания уравнений
- 3. Химическая разминка: 1.Формула аммиака: а)NH2 б) NH4 в)NH3 г) N2 2.Аммиак: а)легче воздуха, б)тяжелее воздуха, в)не
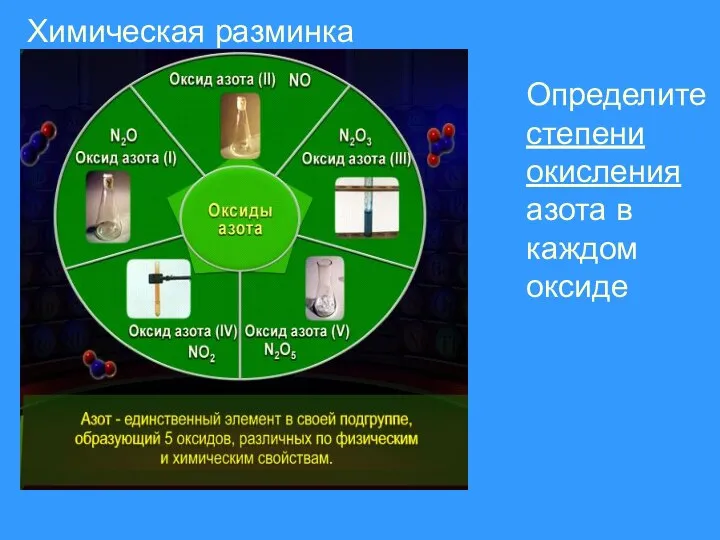
- 4. Химическая разминка Определите степени окисления азота в каждом оксиде
- 5. Азотная кислота HNO3 –одна из наиболее сильных кислот Физические свойства: -бесцветная жидкость - на воздухе «дымит»,tкип=
- 6. Получение HNO3
- 7. Химические свойства Типичные свойства кислот
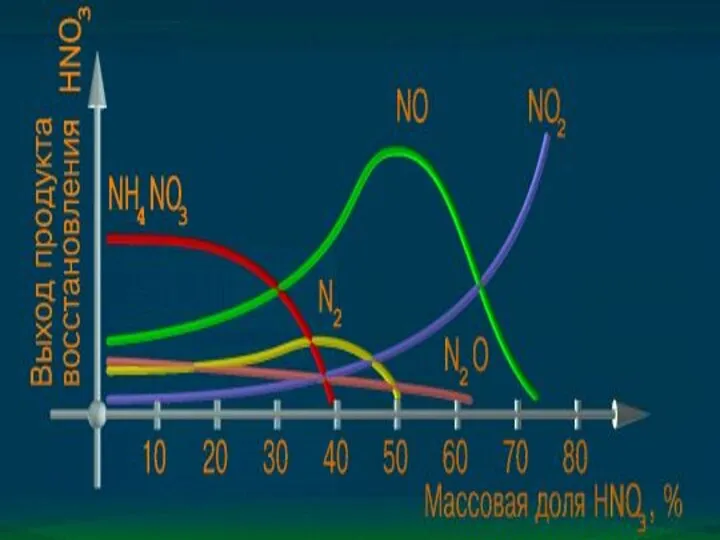
- 8. Химические свойства С металлами реагирует особо:
- 10. Химические свойства: Взаимодействие с неметаллами
- 11. Для любознательных:
- 12. Применение солей HNO3 -в сельском хозяйстве -для крашения тканей -в медицине -в пиротехнике
- 13. Проверь себя: Степень окисления азота в HNO3 а)-3 б)0 в)+5 г)+4 При хранении на свету HNO3
- 14. Закончите предложения: -сегодня на уроке я узнал… -я потренировался… -я увидел…
- 16. Скачать презентацию











 Цікаві факти про Харчові добавки Презентація Гладкіх Ксенії Учениці 11-В класу
Цікаві факти про Харчові добавки Презентація Гладкіх Ксенії Учениці 11-В класу  Кинетика сложных реакций
Кинетика сложных реакций Карбоновые кислоты
Карбоновые кислоты Аккумуляторы и их устройство
Аккумуляторы и их устройство Химическое равновесие. Протолитические равновесия и процессы в растворах электролитов
Химическое равновесие. Протолитические равновесия и процессы в растворах электролитов Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Оксиды. Определение, состав, номенклатура, классификация и структурные формулы
Оксиды. Определение, состав, номенклатура, классификация и структурные формулы Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Минералы. Значение минералов и задачи минералогии
Минералы. Значение минералов и задачи минералогии Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Спирты. Классификация спиртов
Спирты. Классификация спиртов Лужні метали Підготувала: Анна Сідорова
Лужні метали Підготувала: Анна Сідорова  Загрязнение продуктов питания примесями, мигрирующими из оборудования, инвентаря, тары и упаковочных материалов
Загрязнение продуктов питания примесями, мигрирующими из оборудования, инвентаря, тары и упаковочных материалов Поліетелен. Застосування поліетилену
Поліетелен. Застосування поліетилену Химический элемент медь
Химический элемент медь Тема урока: Состав, переработка нефти и экологические проблемы связанные с ней.
Тема урока: Состав, переработка нефти и экологические проблемы связанные с ней. Диазины. Характеристика диазинов. (Лекция 8)
Диазины. Характеристика диазинов. (Лекция 8) Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Сульфат меди
Сульфат меди Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Понятие электродного потенциала и методы его измерения
Понятие электродного потенциала и методы его измерения Путешествие в мир углеводородов нефти
Путешествие в мир углеводородов нефти Звезды Лейденфроста
Звезды Лейденфроста Фотодыхание
Фотодыхание Уголь. Виды угля
Уголь. Виды угля Алюминий и его соединения
Алюминий и его соединения Растворы и их классификация
Растворы и их классификация МЫШЬЯК Презентацию подготовила Юдайханова Юлия Ученица 11 класса В
МЫШЬЯК Презентацию подготовила Юдайханова Юлия Ученица 11 класса В