Содержание
- 2. Электролиз Электро́лиз — физико-химический процесс, состоящий в выделении наэлектродах составных частей растворённых веществ или других веществ,
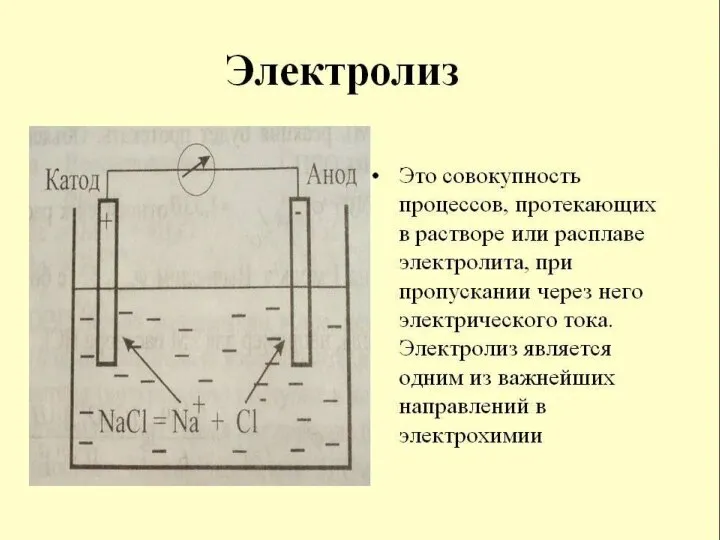
- 3. Схематическое изображение электролитической для исследования электролиза
- 5. Упорядоченное движение ионов в проводящих жидкостях происходит в электрическом поле, которое создаётся электродами — проводниками, соединёнными
- 6. В 1832 году Фарадей установил, что масса m вещества, выделившегося на электроде, прямо пропорциональна электрическому заряду
- 8. Первый закон Фарадея Масса вещества, выделяющегося на электродах, прямо пропорциональна количеству прошедшего через раствор электричества .
- 9. Второй закон Фарадея Второй закон Фарадея: При прохождении через расплав или раствор электролита 96500 Кл электричества
- 10. Электрохимический эквивалент вещества Объеденённый закон Фарадея
- 13. Электролиз в газах Электролиз в газах, при наличии ионизатора, объясняется тем, что при прохождении через них
- 14. Поляризация при электролизе Поляризация при электролизе Поляризация при электролизе складывается из собственно поляризации, которая делится на
- 15. Химическая поляризация Химическая поляризация возникает при использовании инертных электродов. Какими бы ни были инертные электроды (Pt,
- 16. Платина – анод насыщается хлором; платина – катод поглощает водород. Хлор может только восстанавливаться, водород -
- 17. Электродвижущая сила возникшего гальванического элемента направлена против внешнего напряжения и ослабляет его. Данный вид поляризации называется
- 18. Концентрационная поляризация Данная поляризация происходит при активном аноде, например, серебряном В силу диффузии ионы серебра от
- 19. Поскольку диффузия в жидкостях медленная, концентрация ионов Ag в анодном пространстве намного выше, чем в катодном.
- 21. Скачать презентацию

















 Способы разделения смесей
Способы разделения смесей Электрохимические методы обработки металлов
Электрохимические методы обработки металлов Адам мен жануар организміне бордың әсері
Адам мен жануар организміне бордың әсері Эфирные масла
Эфирные масла Мыла и синтетические моющие средства
Мыла и синтетические моющие средства Одноатомные спирты
Одноатомные спирты ЕГЭ. Химия. Содержательный блок Химический элемент. Вопрос А1, А 2
ЕГЭ. Химия. Содержательный блок Химический элемент. Вопрос А1, А 2 Известные ученые и их открытия
Известные ученые и их открытия Радиоактивные элементы почв
Радиоактивные элементы почв Производство сульфата аммония (лекция)
Производство сульфата аммония (лекция) Липиды. Насыщенные и ненасыщенные жирные кислоты
Липиды. Насыщенные и ненасыщенные жирные кислоты Акарицидтер. Тетразиндер. Бензи-латтар. Сульфоқышқыл туындылары. Хина-золиндер . Пирозолдар. Пиридазипондар
Акарицидтер. Тетразиндер. Бензи-латтар. Сульфоқышқыл туындылары. Хина-золиндер . Пирозолдар. Пиридазипондар Вспененные полимерные материалы. Классификация и принцип действия вспенивателей
Вспененные полимерные материалы. Классификация и принцип действия вспенивателей Методы защиты металлов от электрохимической коррозии
Методы защиты металлов от электрохимической коррозии Презентация по Химии "Атом" - скачать смотреть
Презентация по Химии "Атом" - скачать смотреть  Алюминий (лат. Aluminium)
Алюминий (лат. Aluminium) Кристаллические решетки
Кристаллические решетки Люди отличающиеся от нас
Люди отличающиеся от нас Общая характеристика углерода
Общая характеристика углерода Антиоксиданты – антоцианы плодов аронии черноплодной
Антиоксиданты – антоцианы плодов аронии черноплодной Ферменттер. Ферментативті катализдің механизмі. Ферменттердің жіктелуі
Ферменттер. Ферментативті катализдің механизмі. Ферменттердің жіктелуі Вольфрам және молибден
Вольфрам және молибден Молекулярные массы и гибкость полимеров
Молекулярные массы и гибкость полимеров Основные классы неорганических соединений
Основные классы неорганических соединений Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А. Синтетические красители
Синтетические красители Презентация по Химии "Реакции ионного обмена" - скачать смотреть
Презентация по Химии "Реакции ионного обмена" - скачать смотреть  Низкомолекулярные биорегуляторы терпены
Низкомолекулярные биорегуляторы терпены