Содержание
- 4. 1. O 49,5 % (масс.) 15. S 0,048 % 60. Se 8·10–5 % 74. Te 1·10–6
- 5. История открытия кислорода Кислород: 1772-1774 гг., Дж. Пристли, К. Шееле, А.Л. Лавуазье (название элемента) Термическое разложение
- 6. История открытия Se, Te, Po Теллур открыл в 1782 г. Ф. Мюллер фон Райхенштайн (название дал
- 7. Простые вещества Аллотропия: O2, O3 (озон) S8(ромбич.), S8 (монокл.), S6, S4, Sx (пластич.), S2 Se красн.
- 9. Взаимодействие с водой, кислотами и щелочами O2, S(т), Se(т), Te(т) + H2O(ж) ≠ 3S + 2H2O
- 10. Соединения Э–II H2O H2S H2Se H2Te ΔG °, кДж/моль –229 –34 +16 +85 Kк (H2Э/HЭ–, водн.
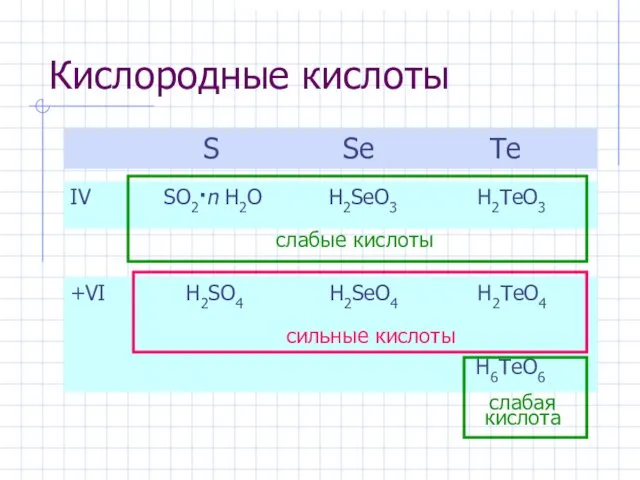
- 11. Кислородные кислоты S Se Te IV SO2·n H2O H2SeO3 H2TeO3 +VI H2SO4 H2SeO4 H2TeO4 H6TeO6
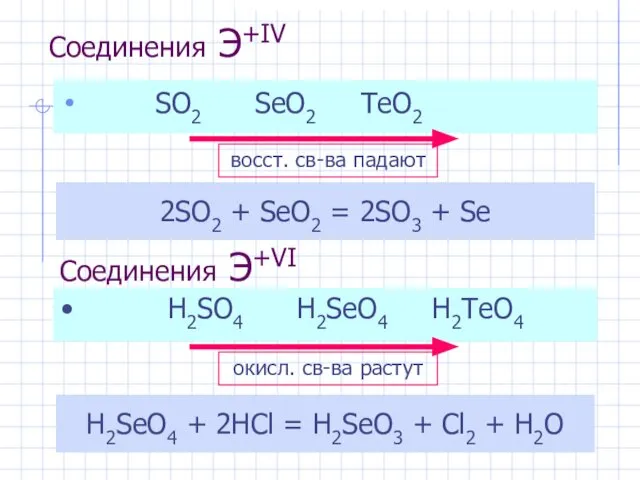
- 12. Соединения Э+IV SO2 SeO2 TeO2 2SO2 + SeO2 = 2SO3 + Se Соединения Э+VI H2SeO4 +
- 15. Физические и химические свойства O2
- 17. Озон O3 O3 – светло-синий газ, т.пл. –192,7 °С, т.кип. –111,9 °С, взрывоопасен и ядовит. В
- 18. Молекула O3 полярна и диамагнитна Обнаружение озона: 2KI + O3 + H2O = I2 + 2KOH
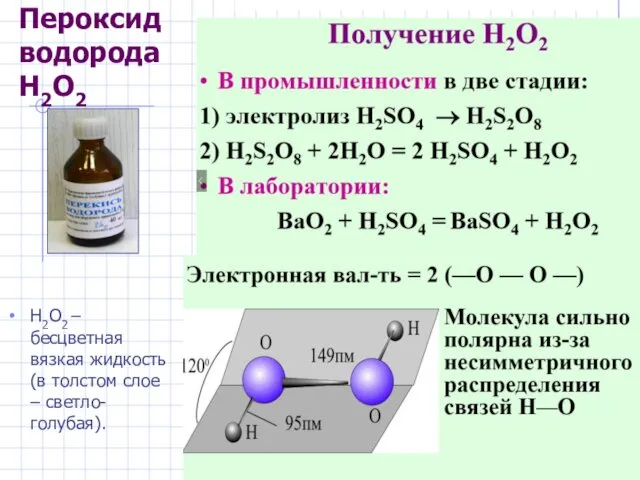
- 19. Пероксид водорода H2O2 H2O2 – бесцветная вязкая жидкость (в толстом слое – светло-голубая).
- 20. Физические свойства H2O и H2O2 Водородные связи: H2O ··· H2O ··· H2O ··· H2O ··· H2O
- 21. Пероксид водорода H2O2 Дисмутация в присутствии катализаторов (например MnO2): 2H2O2–I = 2H2O–II + O20↑ Видеофрагмент Окислительные
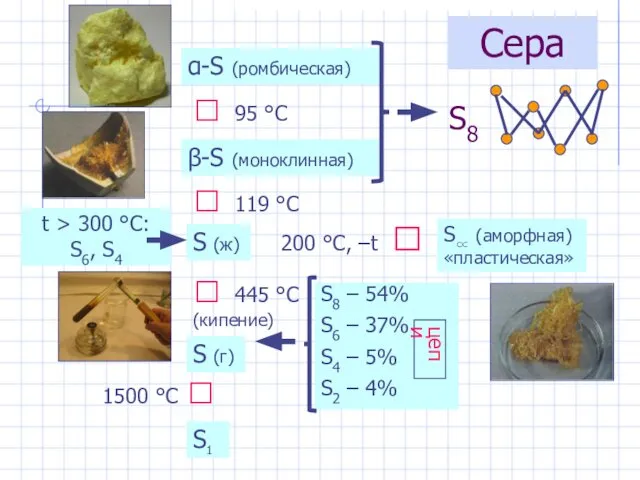
- 24. Сера α-S (ромбическая) β-S (моноклинная) ⮃ 95 °С ⮃ 119 °С S (ж) ⮃ 445 °С
- 25. Шкала степеней окисления серы SO3, SO42−, HSO4−, H2SO4, K2SO4, SF6, SCl2O2 SO2, SO32−, HSO3−, SO2·n H2O,
- 26. Сера: химические свойства S
- 27. Химические свойства серы и получение
- 28. H2S
- 33. Скачать презентацию


























 Квантовая химия
Квантовая химия IV группа главная подгруппа Углерод
IV группа главная подгруппа Углерод Метод комплесонометрии
Метод комплесонометрии Химические процессы в атмосфере. Загрязнение атмосферы. Причины и последствия
Химические процессы в атмосфере. Загрязнение атмосферы. Причины и последствия Вода и растворы. Лекция 3
Вода и растворы. Лекция 3 Презентация по Химии "Определение рода вещества (жидкости) по его плотности" - скачать смотреть
Презентация по Химии "Определение рода вещества (жидкости) по его плотности" - скачать смотреть  Закон постоянства состава веществ
Закон постоянства состава веществ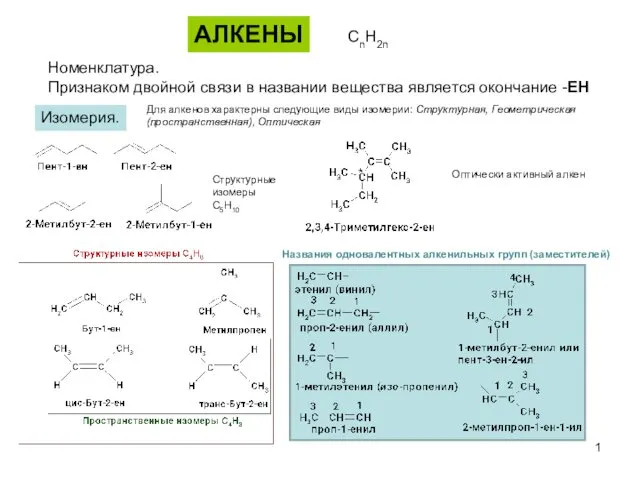 Алкены
Алкены Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение
Карбоновые кислоты. Изомерия. Физические, химические свойства. Получение, применение Химия в медицине
Химия в медицине Углеводы. Моносахариды
Углеводы. Моносахариды Electrochemistry. (Chapter 6)
Electrochemistry. (Chapter 6) Біохімічний рівень організації
Біохімічний рівень організації Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные An introduction to bonding
An introduction to bonding Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Сульфатна кислота
Сульфатна кислота  Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания
Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания Презентация по Химии "Этот многоликий Кальцит" - скачать смотреть
Презентация по Химии "Этот многоликий Кальцит" - скачать смотреть  Композиционные материалы. Материалы порошковой металлургии: пористые, конструкционные, электротехнические
Композиционные материалы. Материалы порошковой металлургии: пористые, конструкционные, электротехнические Гравиметрический метод анализа
Гравиметрический метод анализа Протолитические равновесия в растворах электролитах
Протолитические равновесия в растворах электролитах Хімічна і біологічна зброя Виконала: учениця 10-ФМ класу Сосєдка Катерина
Хімічна і біологічна зброя Виконала: учениця 10-ФМ класу Сосєдка Катерина  Классическая теория гармонического кристалла. Гармоническое приближение. Адиабатическое приближение
Классическая теория гармонического кристалла. Гармоническое приближение. Адиабатическое приближение Ионный обмен или сорбция
Ионный обмен или сорбция Природные источники углеводородов
Природные источники углеводородов Липиды. Переваривание, всасывание, транспорт. (Лекция 8)
Липиды. Переваривание, всасывание, транспорт. (Лекция 8) Продукти її виробництва
Продукти її виробництва