Содержание
- 2. Возникновение органической химии как науки.
- 3. Студент должен: Знать: основы теории строения органических соединений Уметь: описывать свойства органических соединений на основе теории
- 4. Первые классификации (по происхождению):
- 5. Й. БЕРЦЕЛИУС: ВЕЩЕСТВА, ПОЛУЧАЕМЫЕ ИЗ ОРГАНИЗМОВ (РАСТИТЕЛЬНОГО И ЖИВОТНОГО ПРОИСХОЖДЕНИЯ) - ОРГАНИЧЕСКИЕ, НАУКА, ИХ ИЗУЧАЮЩАЯ -
- 6. В 1824 г. НЕМЕЦКИЙ ХИМИК Ф. ВЕЛЕР (УЧЕНИК БЕРЦЕЛИУСА) СИНТЕЗИРОВАЛ ИЗ НЕОГАНИЧЕСКИХ ВЕЩЕСТВ ЩАВЕЛЕВУЮ КИСЛОТУ. 1828
- 7. Вещества органические и не органические. Состав и некоторые свойства органических веществ.
- 8. * И ее соли содержат углерод, но не относятся к органическим веществам.
- 9. Большинство органических веществ горючи, легко разлагаются (t=400-600 С), легко взаимопревращаются. Углерод в органических веществах обнаруживают по
- 10. Органическая химия – это химия соединений углерода; химия углеводородов и их производных.
- 11. ДОСТРУКТИВНЫЕ ТЕОРИИ Теория радикалов (30 гг. XIXв. Й. Берцелиус, Ю. Либих, Ж. Дюма) А) в состав
- 12. Теория типов (30 гг. XIXв. Ш. Жерар, А. Кекуле и др.) А) все органические вещества –
- 13. Б) формулы выражают не внутреннее строение молекулы, а способы образования, свойства определяют все атомы молекулы. В)
- 14. Связь понятий теории химического строения Качественный и количественный состав Свойства Химическое строение Взаимное влияние атомов Структурная
- 15. Предпосылки возникновения теории химического строения органических веществ «Органическая химия может сейчас кого угодно свести с ума.
- 16. Основные «противоречия» органической химии: Многообразие веществ – образовано небольшим числом элементов; Кажущееся несоответствие валентности в органических
- 17. Предпосылки возникновения теории: 1.Развитие и утверждение атомистических представлений (съезд в Карлсруэ, 1860); 2.Установление понятия валентности (Э.
- 18. Теория химического строения органических соединений. Основные положения (А.М. Бутлеров 1861 – 1864 гг.)
- 19. 1. Атомы и молекулы реально существуют. Атомы в молекулах располагаются не беспорядочно, они соединены друг с
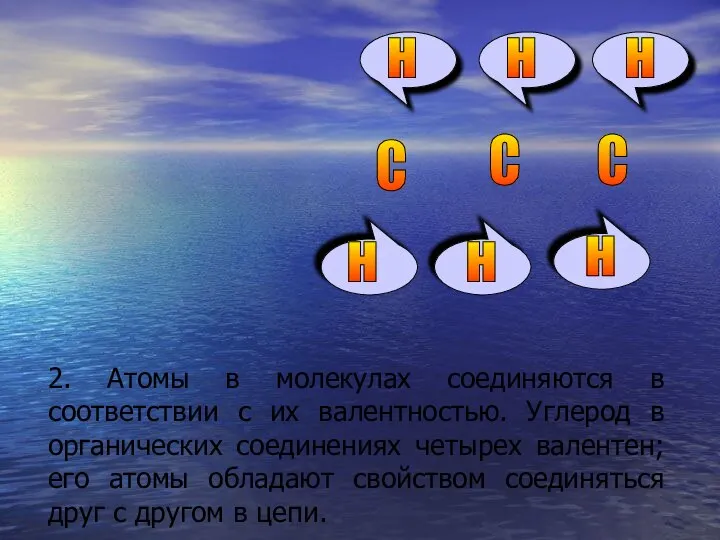
- 20. 2. Атомы в молекулах соединяются в соответствии с их валентностью. Углерод в органических соединениях четырех валентен;
- 21. А) Б) Структурная формула показывает порядок соединения атомов в молекуле, их взаимосвязь друг с другом. (а
- 22. 3. Свойства веществ зависят не только от того, атомы каких элементов и в каком количестве входят
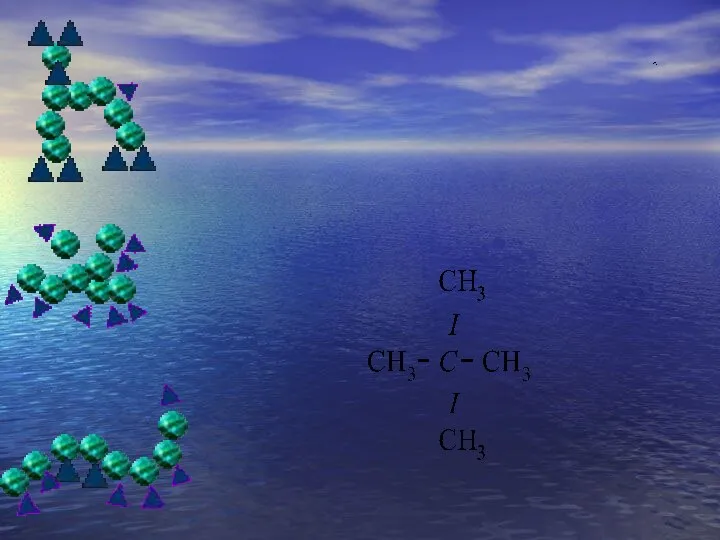
- 23. 4. Различное строение при одном и том же составе и относительной молекулярной массе вещества обуславливает явление
- 25. 5. Химическое строение молекул позноваемо. Оно может быть установлено путем синтеза из веществ известного состава и
- 26. Дальнейшее развитие теории: Изучение пространственного расположения атомов – стерео химия; Изучение органических веществ с применением электронного
- 27. Алгоритм поиска возможных изомеров алканов (изомерия углеродного скелета).
- 28. Изомер №2 Изомер №1 Изомер №3
- 29. Изомер №2 При нумерации цепи справа налево Изомер №4
- 30. Изомер №5 Изомер №4
- 31. Классификация химических реакций, типичных для органических соединений
- 32. По типу химического превращения реакции замещения сопровождаются образованием новых ковалентных связей при замещении одного атома (или
- 33. реакции присоединения (синтеза) сопровождаются образованием новых б (сигма) - связей за счет разрыва π (пи) -
- 34. реакции разложения сопровождаются образованием новых более простых по составу молекул.
- 35. По способу разрыва связи реакции с образованием радикалов сопровождаются симметричным разрывом связи (гомолитический разрыв). Общая электронная
- 36. реакции с образованием ионов сопровождаются несимметричным разрывом связи (гетеролитический разрыв). Общая электронная пара остается у одного
- 37. КЛАССИФИКАЦИЯ УГЛЕВОДОРОДОВ
- 39. МЕТАН. ФИЗИЧЕСКИЕ СВОЙСТВА. СТРОЕНИЕ МОЛЕКУЛЫ. СН 4 МЕТАН БОЛОТНЫЙ ГАЗ Легче воздуха Взрывоопасен!!!
- 40. Два «противоречия» в строении метана: Валентность углерода равна четырем – в наличии только 2 валентных электрона
- 41. 2. В молекуле все четыре связи одинаковые – по теории – одна ss связь и три
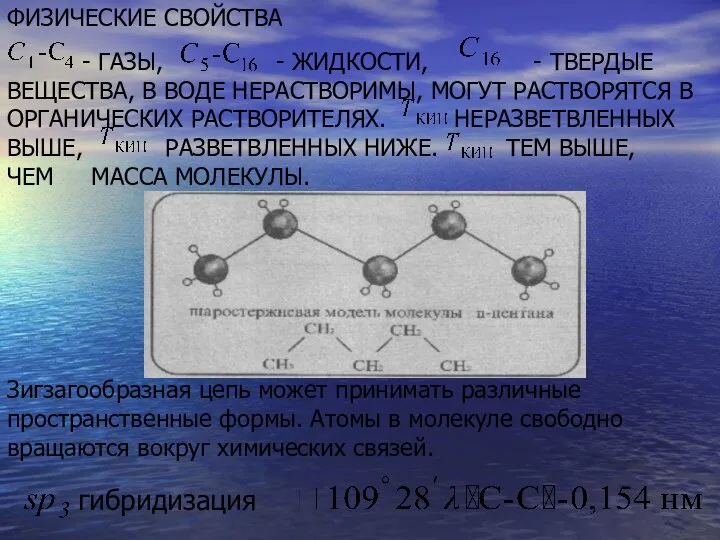
- 42. sp 3 Четыре орбитали max удаления заряженных электронных облаков составляет 0,154 нм
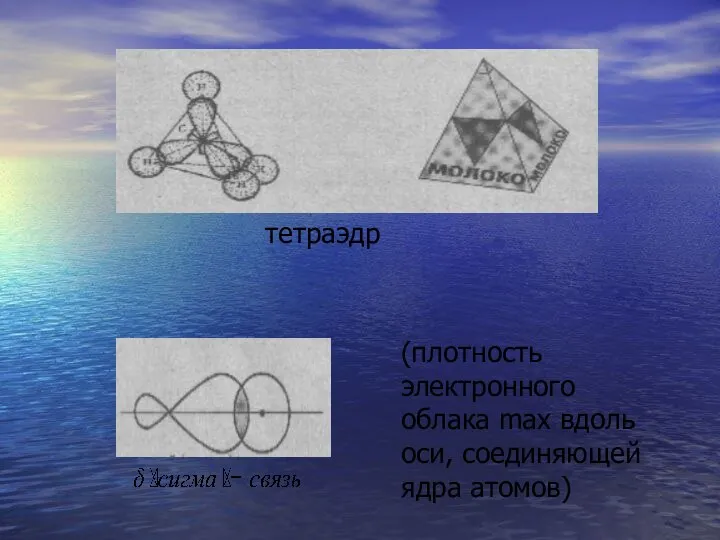
- 43. тетраэдр (плотность электронного облака max вдоль оси, соединяющей ядра атомов)
- 44. Алканы
- 45. (Предельные или насыщенные углеводороды, парафины, жирные или алифатические соединения) Соединения углерода с водородом, в молекулах которых
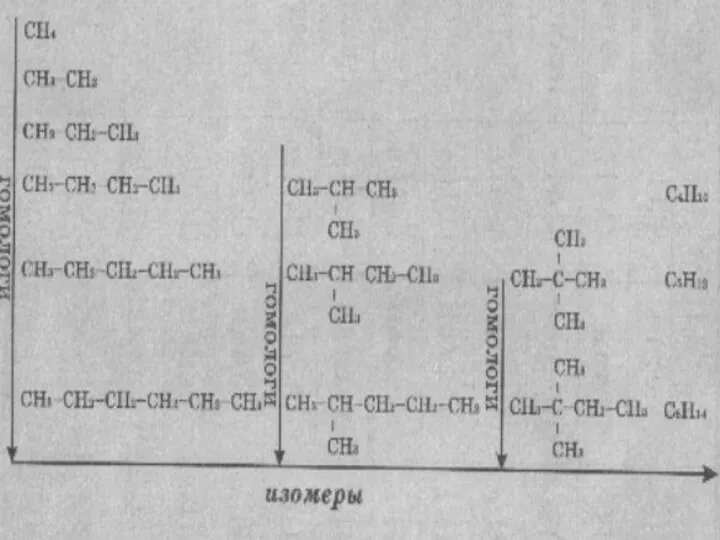
- 46. Соединения, сходные по строению и химическим свойствам и отличающиеся друг от друга на одну или несколько
- 47. ФИЗИЧЕСКИЕ СВОЙСТВА - ГАЗЫ, - ЖИДКОСТИ, - ТВЕРДЫЕ ВЕЩЕСТВА, В ВОДЕ НЕРАСТВОРИМЫ, МОГУТ РАСТВОРЯТСЯ В ОРГАНИЧЕСКИХ
- 48. Изомеры и гомологи
- 51. Алканы (неразветвленного строения) и алкины
- 52. Номенклатура Химическая номенклатура – это система формул и названий химических веществ. Она включает правила составления формул
- 53. Рациональная номенклатура Углеводороды рассматриваются как производные метана, у которого один или несколько атомов водорода замещены на
- 55. Скачать презентацию















































 Номенклатура классов неорганических соединений
Номенклатура классов неорганических соединений Химические элементы в клетках живых организмов Автор: учитель химии МКОУ «Касторенская СОШ №1», п.г.т. Касторное Парамонов А.Ю.,
Химические элементы в клетках живых организмов Автор: учитель химии МКОУ «Касторенская СОШ №1», п.г.т. Касторное Парамонов А.Ю., Презентация по Химии "Вода как жизнь" - скачать смотреть бесплатно
Презентация по Химии "Вода как жизнь" - скачать смотреть бесплатно Гибридизация орбиталей и строение молекул этана, этилена и ацетилена
Гибридизация орбиталей и строение молекул этана, этилена и ацетилена Соли. Классификация. Физические и химические свойства. Получение и применение солей
Соли. Классификация. Физические и химические свойства. Получение и применение солей Physical chemistry of nanostructured systems.( lecture no. 7)
Physical chemistry of nanostructured systems.( lecture no. 7) Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк «Смоленское Поозерье»
Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк «Смоленское Поозерье» Углерод и его соединения
Углерод и его соединения Кремний
Кремний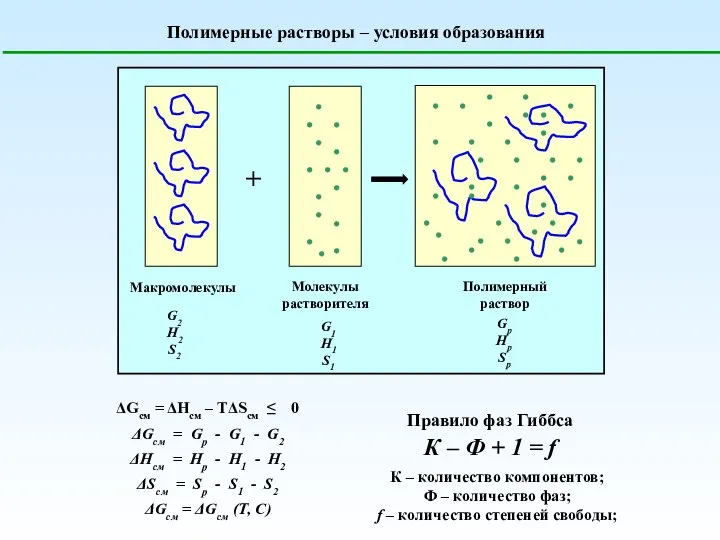 Полимерные растворы – условия образования
Полимерные растворы – условия образования Углерод
Углерод Катализаторы для синтеза лекарственных препаратов и их строительных блоков
Катализаторы для синтеза лекарственных препаратов и их строительных блоков Основы органической химии
Основы органической химии Химическое загрязнение акваторий. Основные термины и определения
Химическое загрязнение акваторий. Основные термины и определения Виникнення процесу горіння. Самозаймання речовин та матеріалів. Особливості самозаймання. Хімічне самозаймання. (Розділ 2.5.8)
Виникнення процесу горіння. Самозаймання речовин та матеріалів. Особливості самозаймання. Хімічне самозаймання. (Розділ 2.5.8) Олигосахариды и полисахариды
Олигосахариды и полисахариды Разработка способа получения аллантоина
Разработка способа получения аллантоина Химия және медицина
Химия және медицина Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Классическая теория гармонического кристалла. Гармоническое приближение. Адиабатическое приближение
Классическая теория гармонического кристалла. Гармоническое приближение. Адиабатическое приближение Синтез наноматериалов золь-гель методом. (Лекция 5)
Синтез наноматериалов золь-гель методом. (Лекция 5) Презентация по химии Стекло
Презентация по химии Стекло  Циклоалканы
Циклоалканы Химерні та трансгенні організми
Химерні та трансгенні організми  Прибор “октис-2”
Прибор “октис-2” Витамины и авитаминоз - презентация_
Витамины и авитаминоз - презентация_ Идентификация органических веществ
Идентификация органических веществ Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров)