Содержание
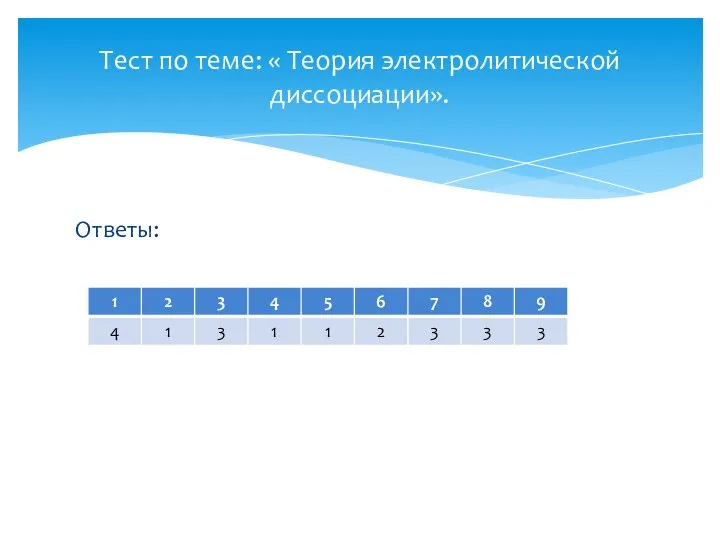
- 2. Ответы: Тест по теме: « Теория электролитической диссоциации».
- 3. Сущность гидролиза сводится к обменному химическому взаимодействию катионов или анионов соли с молекулами воды. В результате
- 4. Гидролизу не подвергается нерастворимые соли и соли, образованные сильным основанием (щёлочи) и сильной кислотой (HCl, HClO4,
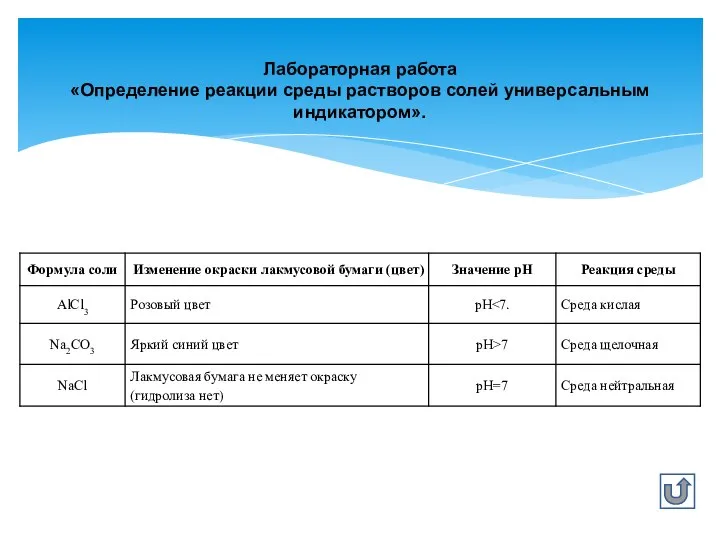
- 5. Лабораторная работа «Определение реакции среды растворов солей универсальным индикатором».
- 6. Алгоритм составления гидролиза солей Дана соль AlCl3 – образована слабым основанием и сильной кислотой.
- 7. Гидролиз соли Na2CO3, образованной сильным основанием и слабой кислотой.
- 8. Гидролиз соли СН3 СООNН4, образованной слабым основанием и слабой кислотой В случае гидролиз соли, образованной слабым
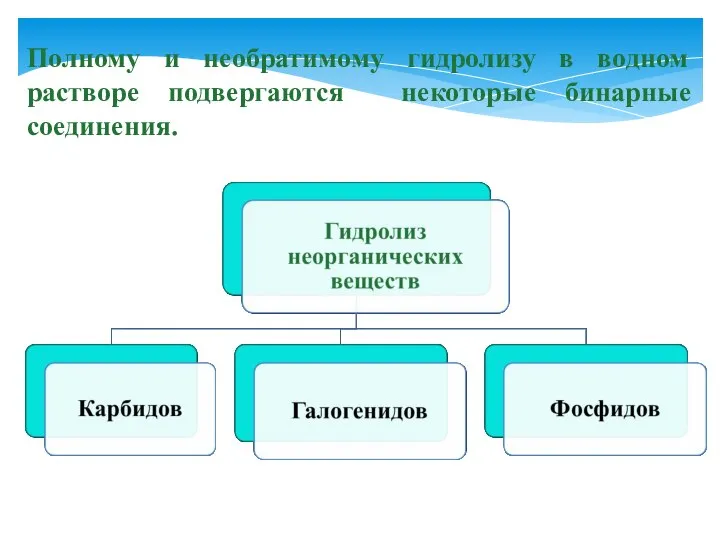
- 9. Полному и необратимому гидролизу в водном растворе подвергаются некоторые бинарные соединения.
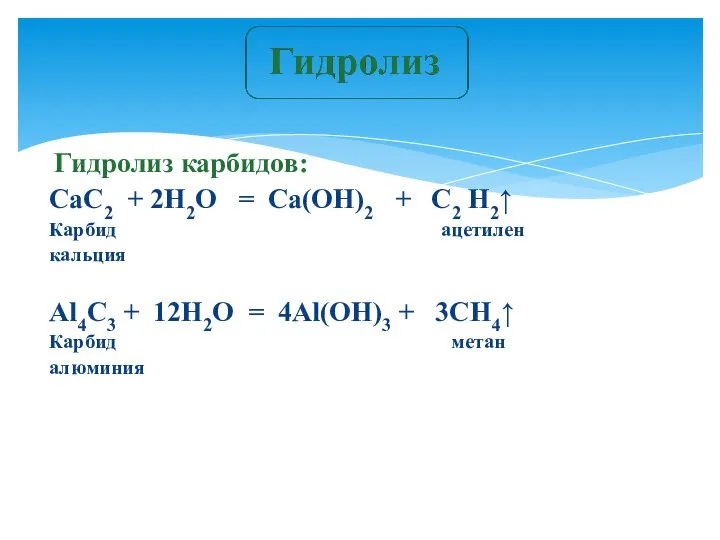
- 10. Гидролиз карбидов: CaC2 + 2H2O = Ca(OH)2 + C2 H2↑ Карбид ацетилен кальция Al4C3 + 12H2O
- 11. Гидролиз галогенидов: SiCl4 + 3H2O = H2SiO4↓ + 4HСl хлорид кремниевая кремния (+4) кислота Гидролиз фосфидов:
- 12. Для обратимого гидролиза условия смещения равновесия определяются принципом Ле Шателье. Условия усиления и ослабления гидролиза:
- 13. Разбор примера ( задание частиВ) Как скажется на состоянии химического равновесия в системе Zn2+ + H2O↔
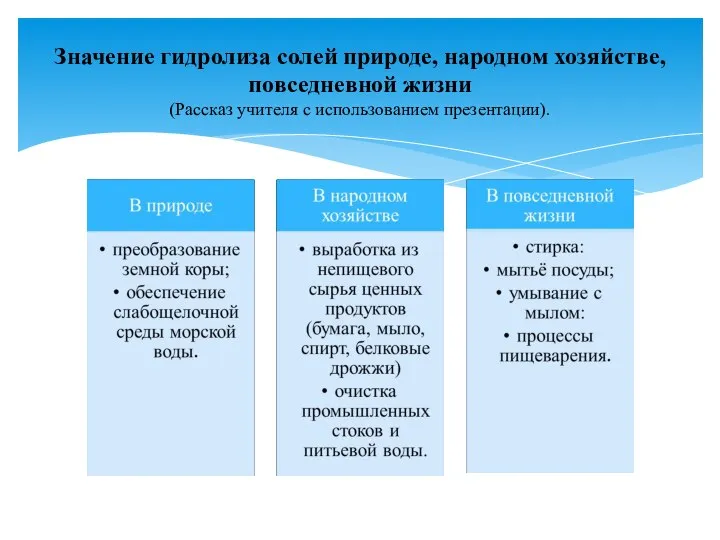
- 14. Значение гидролиза солей природе, народном хозяйстве, повседневной жизни (Рассказ учителя с использованием презентации).
- 15. Ответы к заданиям самостоятельной работы Правильные ответы :
- 16. 1.Тема нашего сегодняшнего урока … 2. Передо мной на уроке стояла цель … 3. Сегодня я
- 18. Скачать презентацию










 ФОСФОР Абдуллина Альфия Ахнафовна учитель химии МБОУ СОШ с.Никифарово МР Альшеевский район РБ
ФОСФОР Абдуллина Альфия Ахнафовна учитель химии МБОУ СОШ с.Никифарово МР Альшеевский район РБ  Соединения галогенов
Соединения галогенов Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Что объединяет вещества. Классификация твёрдых веществ
Что объединяет вещества. Классификация твёрдых веществ Химическая физика горения
Химическая физика горения Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н
Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н Кольцевые силикаты
Кольцевые силикаты Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Кислоты. Индикаторы
Кислоты. Индикаторы Химическая промышленность
Химическая промышленность Алициклические и гетероциклические соединения. Тема № 7, 8
Алициклические и гетероциклические соединения. Тема № 7, 8 Производные карбоновых кислот
Производные карбоновых кислот Жир жиру рознь. Супер омега 3
Жир жиру рознь. Супер омега 3 Экстракция
Экстракция Серная кислота H2SO4
Серная кислота H2SO4 Хроматографія. Мікрогетерогенні дисперсні системи
Хроматографія. Мікрогетерогенні дисперсні системи Строение мицеллы лиофобного золя
Строение мицеллы лиофобного золя Генетическая связь между основными классами органических соединений
Генетическая связь между основными классами органических соединений Презентация по Химии "Фотосинтез" - скачать смотреть
Презентация по Химии "Фотосинтез" - скачать смотреть  Презентация по Химии "Ток в электролитах" - скачать смотреть
Презентация по Химии "Ток в электролитах" - скачать смотреть  Способы разделения смесей
Способы разделения смесей Презентация по Химии "Химические знаки и их история" - скачать смотреть
Презентация по Химии "Химические знаки и их история" - скачать смотреть  Диаграммы состояния сплавов. Диаграмма состояния Fe-C (Fe-Fe3C). Лекция №2
Диаграммы состояния сплавов. Диаграмма состояния Fe-C (Fe-Fe3C). Лекция №2 Обмен веществ. Метаболизм и его функции
Обмен веществ. Метаболизм и его функции Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации
Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации Окислительно-восстановительные реакции в растворах
Окислительно-восстановительные реакции в растворах Переваривание и всасывание жиров
Переваривание и всасывание жиров Фосфор
Фосфор