Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации
Содержание
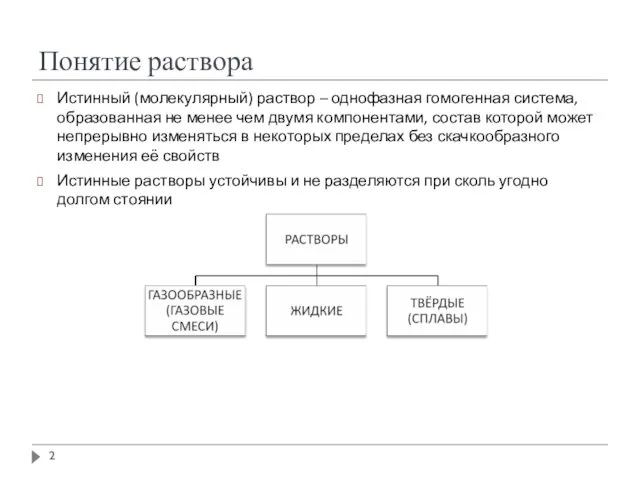
- 2. Понятие раствора Истинный (молекулярный) раствор – однофазная гомогенная система, образованная не менее чем двумя компонентами, состав
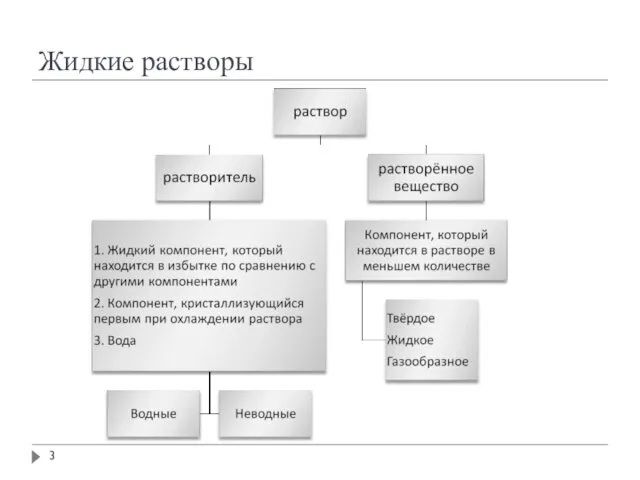
- 3. Жидкие растворы
- 4. Движущая сила образования растворов (1) Энтропийный и энтальпийный факторы При растворении газов в жидкости энтропия всегда
- 5. Движущая сила образования растворов (2) Независимо от знака энтальпии при растворении всегда т.е. переход вещества в
- 6. Растворимость Процесс растворения протекает самопроизвольно до тех пор, пока химический потенциал чистого компонента превышает химический потенциал
- 7. Способы выражения концентрации растворов Концентрация – величина, характеризующая относительное содержание данного компонента в многокомпонентной системе Массовая
- 8. Закон Рауля Парциальное давление насыщенного пара компонента раствора над раствором pi прямо пропорционально мольной доле этого
- 9. Закон Рауля для бинарного раствора Относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле
- 10. Закон Вант -Гоффа.
- 12. Растворы электролитов и неэлектролитов.
- 13. ТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ Электролиты, как сильные, так и слабые и даже очень сильно разбавленные не подчиняются
- 14. Электролитическая диссоциация предполагает, что молекулы электролита в растворе распадаются на положительно и отрицательно заряженные ионы, которые
- 15. С точки зрения степени диссоциации, по силе электролиты делятся на сильные (α > 0,7), средней силы
- 16. Реакции ионного обмена Реакции ионного обмена - это реакции между ионами, образовавшимися в результате диссоциации электролитов.
- 17. 1) образование малодиссоциирующих соединений: а) HCl + NaOH « NaCl + Н2О. Сущность процесса нейтрализации сильной
- 19. Скачать презентацию














 Каучук. История открытия
Каучук. История открытия Рідкі кристали та їх застосування
Рідкі кристали та їх застосування Презентация по Химии "Классификация химических реакций" - скачать смотреть
Презентация по Химии "Классификация химических реакций" - скачать смотреть  Свойства солей. Получение солей
Свойства солей. Получение солей Монотерпеноиды. Химическое строение и общая характеристика. Тема № 2
Монотерпеноиды. Химическое строение и общая характеристика. Тема № 2 Химические свойства солей
Химические свойства солей Глюкоза. Будова глюкози. Хімічні властивості глюкози
Глюкоза. Будова глюкози. Хімічні властивості глюкози Первичная структура белка
Первичная структура белка Интеррактивный кроссворд на тему: Химическая посуда и лабораторное оборудование
Интеррактивный кроссворд на тему: Химическая посуда и лабораторное оборудование Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».
Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека». Презентация Углекислый газ СО2
Презентация Углекислый газ СО2  Фосфор как элемент мысли и жизни
Фосфор как элемент мысли и жизни Решение задачи Неземная магическая кислота
Решение задачи Неземная магическая кислота Углеводы (сахариды)
Углеводы (сахариды) L-3-Biomolecules (1) (1) (1)
L-3-Biomolecules (1) (1) (1) Золото. Серебро. Металлы платиновой группы
Золото. Серебро. Металлы платиновой группы Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Моделирование химико-технологических процессов
Моделирование химико-технологических процессов Жёсткость воды и способы её устранения
Жёсткость воды и способы её устранения Классификация минералов
Классификация минералов Кристаллические системы
Кристаллические системы Электролиз. Задание № 20
Электролиз. Задание № 20 Общие сведения о метаморфизме
Общие сведения о метаморфизме Коррозионные повреждения
Коррозионные повреждения Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Неорганические лекарственные средства. Соединения элементов V и VI группы периодической системы
Неорганические лекарственные средства. Соединения элементов V и VI группы периодической системы Массовая доля растворённого вещества
Массовая доля растворённого вещества Изооктан. Получение. Октановое число и степень сжатия
Изооктан. Получение. Октановое число и степень сжатия