Содержание
- 2. Положение элементов в ПСХЭ Д. И. Менделеева
- 3. Характеристика металлов главной подгруппы II группы
- 4. Общая характеристика элементов главной подгруппы II группы У в е л и ч и в а
- 5. Общая характеристика элементов главной подгруппы II группы Одинаковое строение внешнего электронного слоя Элементы проявляют С.О. +2
- 6. Ве - амфотерный металл, Mg – металл, Сa, Sr,Ba - щёлочноземельные металлы Ra –радиоактивный элемент
- 7. Be – светло-серый, твердый, хрупкий Ca – твердый, пластичный Mg – относительно мягкий, пластичный, ковкий Sr
- 8. Получение щелочноземельных металлов Термическое восстановление их соединений: Be Cl2 + Mg = Be + MgCl2 MgO
- 9. Электролиз расплавов и рстворов галогенидов CuSO4 ⇄ Cu2+ + SO42- K(-): Cu2+ + 2e → Cu0
- 10. Химические свойства Щелочноземельные элементы - химически активные металлы. Они являются сильными восстановителями. Из металлов этой подгруппы
- 11. Взаимодействие с простыми веществами Все легко взаимодействуют с кислородом и серой: 2Be + O2 = 2BeO
- 12. Химические свойства элементов II группы главной подгруппы
- 13. Взаимодействие с водой Бериллий с водой не реагирует, магний реагирует медленно, остальные металлы реагируют с водой,
- 14. Взаимодействие кальция с водой https://yandex.ru/video/search?text=Взаимодействие кальция с водой
- 15. Взаимодействие с кислотами Все взаимодействуют с хлороводородной и разбавленной серной кислотами с выделением водорода: Be +
- 16. Взаимодействие со щелочами Бериллий взаимодействует с водными растворами щелочей с образованием комплексной соли и выделением водорода:
- 17. Соединения бериллия, магния и щелочноземельных металлов
- 18. Кислородные соединения - оксиды BeO – амфотерный оксид MgO CaO SrO Основные оксиды BaO Оксид кальция
- 19. ВеО В природе оксид бериллия встречается в виде минерала бромеллита. Получают оксид бериллия термическим разложение гидроксида
- 20. Химические свойства ВеО Реакционная способность оксида бериллия зависит от способа его получения. Прокаленный при температуре не
- 21. MgO белые кристаллы, нерастворимые в воде, На этом свойстве основано его применение в спортивной гимнастике, нанесенный
- 22. Химические свойства Реагирует с разбавленными кислотами с образованием солей MgO + 2HCl → MgCl2 + H2O
- 23. Взаимодействие оксида кальция с водой ( гашение извести) CaO + H2O → Ca(OH)2 + Q https://goo.gl/B0P1xN
- 24. Взаимодействие основных оксидов с водой https://goo.gl/Z6jPsC Взаимодействие оксидов металлов с кислотами https://goo.gl/r3zZiJ
- 25. Химические свойства гидроксидов Ве(ОН)2 – амфотерный гидроксид Mg(OH)2 – нерастворимое основание Ca(OH)2 Sr(OH)2 Ba(OH)2 Растворимые основания
- 26. Химические свойства Be(OH)2 Взаимодействие с щелочами с образованием соли: Be(OH)2 + 2NaOH ⟶ Na2Be(OH)4 Взаимодействие с
- 27. Взаимодействие гидроксидов с кислотами Ca(OH)2+2HCl=CaCl2+2H2O Mg(OH)2+2HCl=MgCl2+2H2O https://goo.gl/mhngzl
- 28. Окраска пламени солями металлов https://www.youtube.com/watch?v=nMptepCx0Jw https://www.youtube.com/watch?v=rccFLDrWMxc&t=4s
- 29. Жесткость воды Карбонатная, или временная Некарбонатная, или постоянная Общая жесткость Общая жесткость воды – это сумма
- 30. Карбонатная, или временная жесткость Обусловлена присутствием гидрокарбонатов кальция и магния. Её можно устранить: 1. Кипячением Ca(HCO3)2
- 31. Некарбонатная, или постоянная жесткость Обусловлена присутствием сульфатов и хлоридов кальция и магния. Её можно устранить действием
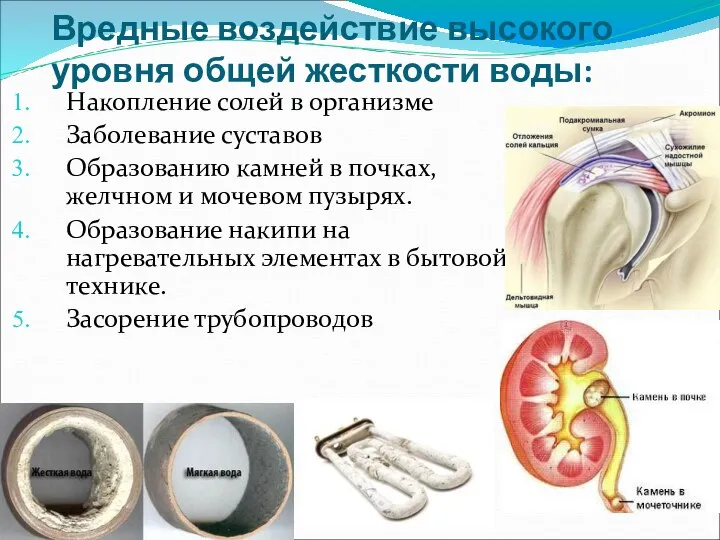
- 32. Вредные воздействие высокого уровня общей жесткости воды: Накопление солей в организме Заболевание суставов Образованию камней в
- 33. Способы снижения общей жесткости воды. БЫТОВЫЕ ПРОМЫШЛЕННЫЕ Кипячение Фильтрование Вымораживание Добавление умягчителей Добавление кальцинированной соды (Na2CO3)
- 34. Кипячение Снижение жесткости примерно на 30 - 40%
- 35. Вымораживание Вымораживание снижает общую жесткость на 70-80%
- 36. Фильтрование Фильтрование воды бытовым фильтром «Барьер-6» снижает общую жесткость до 80%.
- 39. Практическое значение соединений магния и щелочноземельных металлов MgCO – карбонат магния. Используется в производстве стекла, цемента,
- 40. Практическое значение соединений магния MgSO –cульфат магния. Содержится в морской воде и придает ей горький вкус.
- 41. Практическое значение соединений кальция фосфат кальция Входит в состав фосфоритов и апатитов, а также в состав
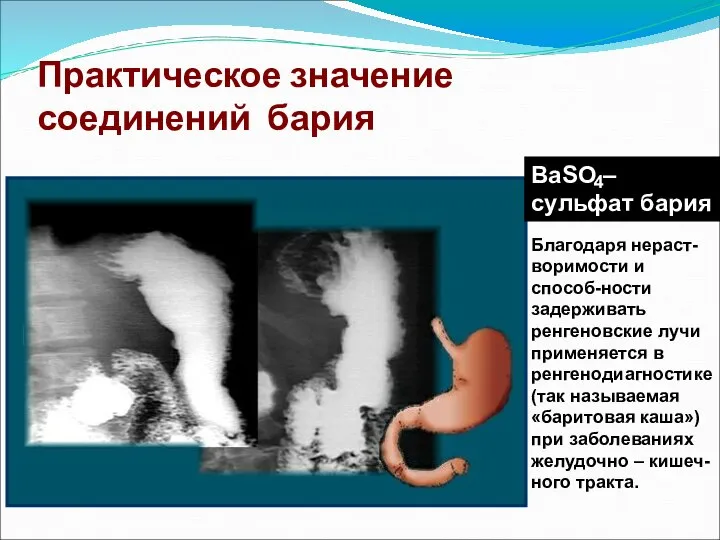
- 42. Практическое значение соединений бария BaSO – сульфат бария 4 Благодаря нераст-воримости и способ-ности задерживать ренгеновские лучи
- 43. Ca→CaH2→Ca(OH)2→ CaCO3→CaO→CaCl2→ Ca3(PO4)2
- 45. Скачать презентацию








































 Химическая организация клетки
Химическая организация клетки Классы дисперсных систем (аэрозоли, порошки, суспензии, эмульсии). Мицеллярные коллоидные системы. Лекция 5
Классы дисперсных систем (аэрозоли, порошки, суспензии, эмульсии). Мицеллярные коллоидные системы. Лекция 5 Водород
Водород Пищевые добавки
Пищевые добавки Электрохимические процессы
Электрохимические процессы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Кислород
Кислород Виробництво біогазу Виконав: студент IV курсу групи БЛБ-43з Вила Віктор
Виробництво біогазу Виконав: студент IV курсу групи БЛБ-43з Вила Віктор  Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Нанотехнологии и науки о материалах
Нанотехнологии и науки о материалах Изотермический процесс в реакционном объеме. (Тема 6.2)
Изотермический процесс в реакционном объеме. (Тема 6.2) Вода
Вода Растворы и растворимость. (8 класс)
Растворы и растворимость. (8 класс) Основы общей химии
Основы общей химии Высокомолекулярные соединения (ВМС) или полимеры
Высокомолекулярные соединения (ВМС) или полимеры «НЕМНОГО О МЕТАЛЛАХ И МЕТАЛЛУРГИИ» ХИМИЧЕСКАЯ ВИКТОРИНА учитель химии МКОУ СОШ №14 пос. Пятигорский Балацкая Татьяна Алексеевна
«НЕМНОГО О МЕТАЛЛАХ И МЕТАЛЛУРГИИ» ХИМИЧЕСКАЯ ВИКТОРИНА учитель химии МКОУ СОШ №14 пос. Пятигорский Балацкая Татьяна Алексеевна Ферменты строение и свойства. Регуляция активности ферментов. (Лекция 1.3)
Ферменты строение и свойства. Регуляция активности ферментов. (Лекция 1.3) Химия ғажайыптары
Химия ғажайыптары Комплексные соединения
Комплексные соединения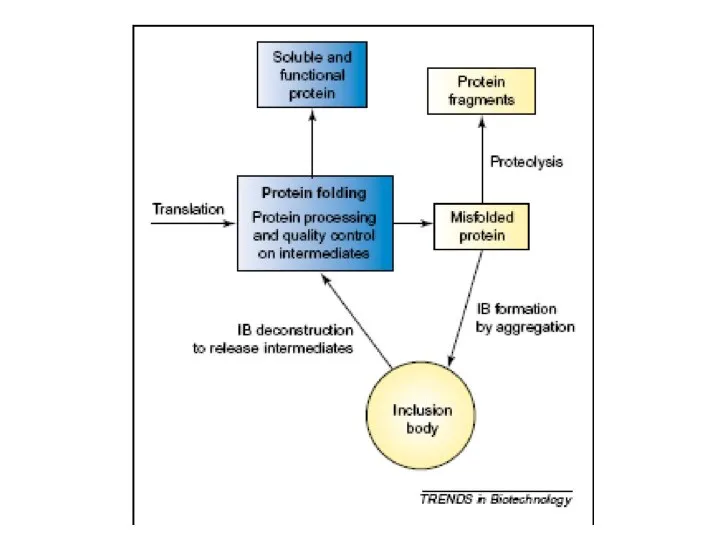 Рефолдинг миниантител
Рефолдинг миниантител Кислоты. Соли (8 класс)
Кислоты. Соли (8 класс) Моделі будови атома
Моделі будови атома Осадочные горные породы
Осадочные горные породы Спирты
Спирты Реакции ионного обмена
Реакции ионного обмена Общая характеристика твердого, жидкого и газообразного видов топлива
Общая характеристика твердого, жидкого и газообразного видов топлива Производные пиридин-4-карбоновой кислоты
Производные пиридин-4-карбоновой кислоты Презентация по химии ПЕПТИДЫ и Белки
Презентация по химии ПЕПТИДЫ и Белки