Содержание
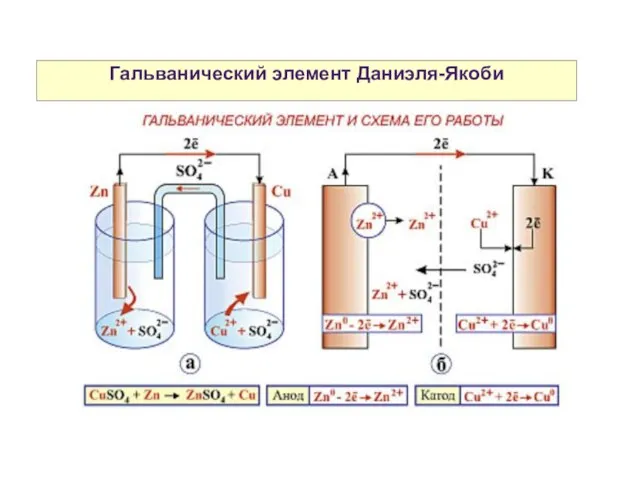
- 2. Гальванический элемент Даниэля-Якоби
- 3. Принцип работы гальванического элемента ΔНрешетки > 0 ΔНгидратации В зависимости от величины значений данных энтальпий на
- 4. Принцип работы гальванического элемента Анод — это электрод, на котором происходит процесс ОКИСЛЕНИЯ (отдачи е-) (восстановитель).
- 5. Принцип работы гальванического элемента
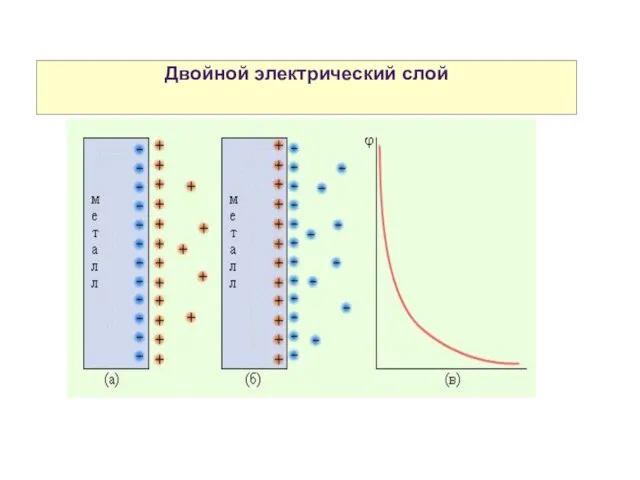
- 6. Двойной электрический слой
- 7. Гальванический элемент Даниэля-Якоби Схема гальванического элемента Даниэля-Якоби: (-) Zn|Zn2+||Cu2+|Cu (+)
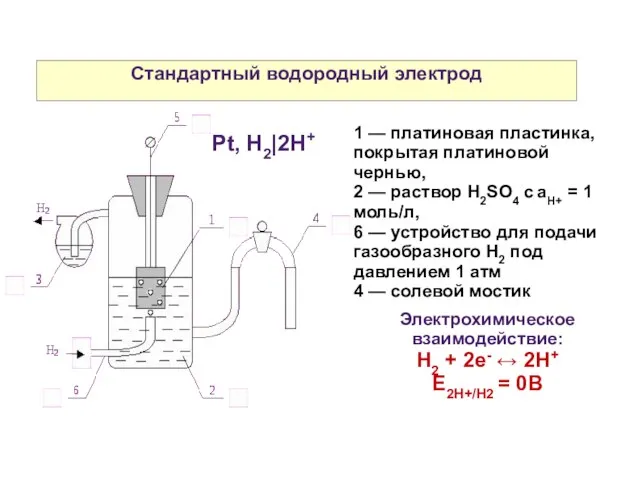
- 8. Стандартный водородный электрод 1 — платиновая пластинка, покрытая платиновой чернью, 2 — раствор H2SO4 c aH+
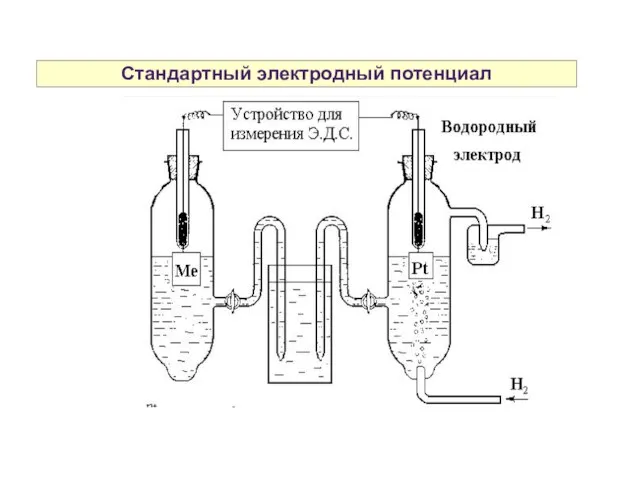
- 9. Стандартный электродный потенциал
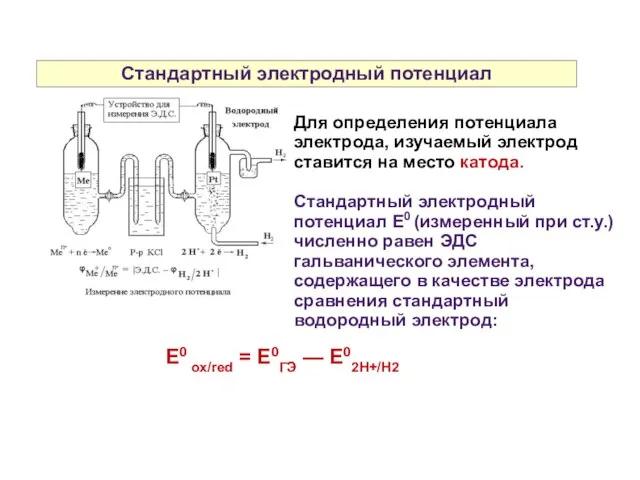
- 10. Стандартный электродный потенциал Для определения потенциала электрода, изучаемый электрод ставится на место катода. Стандартный электродный потенциал
- 11. Таблица стандартных электродных потенциалов
- 12. Стандартный электродный потенциал При составлении произвольного ГЭ, электрод с более положительным потенциалом будет выполнять функции катода
- 13. Уравнение Нернста для отдельного электрода В нестандартных условиях потенциал электрода определяют по уравнению Нернста. (–) Pt
- 14. Уравнение Нернста для отдельного электрода G = – nFE G0 = – nFE0
- 15. Уравнение Нернста для отдельного электрода Общий вид уравнения Нернста для отдельного электрода: где аоф — активность
- 16. Уравнение Нернста для отдельного электрода Задание: определить потенциал медного электрода, молярная концентрация раствора CuSO4 в котором
- 17. Уравнение Нернста для гальванического элемента Процесс идет в прямом направлении, если GГЭ 0, т. к. G
- 18. Уравнение Нернста для гальванического элемента Задание: определить E0ГЭ и ЕГЭ для элемента Даниэля-Якоби. Пусть aCu2+ =
- 19. Уравнение Нернста для гальванического элемента (-) Zn — 2e- → Zn2+ (+) Cu2+ + 2e- →
- 20. Уравнение Нернста для гальванического элемента В общем виде уравнение Нернста для гальванического элемента имеет вид: (-)
- 21. Взаимосвязь константы равновесия Кр со стандартным потенциалом гальванического элемента Е0ГЭ G0 = – nFE0 G0 =
- 22. Взаимосвязь константы равновесия Кр со стандартным потенциалом гальванического элемента Е0ГЭ G0 = – nFE0 G0 =
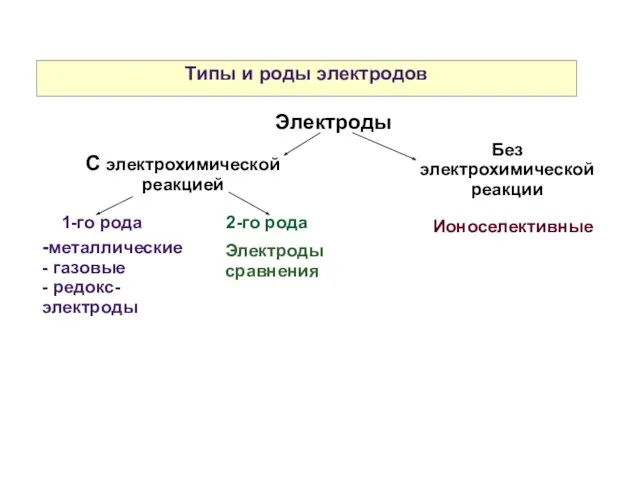
- 23. Типы и роды электродов Электроды С электрохимической реакцией 1-го рода 2-го рода -металлические - газовые -
- 24. Металлические электроды Металл, погруженный в раствор своей соли Me|Men+ Cu|Cu2+ Cu Cu2+ + 2e- Zn|Zn2+ Zn
- 25. Газовые электроды Газовый электрод состоит из инертного проводника 1-го рода (Pt, графит) и газа, находящегося в
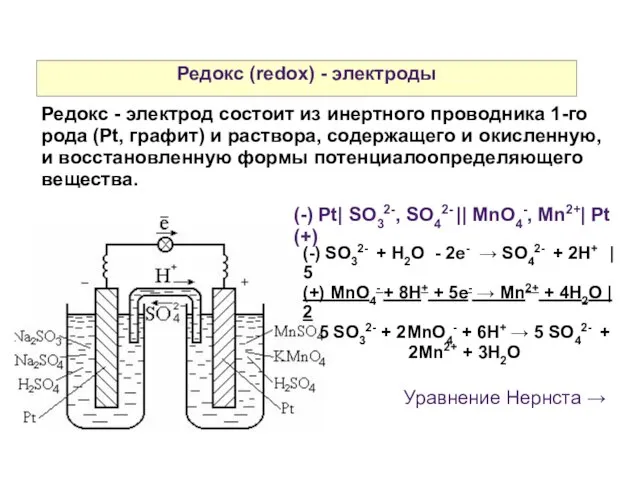
- 26. Редокс (redox) - электроды Редокс - электрод состоит из инертного проводника 1-го рода (Pt, графит) и
- 27. Редокс (redox) - электроды (-) SO32- + H2O - 2e- → SO42- + 2H+ | 5
- 28. Электроды сравнения (2-го рода) Состоят из проводника 1-го рода — металла — покрытого слоем труднорастворимой соли
- 29. Некоторые практически значимые ХИТ Свинцовый (кислотный) аккумулятор (–) Pb, PbSO4 H2SO4 PbO2, Pb (+) (-)
- 30. Некоторые практически значимые ХИТ Свинцовый (кислотный) аккумулятор (–) Pb, PbSO4 H2SO4 PbO2, Pb (+) работа
- 31. Некоторые практически значимые ХИТ Щелочной железо-никелевый аккумулятор (–) Fe, Fe(OH)2 ⏐KOH⏐Ni(OH)2, Ni(OH)3, Ni (+) работа →
- 32. Некоторые практически значимые ХИТ Литий-ионный аккумулятор
- 34. Скачать презентацию
























 Ion exchange
Ion exchange Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск
Кристалл Гришина Л.А., учитель физики МКС(К) ОУ С (К) ОШ 37 I II вида г. Новосибирск Презентація на тему: “Поняття про полімери на прикладі поліетилену”
Презентація на тему: “Поняття про полімери на прикладі поліетилену”  Соли и классы химических веществ
Соли и классы химических веществ Определение разных форм угольной кислоты
Определение разных форм угольной кислоты Строение углеводородов
Строение углеводородов Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов
Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов Водород
Водород  Валентність
Валентність  Ферроцен. Свойства, получение и применение
Ферроцен. Свойства, получение и применение Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу
Основні характеристики атомних електростанцій (АЕС) та підприємств ядерного паливного циклу Изотермический распад переохлажденного аустенита
Изотермический распад переохлажденного аустенита Презентация по Химии "«Химические волокна»" - скачать смотреть
Презентация по Химии "«Химические волокна»" - скачать смотреть  Три кити нанохімії
Три кити нанохімії Гiдроксикислоти. Номенклатура
Гiдроксикислоти. Номенклатура Комплексные соединения
Комплексные соединения Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха
Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха Конструкция ферментатора
Конструкция ферментатора Электролитическая диссоциация. Устойчивость комплексных соединений
Электролитическая диссоциация. Устойчивость комплексных соединений Щелочные металлы
Щелочные металлы Низкомолекулярные биорегуляторы терпены
Низкомолекулярные биорегуляторы терпены Серная кислота H2SO4
Серная кислота H2SO4 Хроматографические методы анализа
Хроматографические методы анализа Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия
Металлы и сплавы, Металлы и сплавы, их свойства и применение в радиоэлектронной аппаратуре Подготовил: учащийся гр.7/8 профессия Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі
Адсорбция-фазалар бөлу беттерінде жүретін бір компоненттің екінші компонентке сіңуі Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость
Диаграммы состояния двухкомпонентных систем типа твердое тело – жидкость