Содержание
- 2. ЛИТЕРАТУРА Слесарев В.И. Химия: Основы химии живого. Саргаев П.М. Неорганическая химия Цитович И.К. Основы аналитической химии
- 3. Учебные вопросы лекции: 1. Основные понятия науки «Химия». Химические реакции, их классификация. 2. Основные законы химии.
- 4. Первый учебный вопрос. Основные понятия науки «Химия». Химические реакции, их классификация.
- 5. Химия – наука о веществах, их строении, свойствах и превращениях. Все тела в природе состоят из
- 7. Физические явления – это изменения формы или агрегатного состояния веществ, в результате которых не образуются новые
- 8. Основные понятия атомно-молекулярного учения В центре любого атома находится ядро, которое состоит из протонов и нейтронов,
- 9. Любой атом содержит равное число протонов и электронов, поэтому сумма положительных зарядов в атоме равна сумме
- 10. Вид атомов с одинаковым зарядом ядер называется химическим элементом. Для каждого элемента известны разновидности атомов, отличающиеся
- 11. Атомы – мельчайшие химически неделимые частицы вещества, они распадаются лишь при ядерных реакциях. Атомы, соединяясь друг
- 12. Химические формулы 3СuCl2 5Al2O3 4FeCl3 СН – эмпирическая (простейшая); С6Н6 – истинная; – структурная.
- 16. Абсолютные атомные массы Масса атома водорода: 1,67·10-27 кг = 1,67·10-24 г; масса атома кислорода: 26,67·10-27 кг.
- 17. Относительной молекулярной массой (Mr) вещества называется величина, равная отношению средней массы молекулы вещества к 1/12 массы
- 18. Количество вещества (n, число молей вещества) вычисляется по формуле: где m – масса вещества, г; M
- 19. Из определения понятия «моль» следует, что это число равно числу молекул (атомов) в одном моле любого
- 20. КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ Химическая реакция – превращение веществ с образованием новых соединений с новыми свойствами. I.
- 21. II. По знаку теплового эффекта: а) экзотермические (происходит выделение теплоты); б) эндотермические (происходит поглощение теплоты). III.
- 22. VI. По числу и составу исходных веществ (реагентов) и продуктов реакции: а) Реакции соединения – это
- 23. в) Реакции замещения – это реакции между простыми и сложными веществами, при протекании которых атомы простого
- 24. Второй учебный вопрос. Основные законы химии.
- 25. В равных объемах (V) различных газов при одинаковых внешних условиях (температуре Т и давлении Р) содержится
- 26. Следовательно, объем одного моля любого газа (т.е. 6,02 ·1023 молекул) при определенных внешних условиях есть величина
- 27. Молярный объем любого газа при н.у. равен 22,4 л/моль. VM (газа) н.у. = 22,4 л/моль. Молярный
- 28. ЗАКОН СОХРАНЕНИЯ МАССЫ ВЕЩЕСТВ В 1748 г. М.В.Ломоносов и в 1789 г. А.Лавуазье независимо друг от
- 29. ЗАКОН ПОСТОЯНСТВА СОСТАВА ВЕЩЕСТВА (Ж.Пруст, 1808) Каждое чистое вещество независимо от способа его получения всегда имеет
- 30. Закон эквивалентов – основа количественных расчетов в химической реакции. Сформулировал в 1793 году немецкий химик Иеремия
- 31. Соединения постоянного состава (дальтониды), или стехиометрические соединения – химические соединения, состав которых постоянен и не зависит
- 32. ЗАКОН ОБЪЁМНЫХ ОТНОШЕНИЙ (Ж.Л.ГЕЙ-ЛЮССАК, 1802 г) Объёмы вступающих в реакцию газов при одинаковых условиях (температуре и
- 33. Химический эквивалент элемента – это такое количество его атомов, которое соединяется полностью с 1 молем атомов
- 35. Скачать презентацию






























 Диеновые углеводороды (алкадиены)
Диеновые углеводороды (алкадиены) Обмен углеводов
Обмен углеводов Натуральные и синтетические каучуки
Натуральные и синтетические каучуки Кобальт. Нахождение Co в природе
Кобальт. Нахождение Co в природе Викторина по химии
Викторина по химии Периодический закон. Периодическая система химических элементов
Периодический закон. Периодическая система химических элементов Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы амины 10 класс
амины 10 класс Золото Aurum
Золото Aurum Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23)
Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23)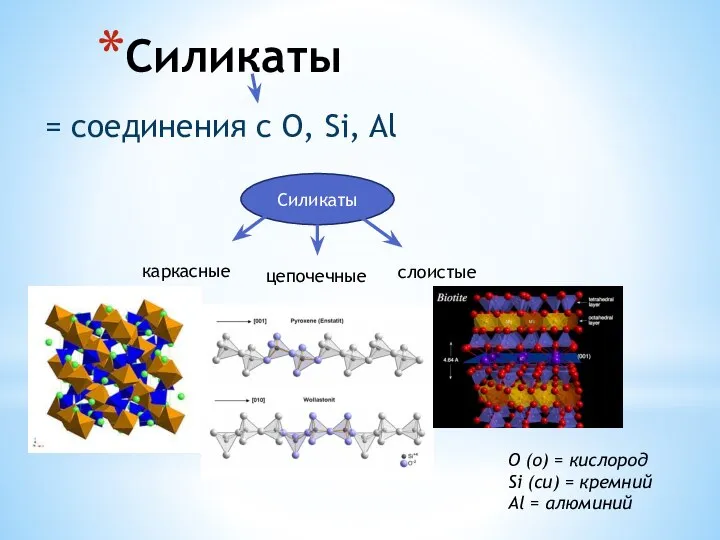 Силикаты. Гранат. Берилл
Силикаты. Гранат. Берилл Курс химии (Литвиновой Татьяны Николаевны)
Курс химии (Литвиновой Татьяны Николаевны) Клонирование генов, создание геномных и кДНК-библиотек, искусственный синтез генов
Клонирование генов, создание геномных и кДНК-библиотек, искусственный синтез генов Реология расплавов и растворов полимеров
Реология расплавов и растворов полимеров Презентация по Химии "Химические антонимы" - скачать смотреть
Презентация по Химии "Химические антонимы" - скачать смотреть  Побочная подгруппа VIII группы периодической системы
Побочная подгруппа VIII группы периодической системы Цикл Кальвина
Цикл Кальвина Белки. Классификация белков. (Тема 2)
Белки. Классификация белков. (Тема 2) Відносна молекулярна маса. Масова частка елемента в складній речовині
Відносна молекулярна маса. Масова частка елемента в складній речовині Презентация 30
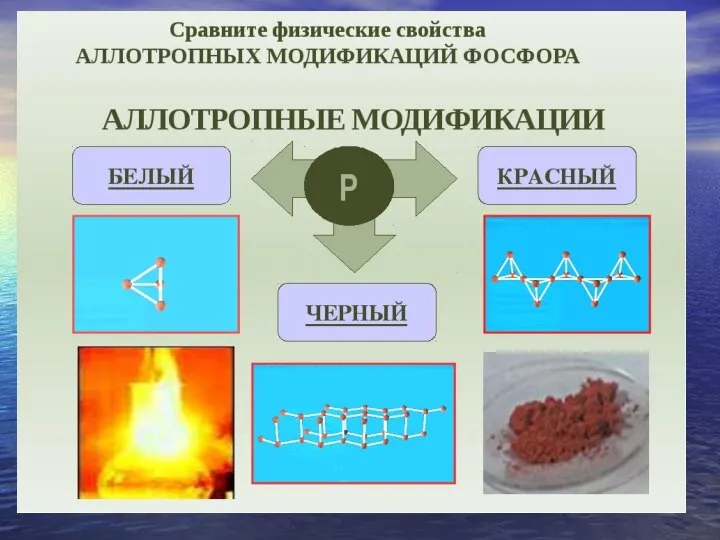
Презентация 30 Фосфорные удобрения
Фосфорные удобрения МОУ Квитокская средняя общеобразовательная школа. УРОК ХИМИИ. 11 КЛАСС. Химия и производство. Учитель: Левицкая Лариса Виктор
МОУ Квитокская средняя общеобразовательная школа. УРОК ХИМИИ. 11 КЛАСС. Химия и производство. Учитель: Левицкая Лариса Виктор Алканы. Гомологический ряд и изомерия
Алканы. Гомологический ряд и изомерия Амины. Общая характеристика, номенклатура, изомерия. Получение. Физико-химические свойства. Отдельные представители
Амины. Общая характеристика, номенклатура, изомерия. Получение. Физико-химические свойства. Отдельные представители Гетерогенные и лигандообменные равновесия и процессы
Гетерогенные и лигандообменные равновесия и процессы Лекция 10. Химия s-элементов
Лекция 10. Химия s-элементов Оксиды
Оксиды Кислородсодержащие органические соединения
Кислородсодержащие органические соединения