Содержание
- 2. Что такое кислоты? Сложные вещества, состоящие из атомов водорода, соединенных с кислотным остатком HR Электролиты, диссоциирующие
- 3. Классификация кислот
- 4. Химические свойства кислот Диссоциация Действие на индикатор Взаимодействие с металлами Взаимодействие с основаниями. Реакция нейтрализации Взаимодействие
- 5. Особые свойства кислот определяются кислотным остатком Реакция ионного обмена H2SO4+BaCl2 = 2HCL+BaSO4 Ba2++SO42-=BaSO4 Окислительно -восстановительная реакция
- 6. Диссоциация кислот H+ R n-=H++Rn- HCl → HNO3→ H2SO4 → H3PO4 → H++ Cl- H+ +
- 7. Взаимодействие с индикатором Помни! Нерастворимые кислоты не меняют окраску индикаторов.
- 8. Взаимодействие с металлами Ме + НR → МеR+ Н2 металл + кислота→соль + водород 2 Zn
- 9. Взаимодействие с основными оксидами МеxOy + HR→ МеR+ H2O Основный оксид + кислота → соль +
- 10. Взаимодействие с основаниями Ме(ОН)m + НR→ MeR+ H2O Основание + кислота → соль + вода 2LiOH
- 12. Скачать презентацию









 Гидролиз. Сущность процесса гидролиза
Гидролиз. Сущность процесса гидролиза Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения Кругообіг Нітрогену
Кругообіг Нітрогену  Химические реактивы
Химические реактивы Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М
Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М Сложные эфиры. 10 класс
Сложные эфиры. 10 класс Алканы. Алкены. Алкины. Задачи урока:
Алканы. Алкены. Алкины. Задачи урока:  Теория резонанса в неорганической химии
Теория резонанса в неорганической химии Пищевые красители
Пищевые красители Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_
Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_ «Уксусная кислота»
«Уксусная кислота»  Физико-химическая и механическая миграция
Физико-химическая и механическая миграция Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс)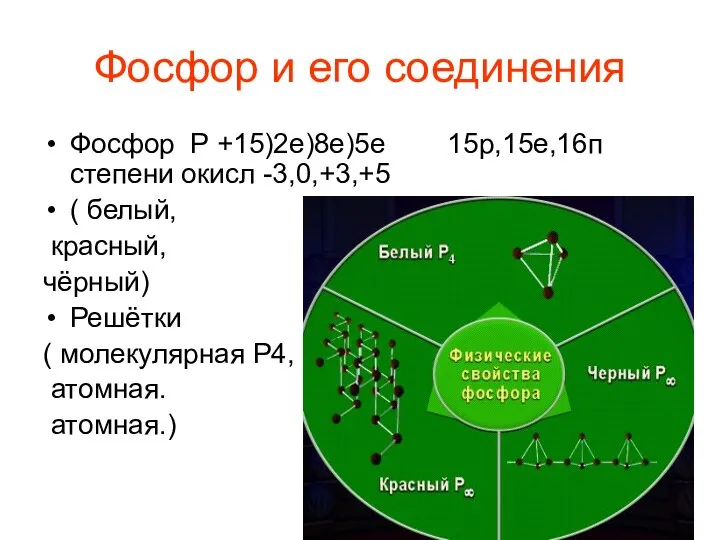 Фосфор и его соединения
Фосфор и его соединения Исследование процесса диффузии на примере движения частиц в жидкостях и газах
Исследование процесса диффузии на примере движения частиц в жидкостях и газах Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Электрометрические методы анализа ЛВ. Термографические методы
Электрометрические методы анализа ЛВ. Термографические методы Янтарь – солнечный камень. Рассказ об удивительном минерале
Янтарь – солнечный камень. Рассказ об удивительном минерале Фармацевтические суспензии и эмульсии
Фармацевтические суспензии и эмульсии Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Галогены: Хлор, бром, иод
Галогены: Хлор, бром, иод Классификация и номенклатура органических соединений
Классификация и номенклатура органических соединений Введение в обмен веществ. Метаболические пути
Введение в обмен веществ. Метаболические пути Залежність фізичних властивостей речовин від типу кристалічних ґраток
Залежність фізичних властивостей речовин від типу кристалічних ґраток Тема урока "Круговорот углерода в природе и последствия его нарушения« Учитель биологии Рабаданова Светлана Ивановна МОУ Лиц
Тема урока "Круговорот углерода в природе и последствия его нарушения« Учитель биологии Рабаданова Светлана Ивановна МОУ Лиц Қызықты химия
Қызықты химия Основы химической кинетики
Основы химической кинетики Трансформация энергии в процессе оксигенного фотосинтеза
Трансформация энергии в процессе оксигенного фотосинтеза