Содержание
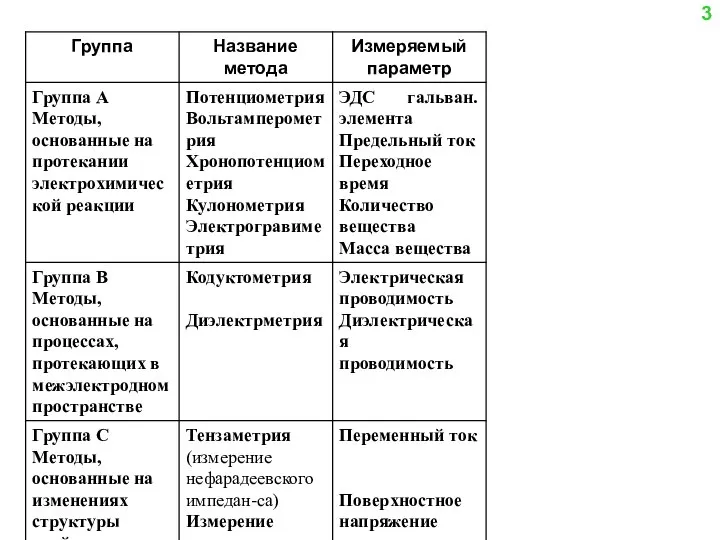
- 2. Классификация по количеству вещества, участвующего в электрохимическом процессе: ∙ методы, в которых все количество определяемого вещества
- 3. 3
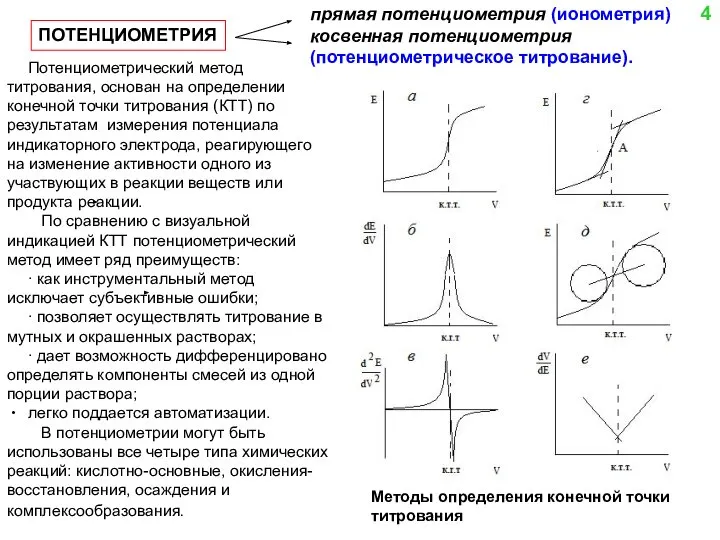
- 4. ПОТЕНЦИОМЕТРИЯ прямая потенциометрия (ионометрия) косвенная потенциометрия (потенциометрическое титрование). 4 Потенциометрический метод титрования, основан на определении конечной
- 5. КИСЛОТНО-ОСНОВНОЕ ТИТРОВАНИЕ. ПРОТОЛИТОМЕТРИЯ Титрование растворами оснований называют алкалиметрия, а растворами кислот - ацидиметрия В кислотно-основном титровании
- 6. y = [B+] = [A-] − [H+] + Kw / [H+] (4) y = сo −
- 7. Для оценки формы кривой титрования можно использовать “буферную емкость” (или для краткости “буферность”) системы Р =
- 8. [H+] pH P=2,3([H+]+[OH-]) 1 0 ≈ 2,3 1·10-1 1 ≈ 2,30·10-1 1·10-2 2 ≈ 2,30·10-2 4·10-3
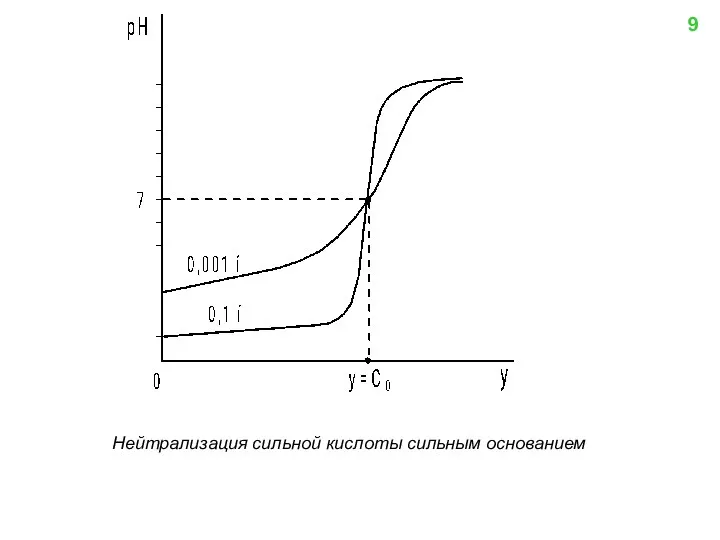
- 9. Нейтрализация сильной кислоты сильным основанием 9
- 10. Нейтрализация слабой кислоты сильным основанием y = [B+] = [A-] − [H+] + Kw / [H+]
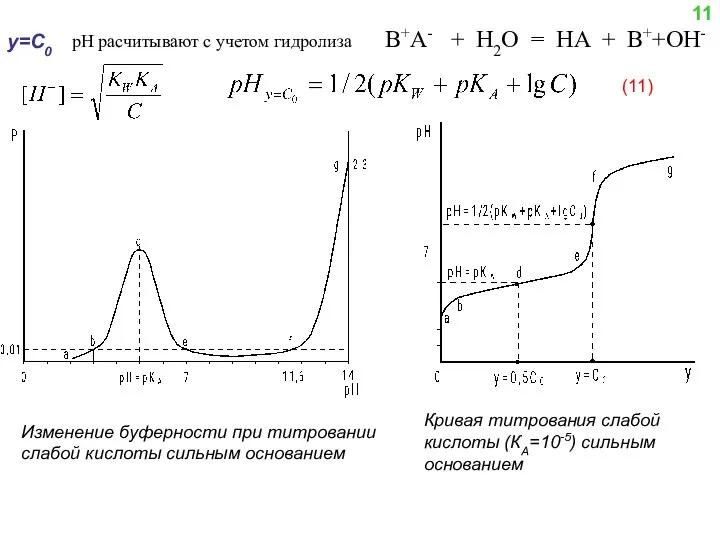
- 11. y=C0 В+А- + H2O = HA + B++OH- Изменение буферности при титровании слабой кислоты сильным основанием
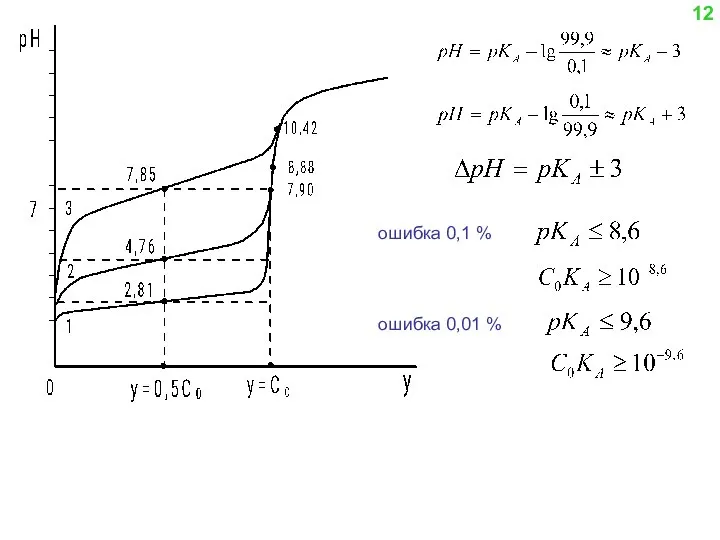
- 12. ошибка 0,1 % ошибка 0,01 % 12
- 13. Титрование смесей протолитов Допустим титруется смесь двух одноосновных кислот HA(1) и HA(2) различной силы, причем рКА,1
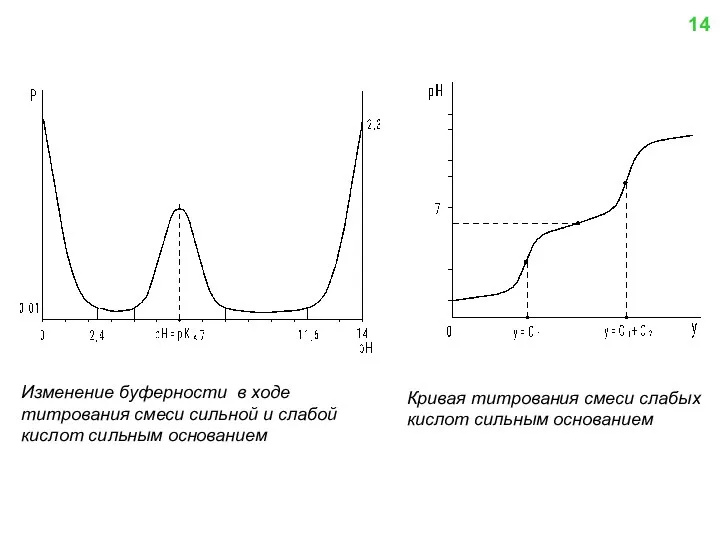
- 14. Изменение буферности в ходе титрования смеси сильной и слабой кислот сильным основанием Кривая титрования смеси слабых
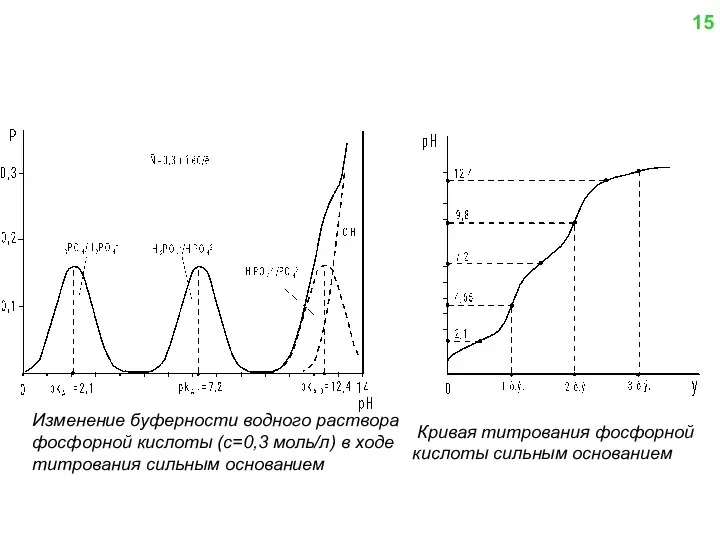
- 15. Изменение буферности водного раствора фосфорной кислоты (с=0,3 моль/л) в ходе титрования сильным основанием Кривая титрования фосфорной
- 16. ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ В НЕВОДНЫХ СРЕДАХ В подходящей неводной среде можно титровать смеси кислот, константы, диссоциации которых
- 17. Протолитическая теория кислот (Бренстед и Лоури) А ↔ H+ + В кислота основание НС1 ↔ Н+
- 18. Органические растворители в соответствии с донорно-акцепторными свойствами по отношению к протону можно разделить на апротонные (непротолитические),
- 19. pKaHSolv = − lg KaHSolv; pH = − lg(H2Solv+); pSolv = − lg(Solv-) pKaHSolv = pH
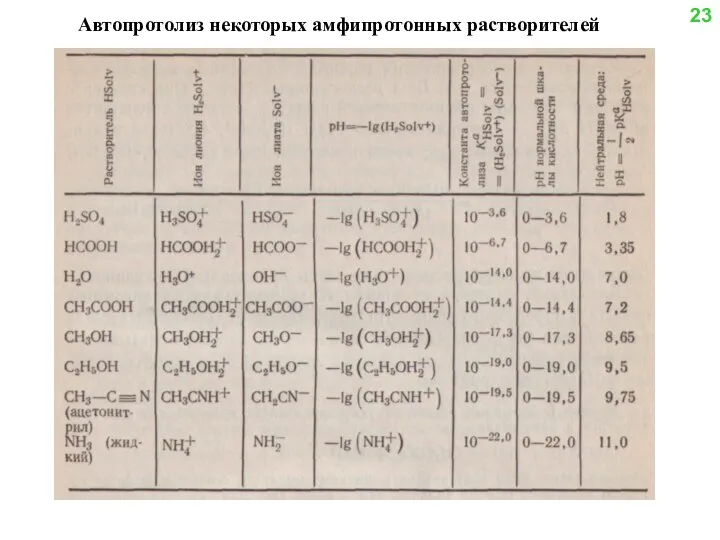
- 20. Автопротолиз некоторых амфипротонных растворителей 23
- 21. Если растворенный протолит по отношению к молекулам растворителя проявляет кислые свойства, устанавливается следующее равновесие: А +
- 22. Если растворенный протолит по отношению к молекулам растворителя проявляет основные свойства, устанавливается равновесие: В + HSolv
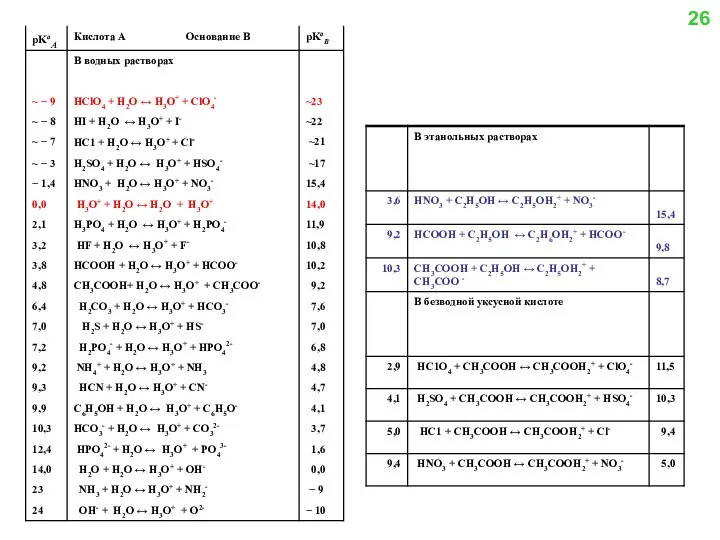
- 23. 26
- 24. Сильными называют протолиты, при растворении которых равновесия (6) или (8) смещены вправо. Для кислот pKaA 1),
- 25. 3. При анализе смесей протолитов важно, чтобы растворитель был высоко дифференцирующим. Дифференцирующее действие растворителей зависит от
- 26. 4. Растворители амфипротонного характера обладают более высоким дифференцирующим действием как в отношении кислот, так оснований. Чем
- 27. Относительную шкалу кислотности данного растворителя выражают числом милливольт, получаемым путем вычитания потенциала полунейтрализации гидроокиси тетраэтиламмония из
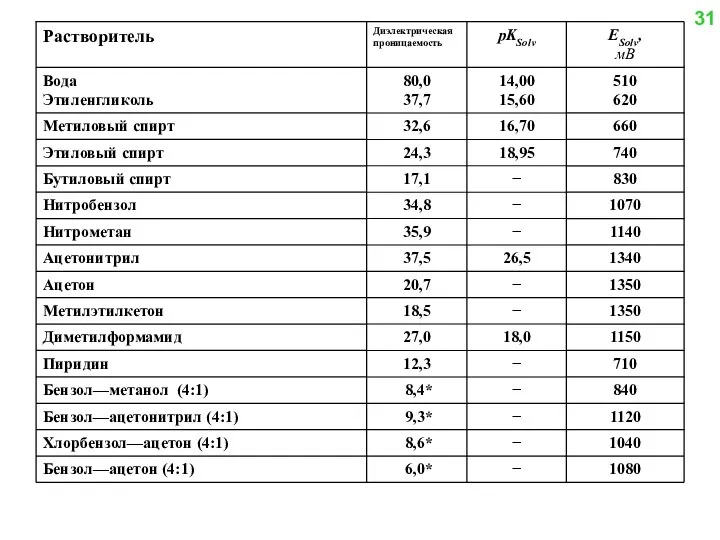
- 28. 31
- 29. 5. Величина диэлектрической проницаемости растворителей также оказывает влияние на дифференцирующее действие растворителей. Дифференциирующая способность уксусной кислоты
- 30. Удобным методом оценки влияния растворителей на силу кислот и оснований, также как и для оценки относительной
- 31. Титрование в неводных растворах осуществляют полумикрометодом (рис. 15) с автоматическими микробюретками (5, 2 или 1 мл
- 32. В качестве титрантов используют в основном неводные растворы хлорной кислоты. Хлорная кислота наиболее сильная кислота в
- 33. А ↔ H+ + В протолитическая пара КαA = (Н+)(В)/(А) константа кислоты Расчет кривой протолитического титрования
- 34. 0 τ = 1; τ >1; pH = - lgc0 - lg(1- τ) pH = -lgc0+
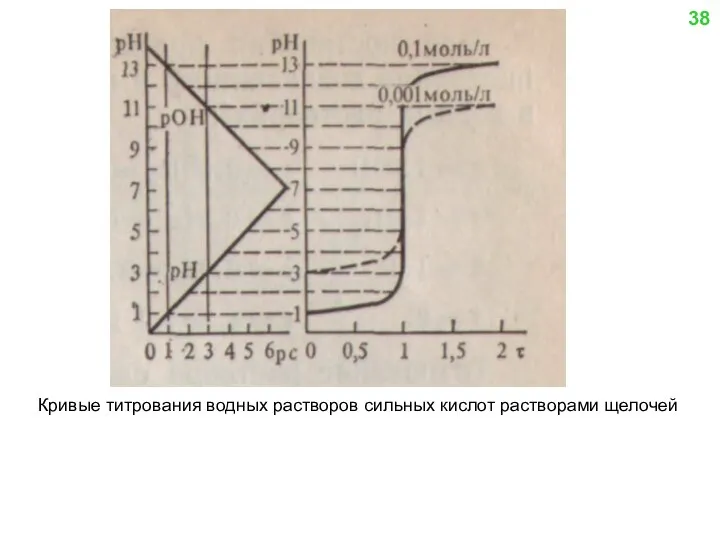
- 35. Расчет рН кривой титрования сильной кислоты сильным основанием 37
- 36. Кривые титрования водных растворов сильных кислот растворами щелочей 38
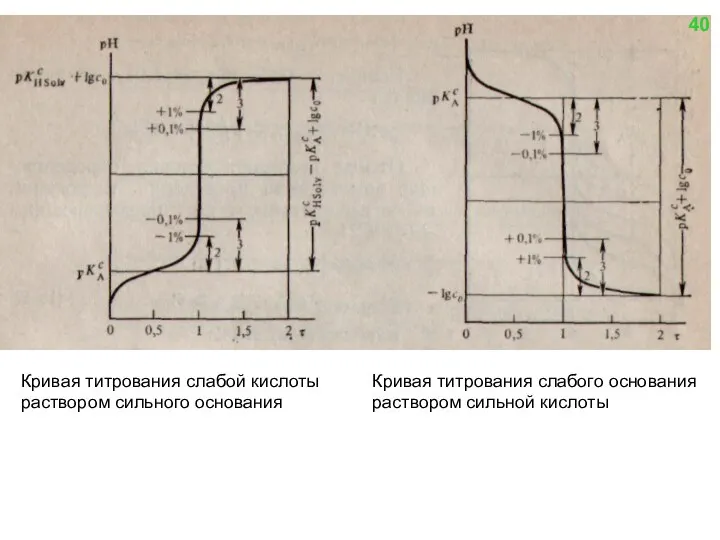
- 37. Расчет кривой титрования слабой кислоты сильным основанием A + Solv- = B + HSolv 0 τ
- 38. Кривая титрования слабой кислоты раствором сильного основания Кривая титрования слабого основания раствором сильной кислоты 40
- 39. Окислительно-восстановительное потенциометрическое титрование Ox + ne = Red, (1) MnO4─ + 5e + 8H+ = Mn2+
- 40. В равновесии Е1=Е2, поэтому приравнивая правые части уравнений 3 и 4, получим Учитывая, что n1α =
- 41. Расчет кривой титрования и анализ ее формы Когда y C0 − уравнение 4 В точке эквивалентности,
- 42. Расчет кривой титрования и анализ ее формы Когда y C0 − уравнение 3 В точке эквивалентности,
- 43. Все остальные точки кривой титрования можно рассчитать, зная исходную концентрацию С0 определяемого вещества и концентрацию y
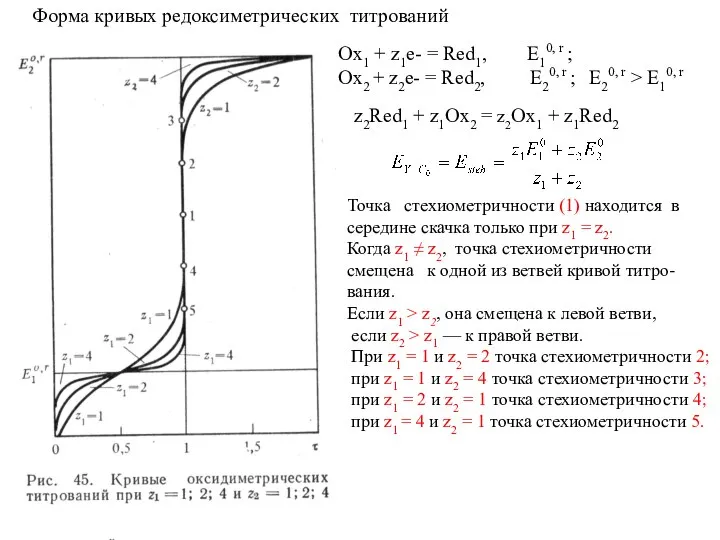
- 44. Форма кривых редоксиметрических титрований Точка стехиометричности (1) находится в середине скачка только при z1 = z2.
- 45. Вычислить скачок можно задаваясь допустимой погрешностью анализа. Допустим, устраивает погрешность 0,1%, тогда в конце титрования восстановителя
- 46. Титрование смесей восстановителей (окислителей) Рассмотрим оксидиметрическое титрование смеси двух восстановителей Red1 и Red2. Титрантом при этом
- 47. Hal- + Ag+ = AgHal↓ Если проводить титрование 0,1 моль/л раствора галогенида 0,1 моль/л раствором нитрата
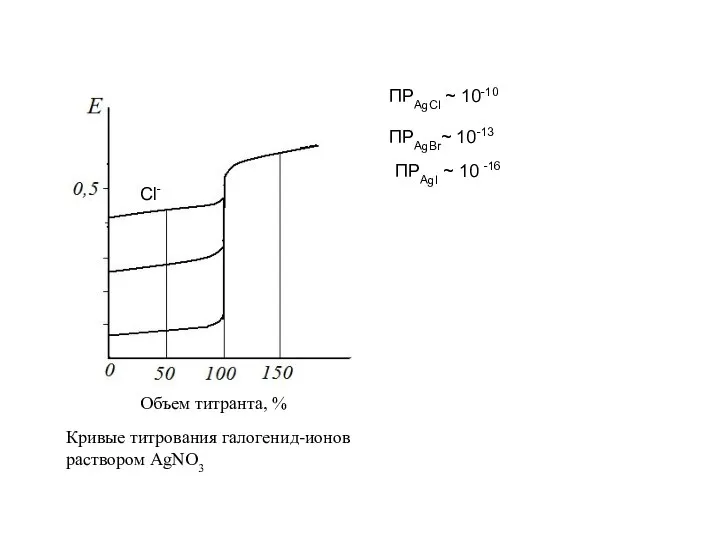
- 48. Объем титранта, % Кривые титрования галогенид-ионов раствором AgNO3 ПРAgCl ~ 10-10 Cl- ПРAgBr~ 10-13 ПРAgI ~
- 49. АI- + B+ = BAI↓ и AII2- + 2B+ = B2AII↓, Например, ионом серебра титруется смесь
- 50. КОМПЛЕКСОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ Bn+ + pA z- = BAp(n-pz) Потенциал индикаторного электрода 1-го рода до точки эквивалентности
- 51. Bz+ + A↔BAz+ Bz+ + A↔BAz+ BAz+ + A↔BA2z+ Bz+ + 2A↔BA2z+ ……………………………………………………………………………………………………… BAi-1z+ + A↔BAiz+
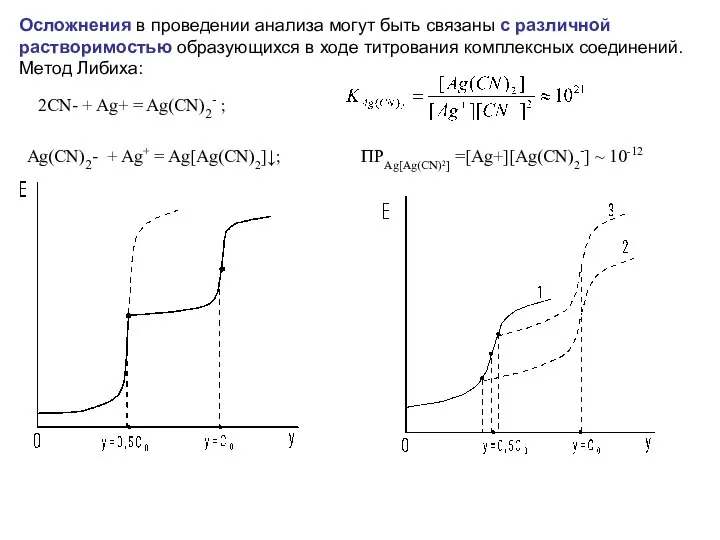
- 52. Осложнения в проведении анализа могут быть связаны с различной растворимостью образующихся в ходе титрования комплексных соединений.
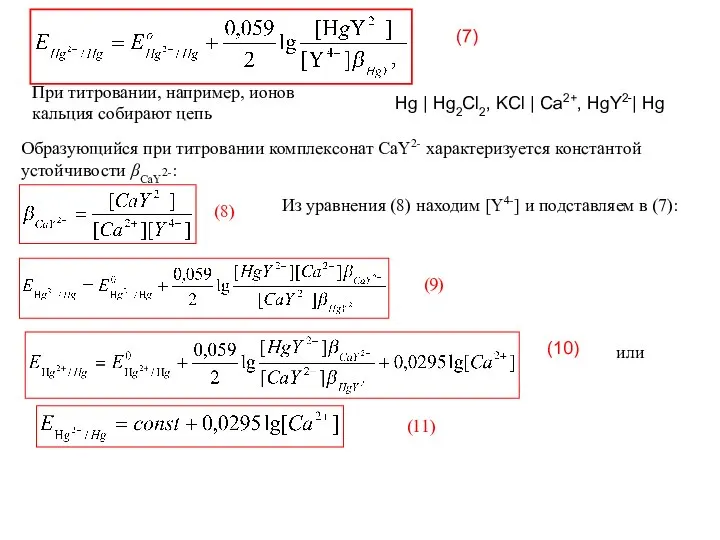
- 53. Хелатометрия (комплексонометрия) (5) При использовании ртутного электрода как индикаторного на его поверхности протекает реакция (6) При
- 54. Образующийся при титровании комплексонат СaY2- характеризуется константой устойчивости βCaY2-: (8) Из уравнения (8) находим [Y4-] и
- 55. (1) (2) (3)
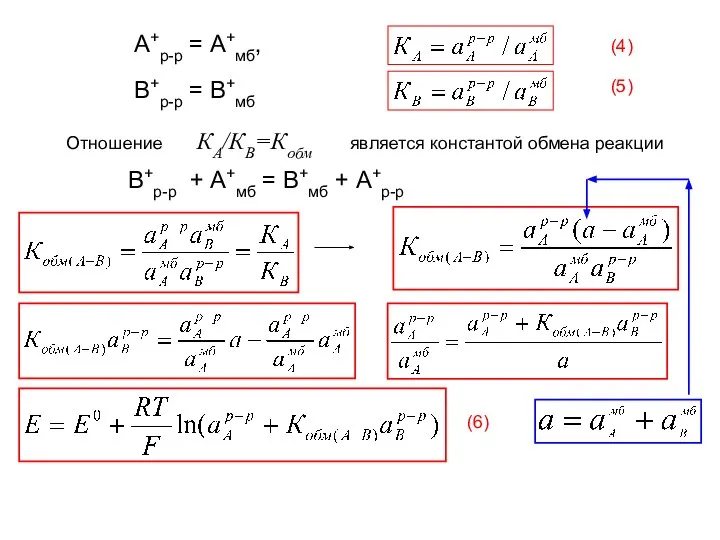
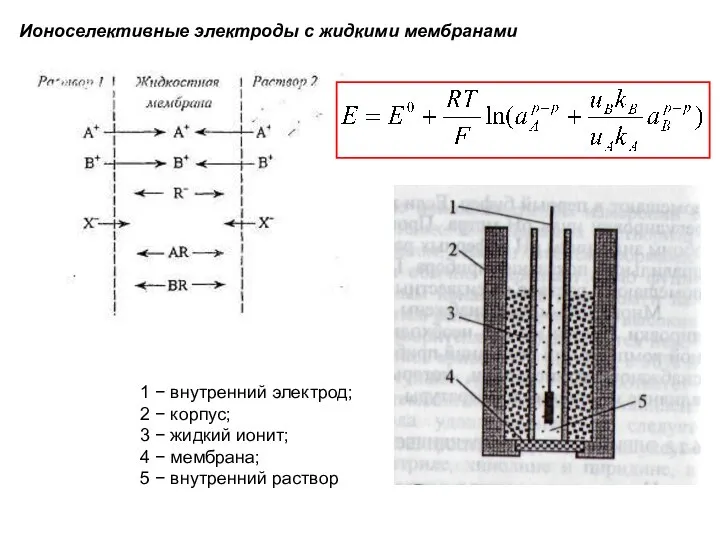
- 56. A+р-р = А+мб, В+р-р = В+мб В+р-р + А+мб = В+мб + А+р-р КА/КВ=Кобм Отношение является
- 57. Величина (иB/иА)Кобм(А-В) в этом выражении называется коэффициентом селективности (КA/B) электрода по отношению к ионам А+ и
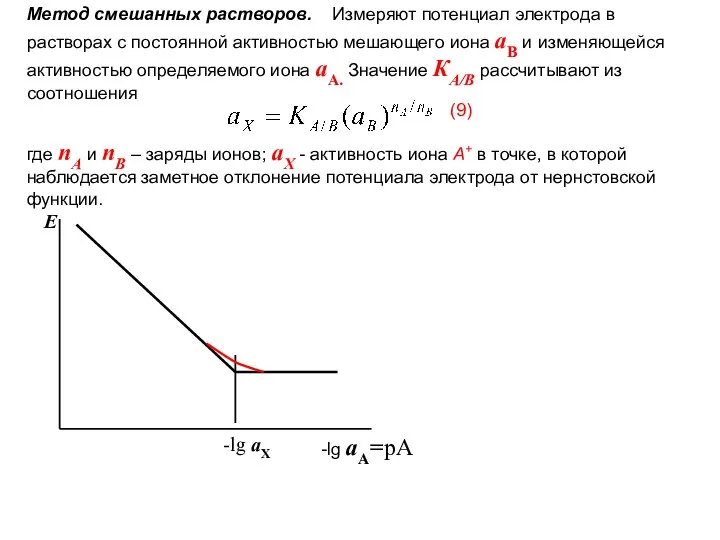
- 58. Метод смешанных растворов. Измеряют потенциал электрода в растворах с постоянной активностью мешающего иона аВ и изменяющейся
- 59. Метод отдельных растворов. Измеряют потенциал электрода в растворе определяемого иона в отсутствие мешающего иона (EА) ,
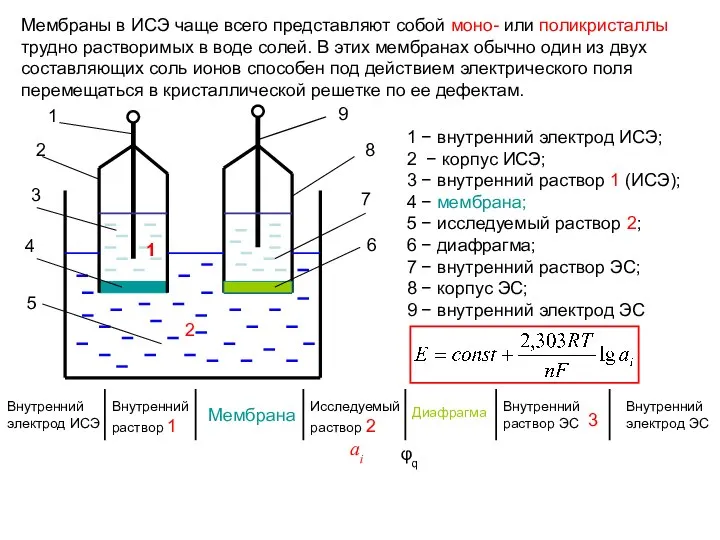
- 60. Мембраны в ИСЭ чаще всего представляют собой моно- или поликристаллы трудно растворимых в воде солей. В
- 61. Электроды с кристаллической мембраной Электрод Мембрана Определяемый Мешающие рН _______________________________ ион________________ ионы___________________ 1. Лантан- LaF3 F
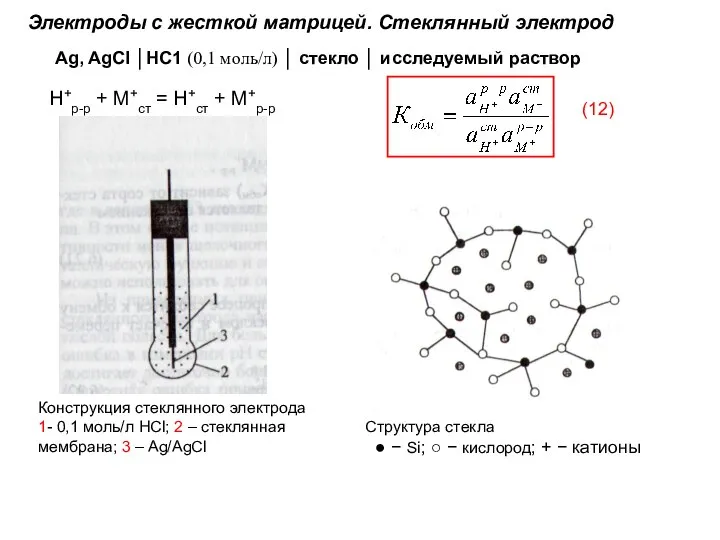
- 62. Электроды с жесткой матрицей. Стеклянный электрод Ag, AgCl │HC1 (0,1 моль/л) │ стекло │ исследуемый раствор
- 63. Если aH+>>Kобма М+, то: Если aH+ В простейшем случае электродный процесс сводится к обмену ионами водорода
- 64. рН 2 11 - Е рН рН>9: щелочная ошибка возникает, когда aH+ ≈ Kобма М+, Натриевое
- 65. Ионоселективные электроды с жидкими мембранами 1 − внутренний электрод; 2 − корпус; 3 − жидкий ионит;
- 66. Первым ИСЭ с жидкой мембраной был кальций-селективный электрод на основе кальциевой соли додецилфосфорной кислоты, растворенной в
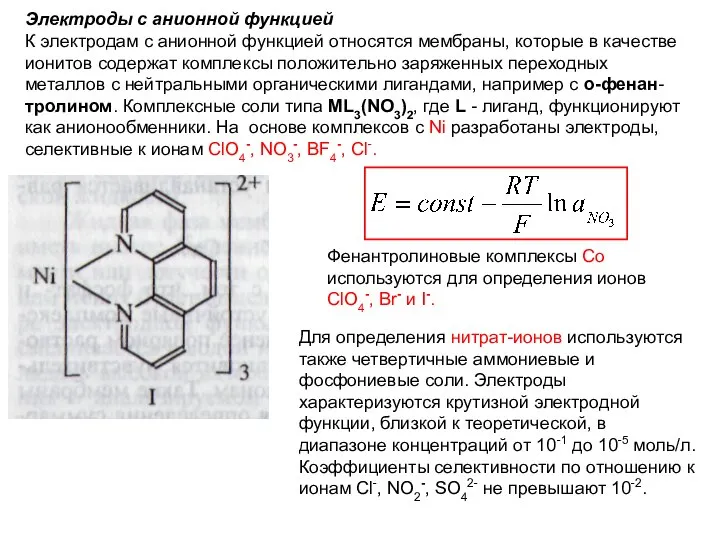
- 67. Электроды с анионной функцией К электродам с анионной функцией относятся мембраны, которые в качестве ионитов содержат
- 68. Ионообменники на основе солей тетраалкиламмония применяют для изготовления хлоридных электродов. В качестве органического катиона в них
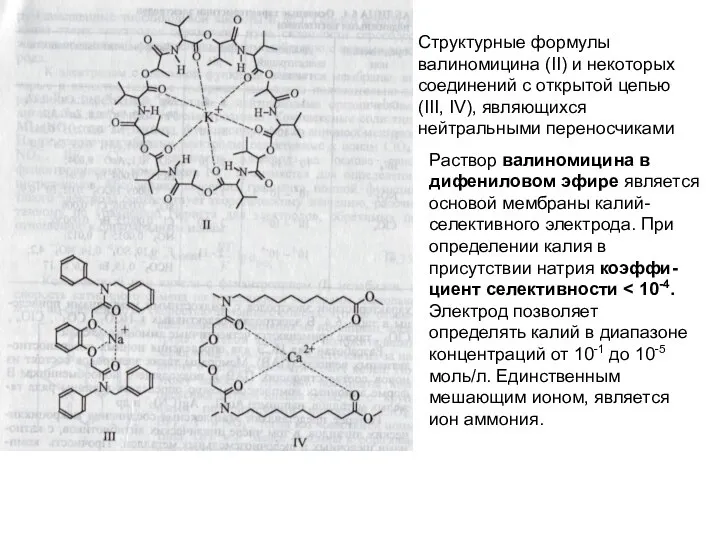
- 69. Структурные формулы валиномицина (II) и некоторых соединений с открытой цепью (III, IV), являющихся нейтральными переносчиками Раствор
- 70. Известны специфические нейтральные переносчики (депсипептиды, макротетролиды, полиэфиры, диамиды карбоновых кислот и др.), которые используются в электродах,
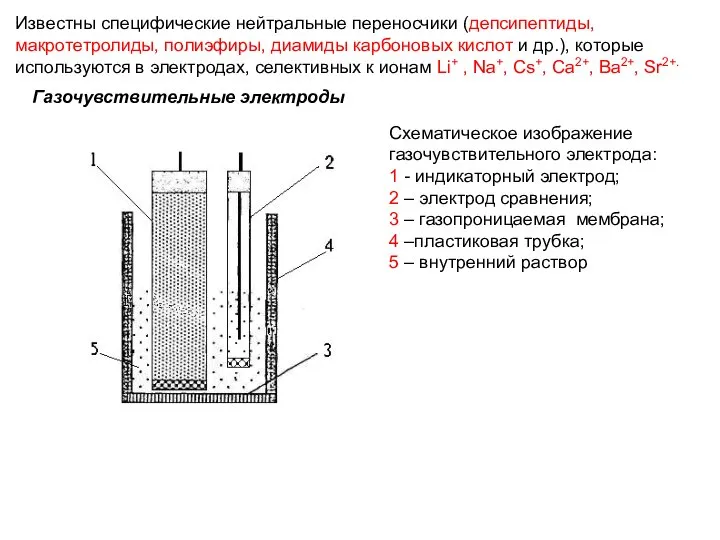
- 71. Типы газочувствительных электродов
- 72. Потенциометрические биосенсоры Если индикаторная реакция катализируется ферментами, то электрохимические системы называют ферментными электродами. В ферментных электродах
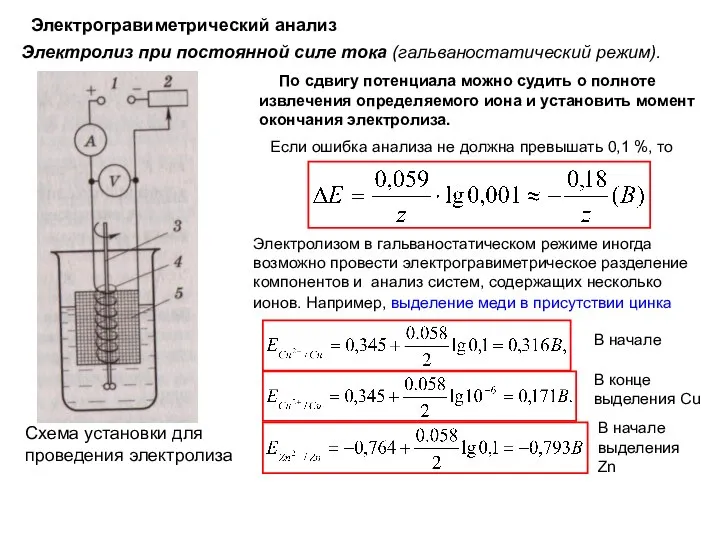
- 74. Электрогравиметрический анализ Электролиз при постоянной силе тока (гальваностатический режим). Схема установки для проведения электролиза По сдвигу
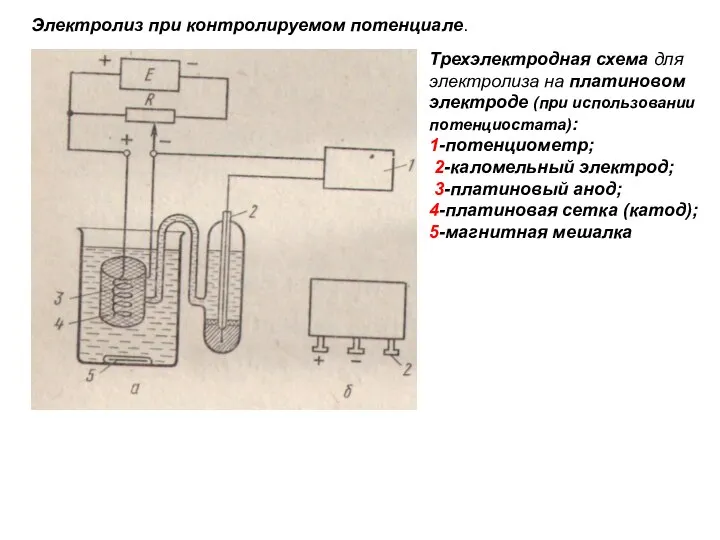
- 75. Электролиз при контролируемом потенциале. Трехэлектродная схема для электролиза на платиновом электроде (при использовании потенциостата): 1-потенциометр; 2-каломельный
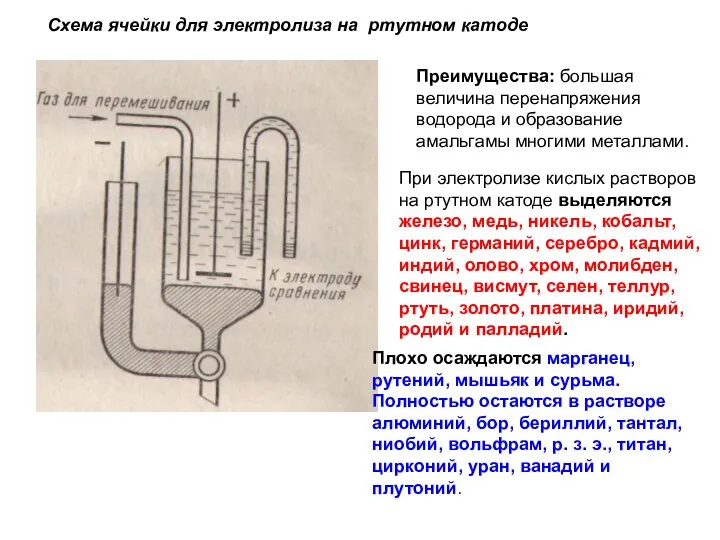
- 76. Схема ячейки для электролиза на ртутном катоде Преимущества: большая величина перенапряжения водорода и образование амальгамы многими
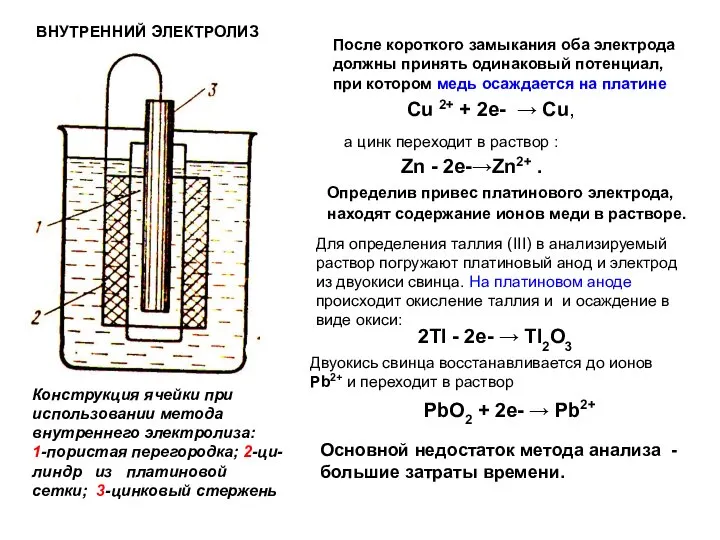
- 77. ВНУТРЕННИЙ ЭЛЕКТРОЛИЗ Конструкция ячейки при использовании метода внутреннего электролиза: 1-пористая перегородка; 2-ци-линдр из платиновой сетки; 3-цинковый
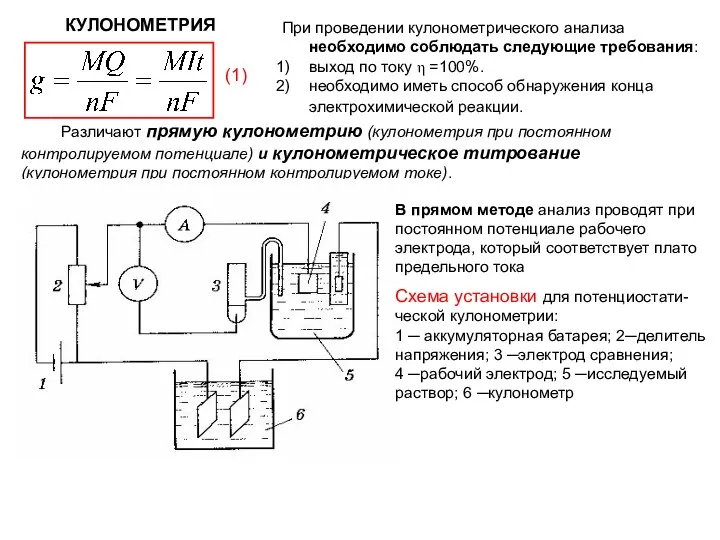
- 78. КУЛОНОМЕТРИЯ При проведении кулонометрического анализа необходимо соблюдать следующие требования: выход по току η =100%. необходимо иметь
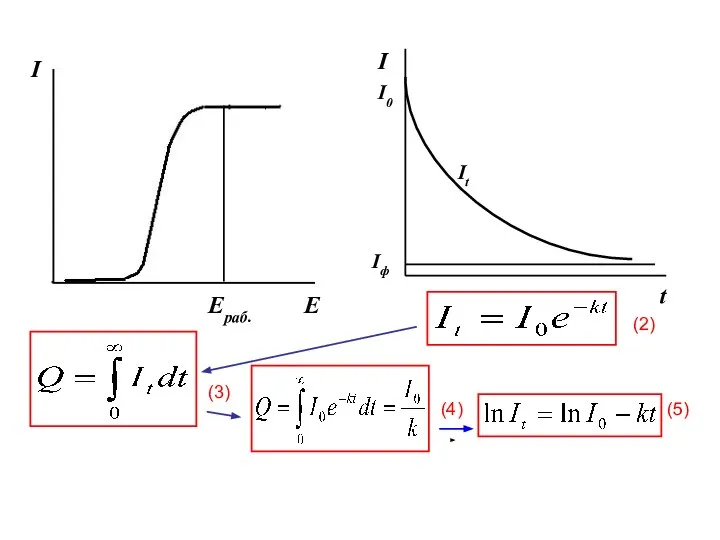
- 79. Eраб. I t E I Iф I0 It (2) (3) (4) (5)
- 81. Скачать презентацию


![y = [B+] = [A-] − [H+] + Kw / [H+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395258/slide-5.jpg)

![[H+] pH P=2,3([H+]+[OH-]) 1 0 ≈ 2,3 1·10-1 1 ≈ 2,30·10-1](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395258/slide-7.jpg)
![Нейтрализация слабой кислоты сильным основанием y = [B+] = [A-] −](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1395258/slide-9.jpg)










































 Элементы IV группы, побочной подгруппы периодической системы Менделеева
Элементы IV группы, побочной подгруппы периодической системы Менделеева Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Альдегиды: химические свойства и применение
Альдегиды: химические свойства и применение Валентность
Валентность Періодичний закон і періодична система хімічних елементів Д.І. Менделєєва. Будова атома
Періодичний закон і періодична система хімічних елементів Д.І. Менделєєва. Будова атома Кристаллы в нашей жизни
Кристаллы в нашей жизни Ионные равновесия в растворах электролитов
Ионные равновесия в растворах электролитов СОЛИ Классификация сложных неорганических веществ
СОЛИ Классификация сложных неорганических веществ Валериановая кислота
Валериановая кислота Применение эксклюзионной хроматографии в биологии
Применение эксклюзионной хроматографии в биологии Stirring in liquid media
Stirring in liquid media Биосинтез и катаболизм пуриновых и пиримидиновых нуклеотидов
Биосинтез и катаболизм пуриновых и пиримидиновых нуклеотидов Бионеорганическая химия. Комплексообразование в организме. (Лекция 3)
Бионеорганическая химия. Комплексообразование в организме. (Лекция 3) Атомно-кристаллическое строение материалов
Атомно-кристаллическое строение материалов Презентация по Химии "ХИМИЯ В НАШЕЙ ЖИЗНИ" - скачать смотреть
Презентация по Химии "ХИМИЯ В НАШЕЙ ЖИЗНИ" - скачать смотреть  Минералы натрия
Минералы натрия Железо, пирит
Железо, пирит Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Игра по химии по теме «Атомы химических элементов. Простые вещества»
Игра по химии по теме «Атомы химических элементов. Простые вещества» Применение неорганических соединений в пищевой промышленности
Применение неорганических соединений в пищевой промышленности Многоатомные Спирты
Многоатомные Спирты  Строение атома
Строение атома Химические средства защиты растений
Химические средства защиты растений Типы химических реакций в органической химии
Типы химических реакций в органической химии Неорганическая химия 8 класс г. Азов школа №9 учитель: Карасёв Евгений Владимирович
Неорганическая химия 8 класс г. Азов школа №9 учитель: Карасёв Евгений Владимирович  Электролиз воды
Электролиз воды Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности
Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности Состав воздуха и его загрязненность Отдел образования администрации Тальменского района Алтайского края
Состав воздуха и его загрязненность Отдел образования администрации Тальменского района Алтайского края