Содержание
- 2. Мета відкритого заняття: Навчальна: повторити і узагальнити основні поняття з теми, закріпити вміння за електронною формулою
- 3. Тип уроку: комбінований, урок узагальнення та систематизації знань Методи, прийоми роботи: практичні – розв’язування задач, вправ;
- 4. Хід заняття І. Організаційний етап ІІ. Повторення домашнього завдання Виконання досліду з допомогою віртуальної лабораторії з
- 5. ДЗ. Задача на генетичний зв'язок неорганічних речовин: У ривок з роману Луи Буссенару «Викрадачі діамантів» «
- 6. Злива, що осталася після грози, залила всю цю величезну масу негашеного вапна. Вона розбухла, почала з
- 7. Завдання: а) Які хімічні процеси відбулися в печері? б) напишіть рівняння відповідних реакцій. в) сформулюйте узагальнюючий
- 8. Вихідні речовини: вугілля, вапняк, вода, кисень, метан, вогонь Кислотні оксиди СН 4 + 2О2 =СО2 +2Н2О
- 9. Пам'ятаймо! Хімічні речовини та продукти, дорожньо будівельні матеріали на їх основі, паливо, потребують уваги, так як
- 10. Періодичний закон, періодична система елементів Д.І. Менделєєва і будова атома. Види хімічного зв’язку План заняття: 1.
- 11. Заповіт Дмитрія Менделеева « Главный секрет жизни вот какой: один человек – нуль, вместе только люди.
- 12. Періодичний закон. Періодична система хімічних елементів «Истина одна, а путей отыскания много» Д.Менделєєв Формулювання Періодичного закону,
- 13. За якими даними можна знайти хімічний елемент у даній таблиці? Японська ПСХЕ
- 14. Інформацію про будову атома дає: Порядковий номер елементу Номер групи Номер періоду Можна визначити, користуючись таблицею
- 15. Теорія будови атома Атом — це електронейтральна частинка, що складається з позитивно зарядженого ядра, нейтральних часток
- 16. Маси протона та нейтрона приблизно однакові, їх приймають рівними 1 Атоми з однаковим зарядом ядра складають
- 17. He42 He42 Число позитивно заряджених протонів у ядрі дорівнює числу негативно заряджених електронів, тобто атом у
- 18. Порядковий номер елементу – загальне число електронів у атомі, які утворюють електронну оболонку атома. Порядковий номер
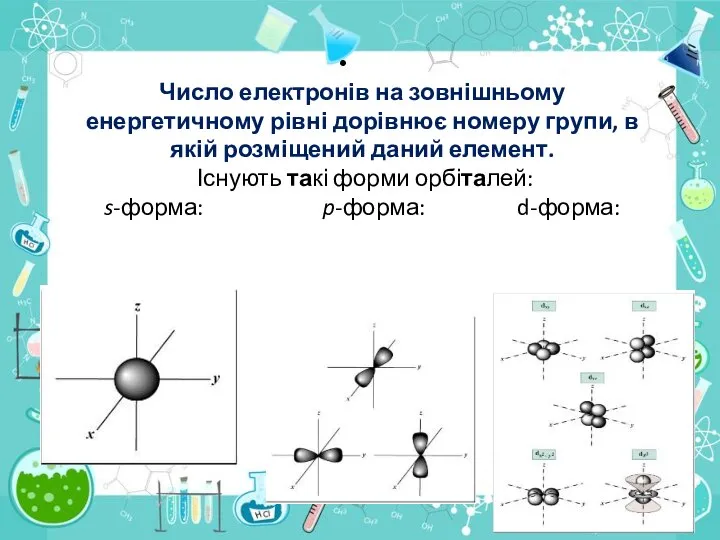
- 19. Число електронів на зовнішньому енергетичному рівні дорівнює номеру групи, в якій розміщений даний елемент. Існують такі
- 20. Простір навколо ядра, у якому найімовірніше перебування електрона, називається орбіталлю. Електрон у атомі не рухається за
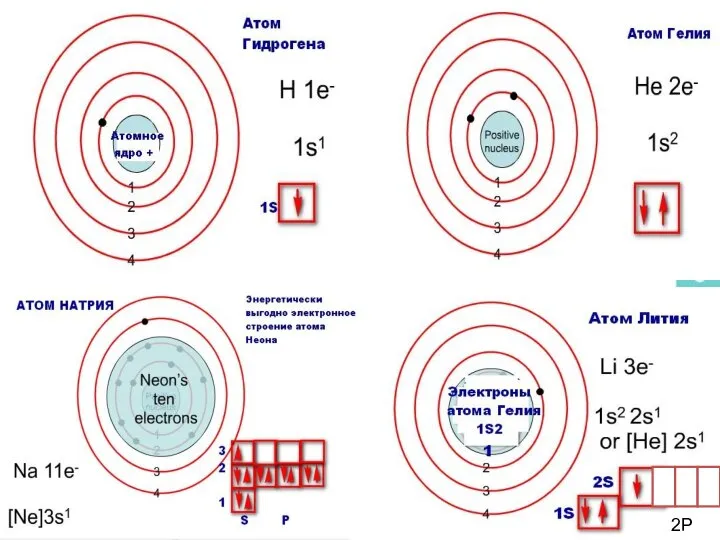
- 21. Розподіл електронів по енергетичним рівням Третій період 3 енергетичних рівня n=3 кількість орбіталей n2=9 електронів 2
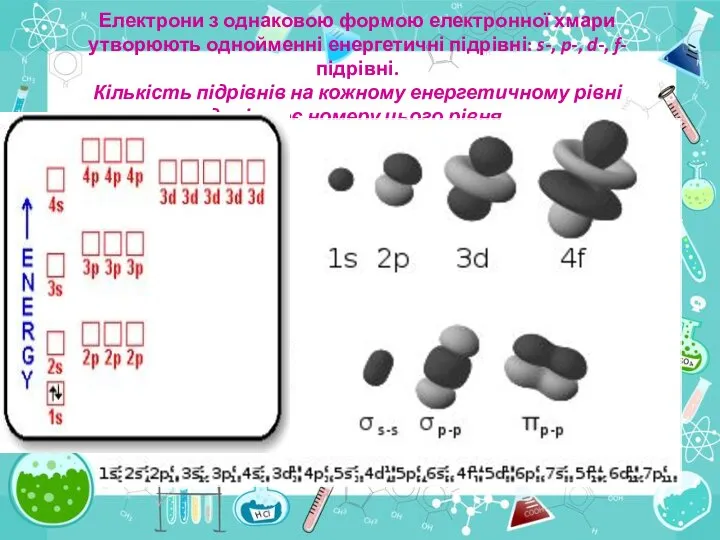
- 22. Електрони з однаковою формою електронної хмари утворюють однойменні енергетичні підрівні: s-, p-, d-, f- підрівні. Кількість
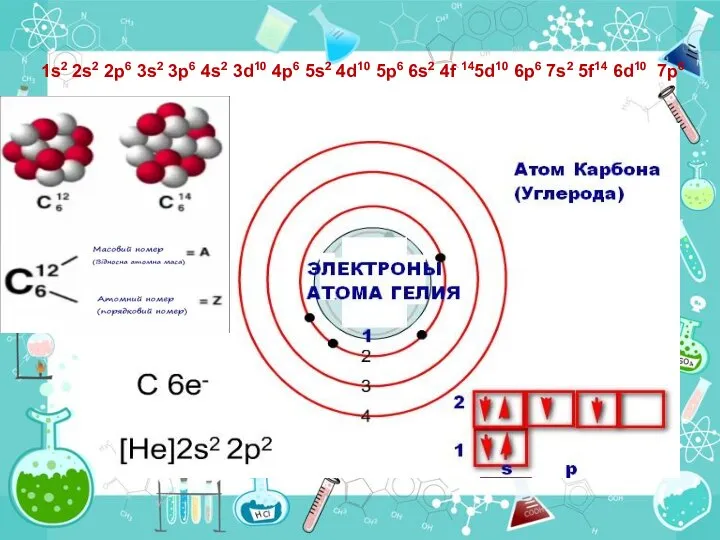
- 24. 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f 145d10 6p6 7s2
- 25. 2Р
- 26. Подумайте: В ядрі атома 30 протонів та 35 нейтронів. Який порядковий номер та відносна атомна маса
- 28. Знайти елементи за будовою їх електронних шарів: a)1S22S2 b)1S22S22P3 c)1S22S22P63S1 d)1S22S22P63S2 а) одного періоду б) однієї
- 29. Знайти елементи за будовою їх електронних шарів: а) одного періоду другого 1S22S2 1S22S22P3 третього 1S22S22P63S1 1S22S22P63S2
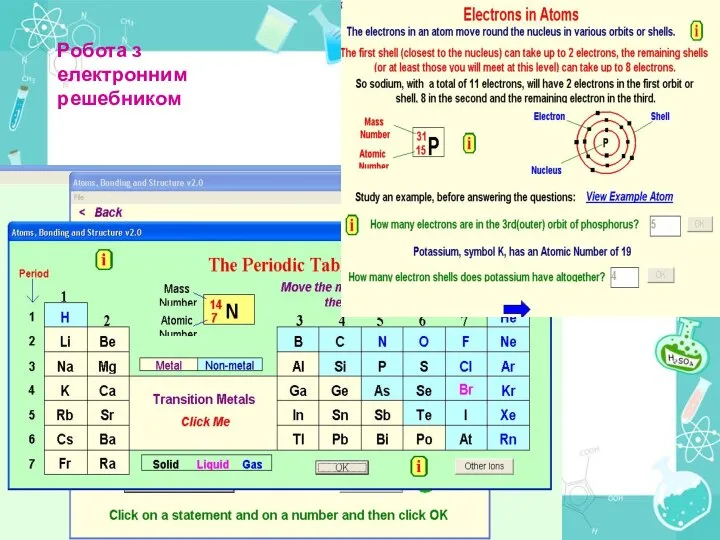
- 30. Робота з електронним решебником
- 31. Типи хімічного зв'язку Йонний зв’язок – зв’язок між йонами
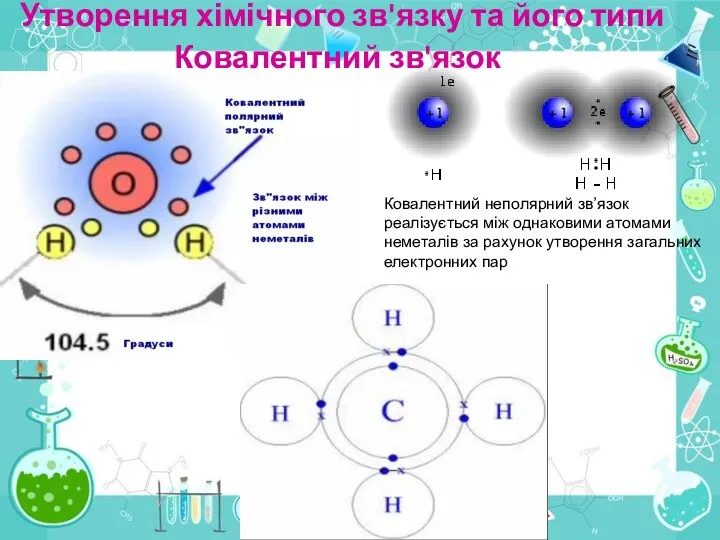
- 32. Утворення хімічного зв'язку та його типи Ковалентний зв'язок Ковалентний неполярний зв’язок реалізується між однаковими атомами неметалів
- 33. В комплект презентации входят видеофильмы, которые расположены на сайте автора Иволга сайт химии и биологии В
- 34. Металічний зв’язок Водневий зв’язок це зв’язок між позитивними йонами металів, що знаходяться у вузлах кристалічних ґраток,
- 36. Робота з електронним решебником
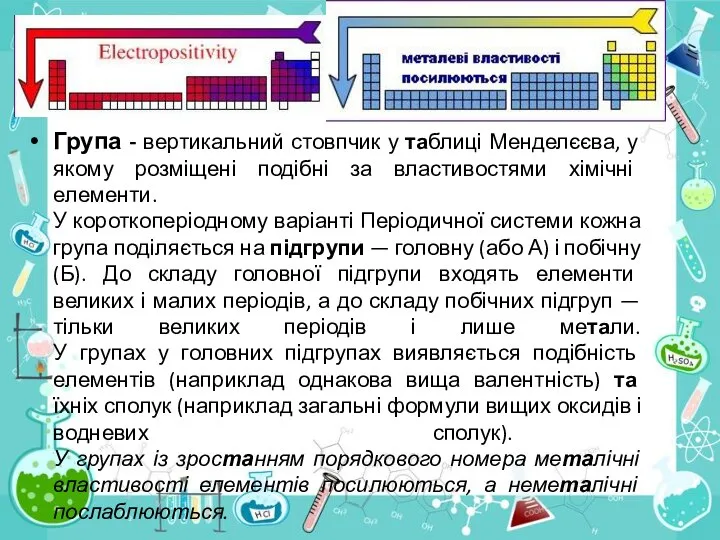
- 37. Група - вертикальний стовпчик у таблиці Менделєєва, у якому розміщені подібні за властивостями хімічні елементи. У
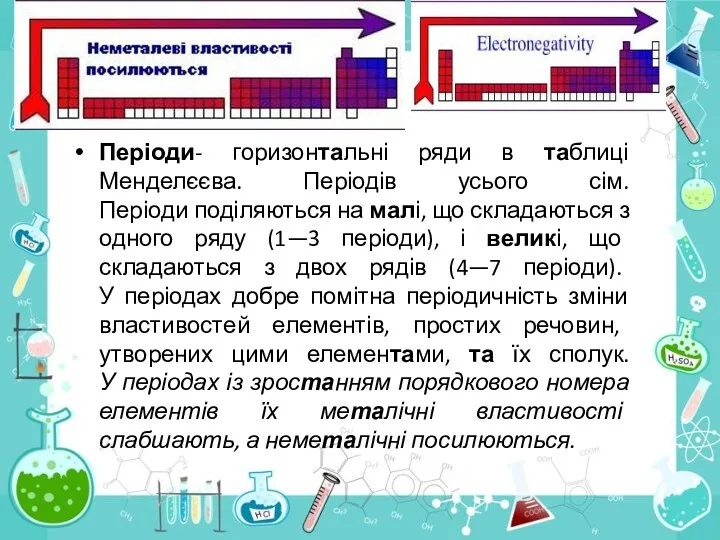
- 38. Періоди- горизонтальні ряди в таблиці Менделєєва. Періодів усього сім. Періоди поділяються на малі, що складаються з
- 39. Фізичний зміст Періодичного закону В атомах елементів із зростанням порядкового номера відбувається збільшення кількості протонів у
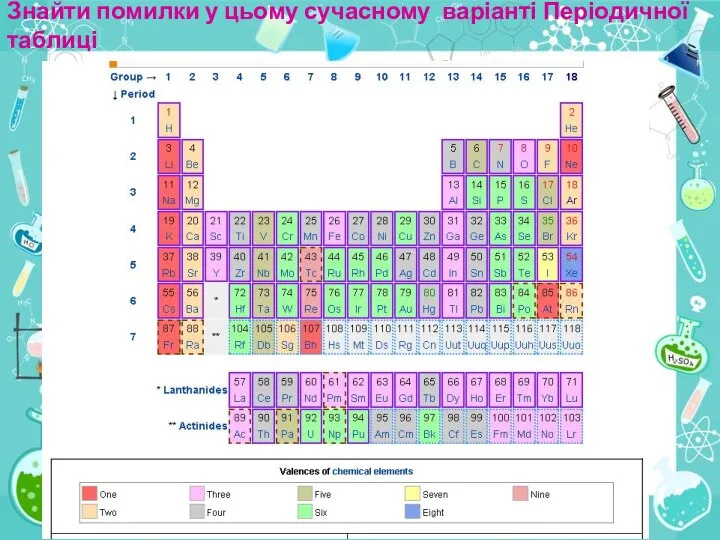
- 40. Знайти помилки у цьому сучасному варіанті Періодичної таблиці
- 41. Електронегативність Електронегативність — здатність атома притягати до себе електрони інших атомів (маються на увазі валентні електрони
- 43. Самоперевірка
- 44. Вірні відповіді: Кожна вірна відповідь 1 бал!
- 45. Контроль знань а) Серед наведених електронних конфігурацій вкажіть ті, які не можуть існувати: 1р3, Зр6, 5d2,
- 46. Взаємоперевірка за зразком Вірні відповіді для самоаналізу: А) 1р3 - на першому енергетичному рівні не можуть
- 47. Валентності хлору I
- 48. ДОМАШНЄ ЗАВДАННЯ Ярошенко О.Г. Хімія : Підручн. для 10кл заг.осв. навч. закл. – К.: Грамота, 2010§
- 49. Д.Менделєєв- Російський Ленардо да Винчи В 7 августа 1887г., Д.И.Менделеев совершил самостоятельный полет для наблюдения солнечного
- 51. Скачать презентацию







































 Простые вещества, металлы
Простые вещества, металлы Глобальні екологічні проблеми повязані з добуванням та переробкою вуглеводної сировини Підготувала учениця 11-А класу Гребі
Глобальні екологічні проблеми повязані з добуванням та переробкою вуглеводної сировини Підготувала учениця 11-А класу Гребі Бетаин (триметилглицин)
Бетаин (триметилглицин) Обобщающий урок по теме: Простые вещества Учитель химии I квалификационной категории Сучкова Н.В. 2009г.
Обобщающий урок по теме: Простые вещества Учитель химии I квалификационной категории Сучкова Н.В. 2009г. Русские ученые-химики
Русские ученые-химики Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ
Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ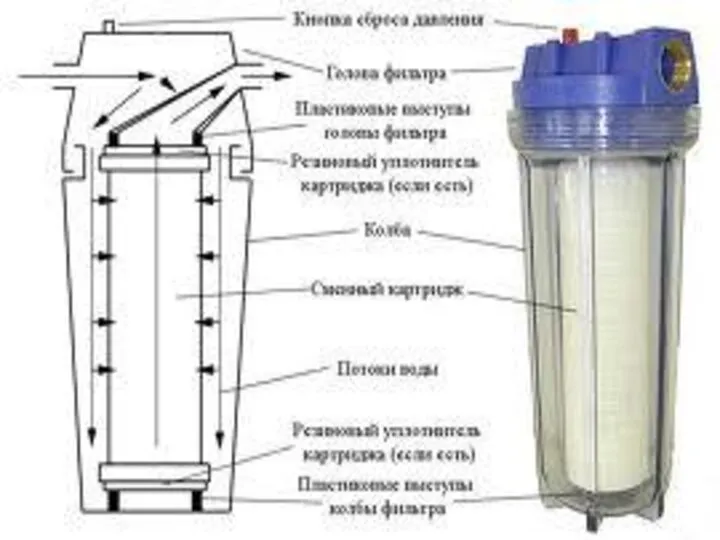 Суды тазарту әдістері
Суды тазарту әдістері Сероводород, сернистый водород
Сероводород, сернистый водород Карбонильные соединения
Карбонильные соединения Презентация на тему "Коллоидная химия"
Презентация на тему "Коллоидная химия" Источники сырья для производства полимера полиуретана, области применения, его свойства, объемы его производства
Источники сырья для производства полимера полиуретана, области применения, его свойства, объемы его производства Ерітінділер. Ерітінділердің химиялық теориясы
Ерітінділер. Ерітінділердің химиялық теориясы Углерод и его соединения
Углерод и его соединения Общая и неорганическая химия
Общая и неорганическая химия Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.
Органическая химия: «Жиры» Орлова Ольга Николаевна Школа №357 Приморского р-на.  Альдегиды (номенклатура и изомерия)
Альдегиды (номенклатура и изомерия) Присадки к маслам
Присадки к маслам Алканы. Строение и свойства алканов
Алканы. Строение и свойства алканов Карбонові кислоти
Карбонові кислоти Открытия в химии Теория Александра Бутлерова
Открытия в химии Теория Александра Бутлерова Физические методы анализа
Физические методы анализа Презентация по химии Биополимеры и их компоненты
Презентация по химии Биополимеры и их компоненты  Характеристика высших гидроксидов по положению в ПСХЭ
Характеристика высших гидроксидов по положению в ПСХЭ Энергетика химических процессов. Энтропия и энергия Гиббса
Энергетика химических процессов. Энтропия и энергия Гиббса Стеариновая кислота
Стеариновая кислота Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс
Основные понятия аналитической химии. Положения теории растворов электролитов и закона действующих масс Роль химии в нашей жизни
Роль химии в нашей жизни Применение муравьиного спирта
Применение муравьиного спирта