Содержание
- 2. * Лекция №2 Введение. Литература. Классификация и суть методов анализа живых систем. Особенности анализа живых систем.
- 3. * Введение Данный курс посвящен изучению методов анализа живых систем (биологических методов анализа) В научных биологических
- 4. * Литература Г.А. Урванцева, Е.Л.Грачева.Методы анализа живых систем: уч. пособие.Яросл. гос. ун-т им.П.Г. Демидова,-Ярославль:ЯрГУ, 2013.-104 с.
- 5. * Классификация и суть биологических методов анализа I. Оптические (спектральные методы): 1.Абсорбционная спектроскопия: а).Измерение светопоглощения,фотометрия ,
- 6. * 2.Рефрактометрия (измерение показателя преломления веществ).Например, определение концентрации белка в биологической жидкости. --------------------------------------------------------------- II.Электрохимические методы: 1.Электрофорез
- 7. * Ш.Хроматографические методы анализа- это методы, основанные на различии скорости переноса веществ в системе двух фаз,
- 8. * IV.Гидродинамические методы. 1.центрифугирование. 2.ультрацентрифугирование. 3.вискозиметрия. V.Метод рентгеноструктурного анализа. VI.Иммунохимические методы (ИФА,ИХА). VII.ПЦР и метод молекулярных
- 9. * Особенности анализа живых систем Исходный материал (биомасса), из которого предстоит выделить интересующее вещество – состоит
- 10. * Работа с биологическими объектами заключается в необходимости манипулировать с очень маленькими количествами вещества: мг, мкг
- 11. * Хроматография – физико-химический метод, используется для разделения веществ аналитические цели препаративные цели
- 12. * Принцип хроматографического разделения веществ Неподвижная фаза Подвижная фаза Молекулы разделяемых веществ Эффект разделения основывается на
- 13. * Из истории хроматографии Михаил Семёнович Цвет (1872—1919) День рождения хроматографии – 21 марта 1903 г.
- 14. * Классификация методов хроматографии По типу агрегатного состояния фаз Газовая хроматография (ГХ) Жидкостная хроматография (ЖХ) По
- 15. * Классификация методов хроматографии По форме проведения процесса Плоскостная Колоночная По цели проведения процесса Анализ качественного
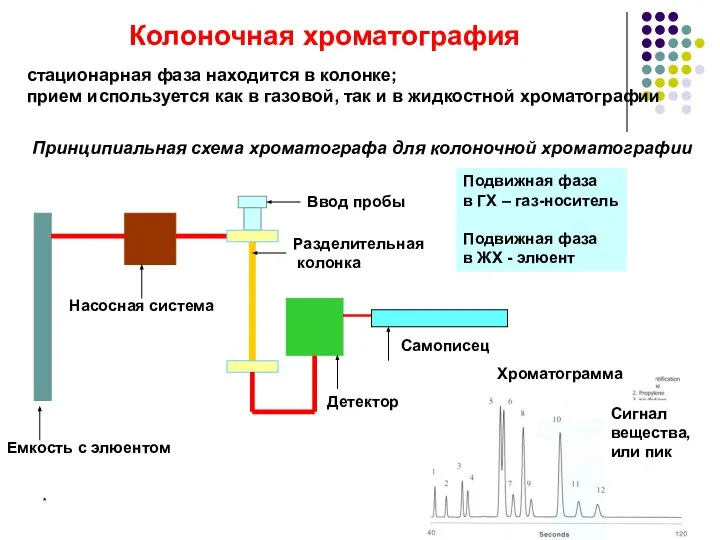
- 16. * Колоночная хроматография стационарная фаза находится в колонке; прием используется как в газовой, так и в
- 17. * Хроматограмма Хроматографический пик – концентрация пробы в подвижной фазе на выходе из колонки как функция
- 18. * высокоэффективная жидкостная хроматография (ВЭЖХ), высокоэффективная тонкослойная хроматография (ВЭТСХ), высокоэффективная ионная хроматография (ВЭИХ), сверхкритическая флюидная хроматография
- 19. * Хроматографические методы очистки белков Ионообменная хроматография Хроматография гидрофобных взаимодействий Гель-проникающая хроматография Афинная хроматография --------------------------------------------------------- Эти
- 20. * ВИРТУАЛЬНАЯ ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ http://phram.ru/ChromLab/ (адрес в Интернете) 66525536652553@mail.ru (e-mail) OVY123 (пароль) Раздел оборудование/процесс (пошаговый) +
- 21. * Контрольные вопросы по окончании работы: Назначение хроматографической установки Biologic LР? Что такое ВЭТТ? Что такое
- 23. Скачать презентацию



















 Реакции при участии катализатора
Реакции при участии катализатора Диоксины и полихлорированные бифенилы: источники, распространение в окружающей среде, влияние на организм человека
Диоксины и полихлорированные бифенилы: источники, распространение в окружающей среде, влияние на организм человека Бактериалық жасушаның химиялық құрамы
Бактериалық жасушаның химиялық құрамы Создание косметических средств
Создание косметических средств Термодинамика и термохимия процессов горения и взрыва
Термодинамика и термохимия процессов горения и взрыва Шыны тәріздес фосфат
Шыны тәріздес фосфат Обобщение по теме неметаллы
Обобщение по теме неметаллы Хімія в медицині
Хімія в медицині  Получение металлов
Получение металлов  Химия в произведениях художественной литературы
Химия в произведениях художественной литературы Элементы группы галогенов
Элементы группы галогенов Степень окисления
Степень окисления Презентация по Химии "Вода как растворитель" - скачать смотреть
Презентация по Химии "Вода как растворитель" - скачать смотреть  Технологии, используемые в исследованиях лаборатории механизмов нейрохимической модуляции
Технологии, используемые в исследованиях лаборатории механизмов нейрохимической модуляции Реакции разложения и реакции соединения
Реакции разложения и реакции соединения Химические сюжеты в научно-фантастических произведениях
Химические сюжеты в научно-фантастических произведениях Простые и сложные эфиры
Простые и сложные эфиры Решение задач по уравнениям химических реакций
Решение задач по уравнениям химических реакций Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Білки. Властивості та функції
Білки. Властивості та функції Спирты. Классификация, номенклатура, изомерия. Спирты в природе
Спирты. Классификация, номенклатура, изомерия. Спирты в природе Реакции ионного обмена и условия их осуществления
Реакции ионного обмена и условия их осуществления Минералы земной коры
Минералы земной коры Электрохимические методы анализа: потенциометрия. Потенциометрическое титрование
Электрохимические методы анализа: потенциометрия. Потенциометрическое титрование Представники d-елементів (перехідних елементів) періодичної системи елементів
Представники d-елементів (перехідних елементів) періодичної системи елементів “Су. Ерітінділер” тарауын қорытындылау
“Су. Ерітінділер” тарауын қорытындылау Гетероциклические соединения
Гетероциклические соединения Снег и лед. Тайны твердой воды
Снег и лед. Тайны твердой воды