Содержание
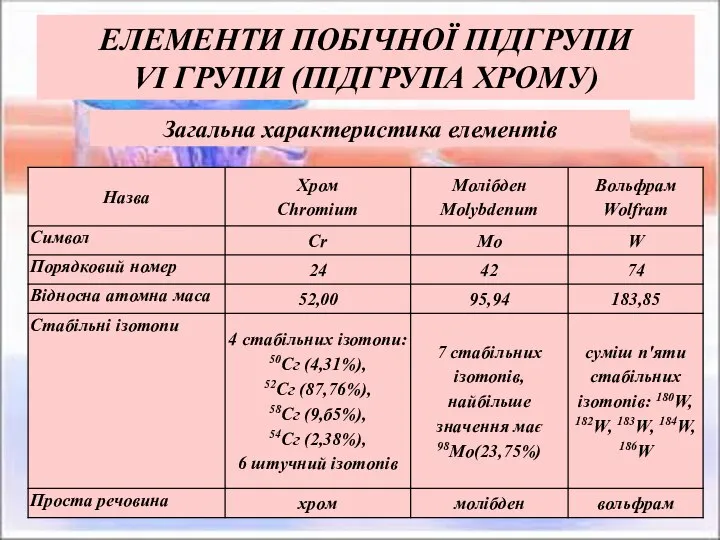
- 2. ЕЛЕМЕНТИ ПОБІЧНОЇ ПІДГРУПИ VІ ГРУПИ (ПІДГРУПА ХРОМУ) Загальна характеристика елементів
- 3. Електронна будова атомів Хром – сріблясто-білий метал, твердий, тугоплавкий (tпл = 19030С). При кімнатній температурі він
- 4. Фізичні властивості Хром на холоді дуже інертний елемент. При нагріванні його хімічна активність підвищується. Характерні реакції
- 5. Хімічна активність в ряді Cr-Mo-W суттєво зменшується. Хром розчиняється в розбавленій хлоридній та сульфатній кислотах. Cr
- 6. Вольфрам при звичайних умовах стійкий. При нагріванні до 400-500 °С окиснюється на повітрі до WO2. З
- 7. Оксид хрому (ІІ) CrO та гідроксид хрому (ІІ) Сr(OH)2 проявляють основні властивості та реагують з кислотами
- 8. Оксид хрому (ІІІ) Cr2O3: зеленого забарвлення тверда речовина, нерозчинна у воді; проявляє амфотерні властивості; при сплавленні
- 9. В залежності від умов (температура, концентрація солі, рН середовища) склад гідратованих комплексів хрому (ІІІ) змінюється, це
- 10. Оксид хрому (VІ) CrO3: яскраво червоні кристали, розчинні у воді; типовий кислотний оксид, утворює хромову кислоту
- 11. Хром — один із необхідних елементів в організмі людини. Бере участь в обміні жирів, білків, вуглеводів.
- 12. Хром застосовується в металургії з метою підвищення міцності й твердості сталей, в електротехніці при виготовленні електроприладів,
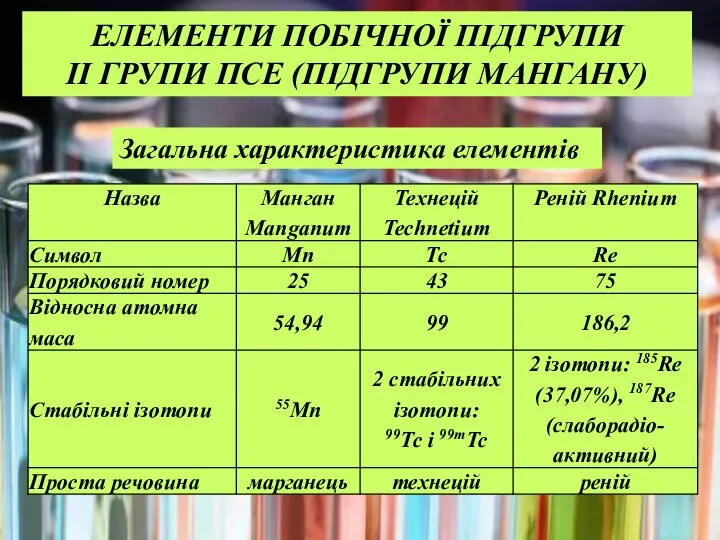
- 13. Загальна характеристика елементів ЕЛЕМЕНТИ ПОБІЧНОЇ ПІДГРУПИ II ГРУПИ ПСЕ (ПІДГРУПИ МАНГАНУ)
- 14. Електронна будова атомів
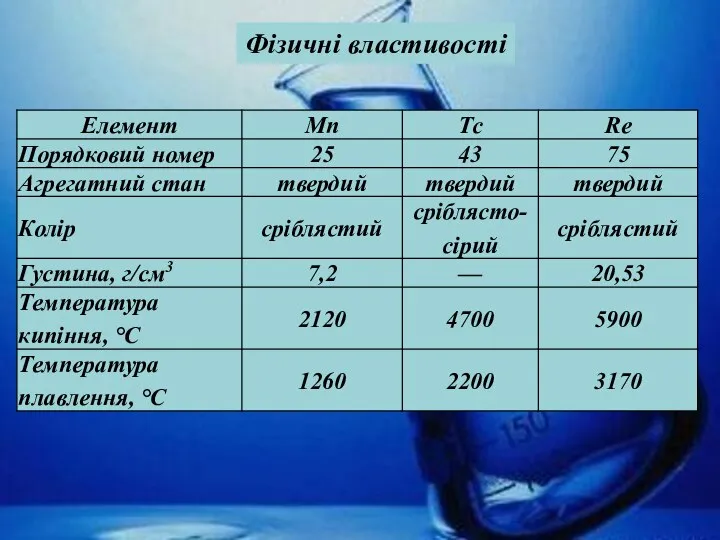
- 15. Фізичні властивості
- 16. В холодній нітратній кислоті манган пасивується. Хімічна активність металів в ряді Mn – Tc – Re
- 17. Реній при звичайних умовах стійкий. Взаємодія з оксигеном відбувається при нагріванні до t > 300°С: утворюються
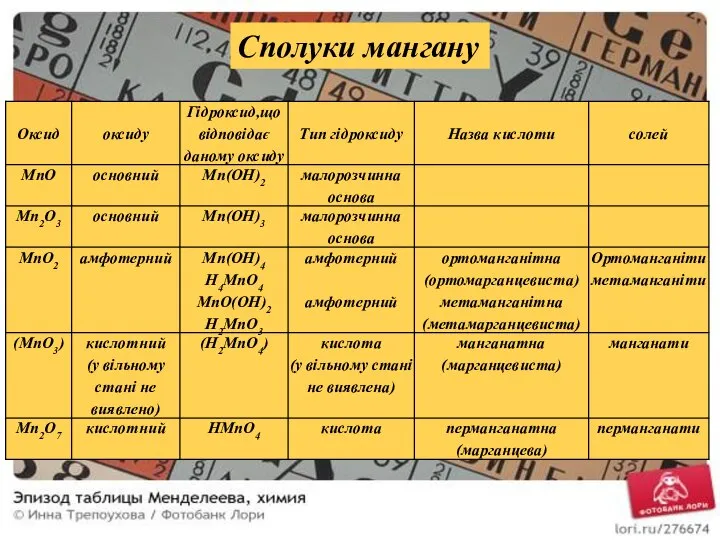
- 18. Сполуки мангану
- 19. У повній відповідності із властивостями оксидів знаходяться властивості гідроксидів: Характер і властивості оксидів і гідроксидів мангану
- 20. Всі сполуки мангану (ІІ) виявляють тільки відновні властивості: Mn2+(OH)2 + H2O1-2 = Mn4+O(OH)2 + H2O Оксид
- 21. Оксид мангану (ІV) - MnO2 – амфотерний оксид. Кислотні та основні властивості виявлені слабко. MnO2 +
- 22. Оксид мангану (VI) – MnO3 – кислотний оксид MnO3 → H2MnO4 манганатна кислота гідроліз K2MnO4 +
- 23. Здатні утворювати стійкі у твердому стані солі зменшується у ряду Мn(ІІ) → Мn(ІІІ) → Mn(IV). Так,
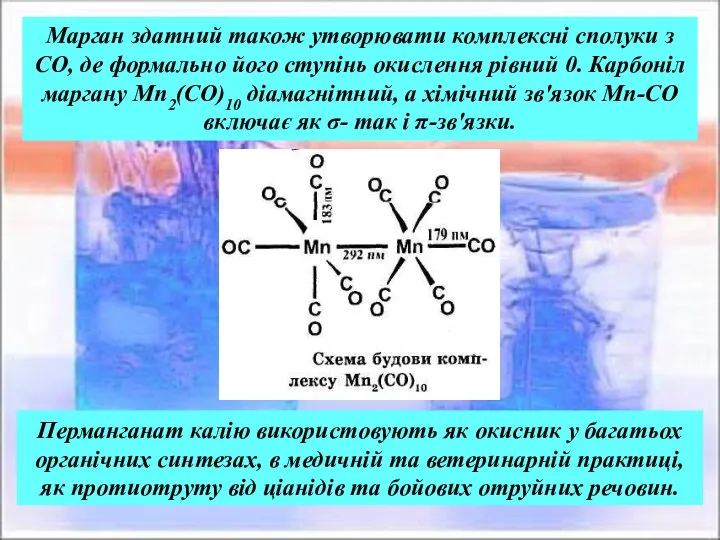
- 25. Перманганат калію використовують як окисник у багатьох органічних синтезах, в медичній та ветеринарній практиці, як протиотруту
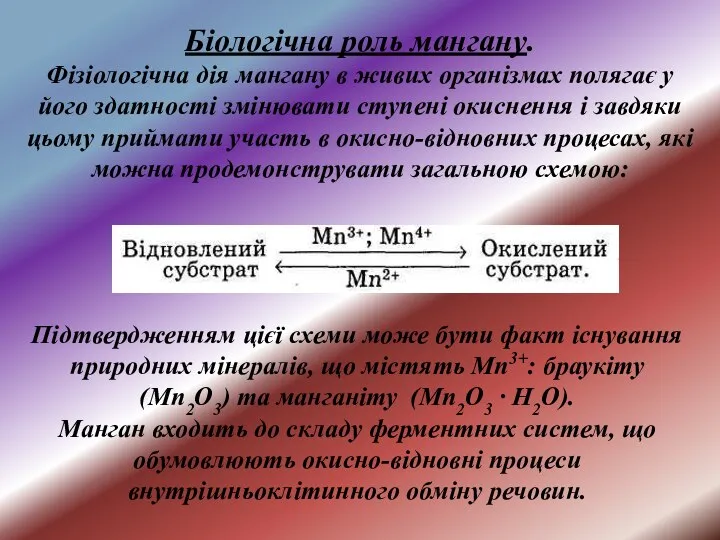
- 26. Підтвердженням цієї схеми може бути факт існування природних мінералів, що містять Мn3+: браукіту (Мn2О3) та манганіту
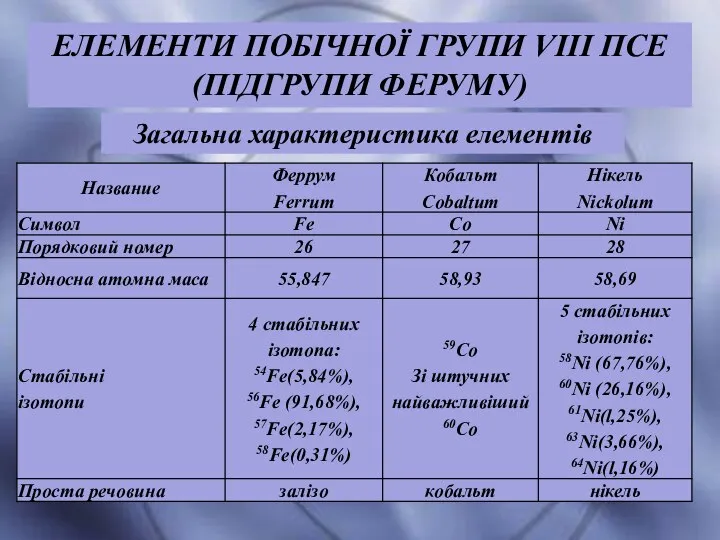
- 27. Загальна характеристика елементів ЕЛЕМЕНТИ ПОБІЧНОЇ ГРУПИ VIII ПСЕ (ПІДГРУПИ ФЕРУМУ)
- 28. Електронна будова атомів
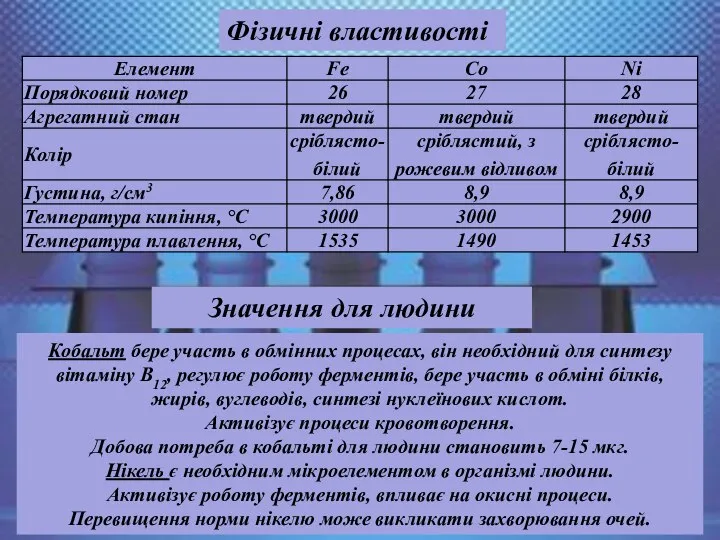
- 29. Фізичні властивості Кобальт бере участь в обмінних процесах, він необхідний для синтезу вітаміну В12, регулює роботу
- 30. Фізичні властивості Залізо Fe — м'який метал сріблясто-білого кольору з металевим блиском. Характеризується високою пластичністю, ковкістю,
- 31. 3. Взаємодія з неметалами при нагріванні: Fe + S → FeS — ферум (II) сульфід 3Fe
- 32. 5. Взаємодія з концентрованими кислотами при нагріванні: 2Fe + 6Н2SО4(конц) → Fe2(SO4)3 + 3SO2↑ + 6Н2О
- 33. СПОЛУКИ ФЕРУМУ Оксиди
- 34. Гідроксиди
- 35. Солі Феруму
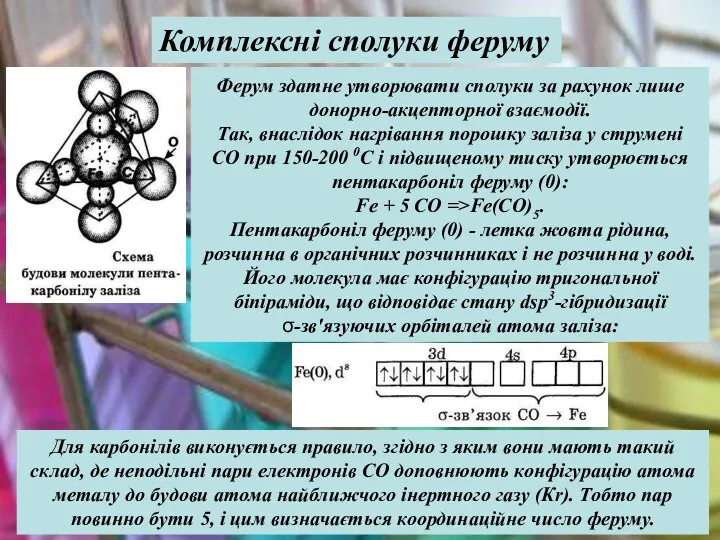
- 36. Ферум здатне утворювати сполуки за рахунок лише донорно-акцепторної взаємодії. Так, внаслідок нагрівання порошку заліза у струмені
- 37. Найбільш стійкі комплексні сполуки феруму утворюються з лігандами CN- - залишками ціанідної кислоти: FeSO4 + 6KCN
- 38. Значення для людини Залізо — необхідний елемент для життєдіяльності організм людини. Бере участь синтезі гемоглобіну, міоглобіну,
- 40. ,
- 42. Скачать презентацию




























 ФОСФОР Абдуллина Альфия Ахнафовна учитель химии МБОУ СОШ с.Никифарово МР Альшеевский район РБ
ФОСФОР Абдуллина Альфия Ахнафовна учитель химии МБОУ СОШ с.Никифарово МР Альшеевский район РБ  Соединения галогенов
Соединения галогенов Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Что объединяет вещества. Классификация твёрдых веществ
Что объединяет вещества. Классификация твёрдых веществ Химическая физика горения
Химическая физика горения Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н
Феромагнетики До феромагнетики (ferrum - залізо) належать речовини, магнітна сприйнятливість яких позитивна і досягає значень. Н Кольцевые силикаты
Кольцевые силикаты Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Кислоты. Индикаторы
Кислоты. Индикаторы Химическая промышленность
Химическая промышленность Алициклические и гетероциклические соединения. Тема № 7, 8
Алициклические и гетероциклические соединения. Тема № 7, 8 Производные карбоновых кислот
Производные карбоновых кислот Жир жиру рознь. Супер омега 3
Жир жиру рознь. Супер омега 3 Экстракция
Экстракция Серная кислота H2SO4
Серная кислота H2SO4 Хроматографія. Мікрогетерогенні дисперсні системи
Хроматографія. Мікрогетерогенні дисперсні системи Строение мицеллы лиофобного золя
Строение мицеллы лиофобного золя Генетическая связь между основными классами органических соединений
Генетическая связь между основными классами органических соединений Презентация по Химии "Фотосинтез" - скачать смотреть
Презентация по Химии "Фотосинтез" - скачать смотреть  Презентация по Химии "Ток в электролитах" - скачать смотреть
Презентация по Химии "Ток в электролитах" - скачать смотреть  Способы разделения смесей
Способы разделения смесей Презентация по Химии "Химические знаки и их история" - скачать смотреть
Презентация по Химии "Химические знаки и их история" - скачать смотреть  Диаграммы состояния сплавов. Диаграмма состояния Fe-C (Fe-Fe3C). Лекция №2
Диаграммы состояния сплавов. Диаграмма состояния Fe-C (Fe-Fe3C). Лекция №2 Обмен веществ. Метаболизм и его функции
Обмен веществ. Метаболизм и его функции Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации
Растворы неэлектролитов. Закон Вант- Гоффа и Рауля. Растворы электролитов. Теория электронной диссоциации Окислительно-восстановительные реакции в растворах
Окислительно-восстановительные реакции в растворах Переваривание и всасывание жиров
Переваривание и всасывание жиров Фосфор
Фосфор