Содержание
- 2. Вопросы для повторения Какими способами может быть получен этиловый спирт? Назовите условия промышленного процесса гидратации этилена
- 3. Задания Напишите структурные формулы пропанола-2, 2,2-диметилпропанола-1; На примере пропилового спирта охарактеризуйте химические свойства одноатомных спиртов. Напишите
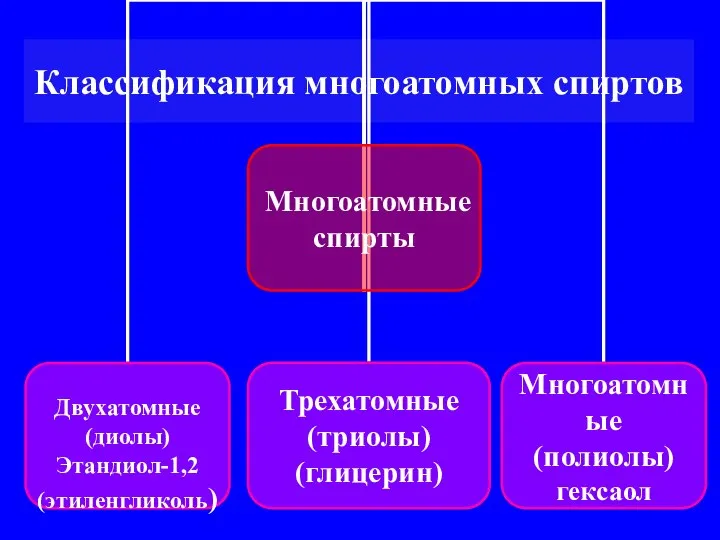
- 4. Классификация многоатомных спиртов
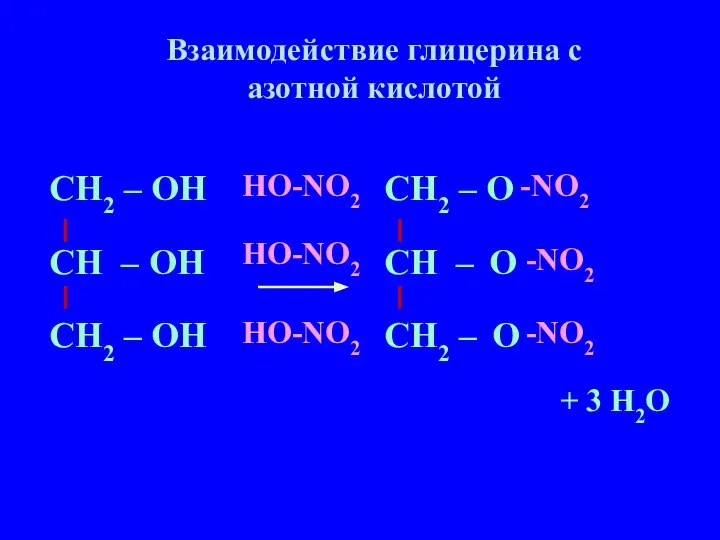
- 5. Структурные формулы Этандиол-1,2 (этиленгликоль) Пропантриол-1,2,3 (глицерин) СН2 – СН2 ОН ОН
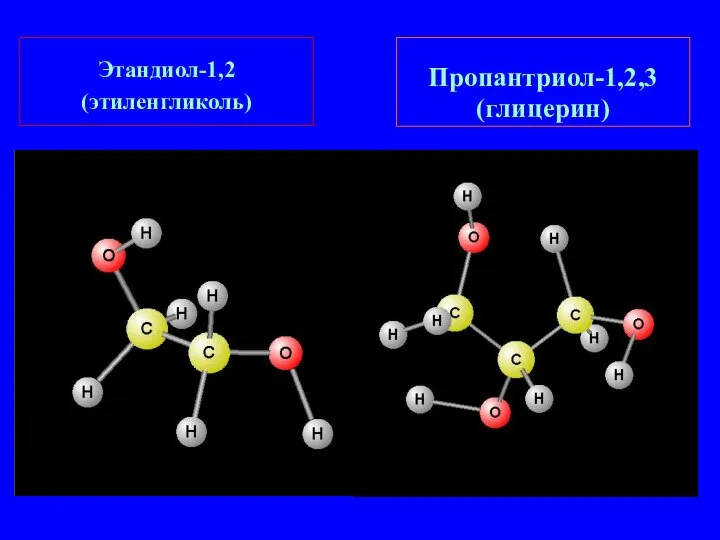
- 6. Этандиол-1,2 (этиленгликоль) Пропантриол-1,2,3 (глицерин)
- 7. Бесцветная, прозрачная, вязкая, сиропообразная жидкость, сладкая на вкус. не ядовит t кип= 2900 С Неограниченно растворим
- 8. Физические свойства этиленгликоля бесцветная вязкая жидкость со своеобразным запахом, сладкого вкуса ядовит t кип= 1980 С
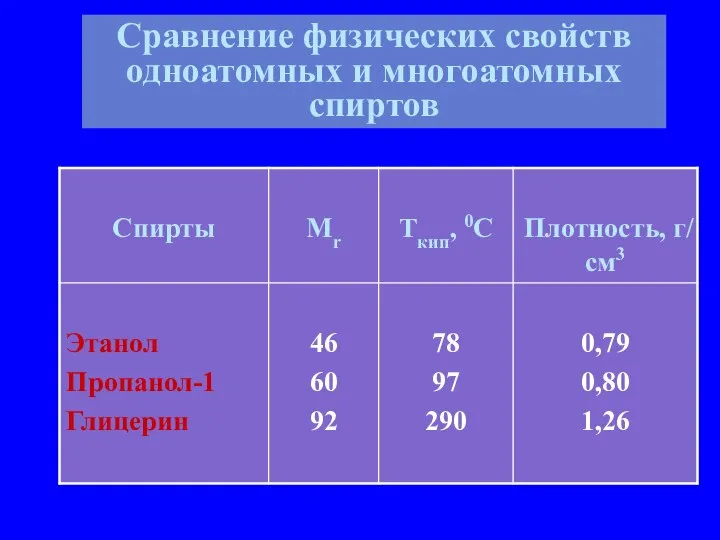
- 9. Сравнение физических свойств одноатомных и многоатомных спиртов
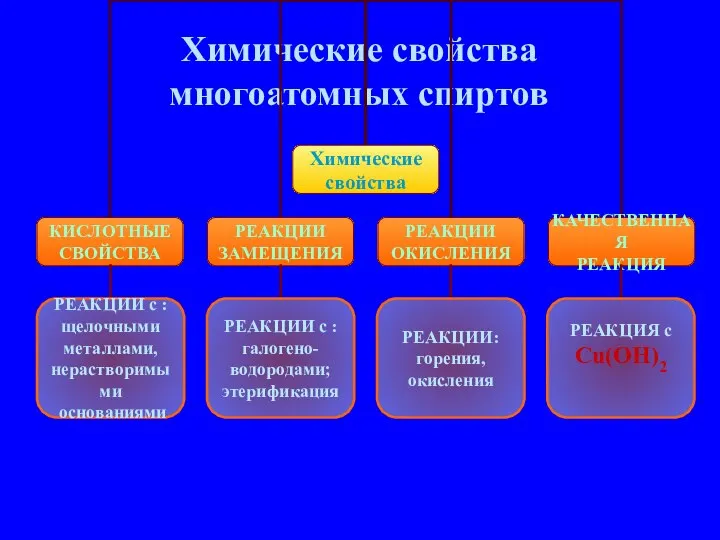
- 10. Химические свойства многоатомных спиртов РЕАКЦИИ с : щелочными металлами, нерастворимыми основаниями РЕАКЦИИ с : галогено- водородами;
- 11. СН – ОН СН2 – СН2 – ОН ОН СН – О СН2 – СН2 –
- 12. Задание Получите гидроксид меди (II), путем сливания растворов гидроксида натрия и сульфата меди (II). Прилейте полученный
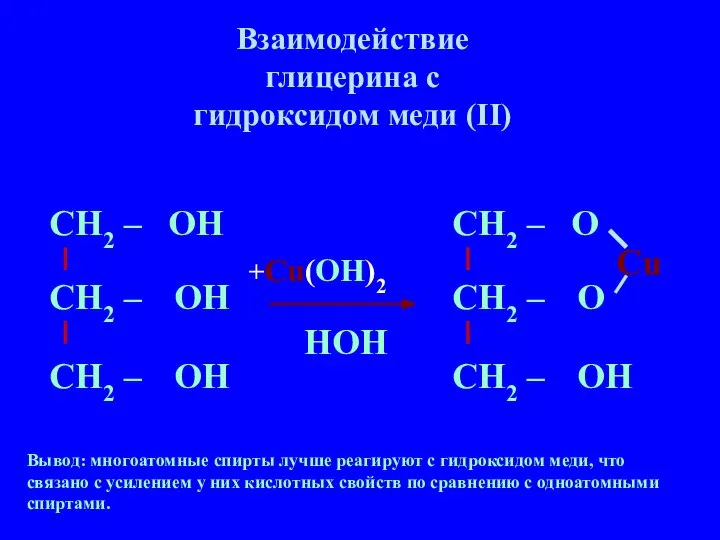
- 13. Взаимодействие глицерина с гидроксидом меди (II) Вывод: многоатомные спирты лучше реагируют с гидроксидом меди, что связано
- 14. Получение 3CH2=CH2 + 2KMnO4 + 4H2O → 3HO–CH2–CH2–OH + 2MnO2 + 2KOH Этиленгликоль (этандиол-1,2) синтезируют из
- 15. Применение этиленгликоля Антифризы – незамерзающие жидкости Пластиковые бутылки Синтетическое волокно лавсан
- 16. Применение глицерина Крема Мыло Помады Зубные пасты Кондитерские изделия Изделия из кожи Нитроглицерин Пластмассовые изделия
- 17. Применение многоатомных спиртов
- 18. Применение многоатомных спиртов
- 20. Скачать презентацию











 Исследовательская работа Химические средства в быту
Исследовательская работа Химические средства в быту Серосодержащие макрогетероциклы (тиакраун-соединения)
Серосодержащие макрогетероциклы (тиакраун-соединения) Углерод
Углерод ПРЕЗЕНТАЦИЯ ПО ХИМИИ НА ТЕМУ:”Химия вокруг нас “ Выполнила ученица 9 класса « Г» Ларченко Дарья
ПРЕЗЕНТАЦИЯ ПО ХИМИИ НА ТЕМУ:”Химия вокруг нас “ Выполнила ученица 9 класса « Г» Ларченко Дарья Биологически активные гетероциклические соединения. Нуклеиновые кислоты
Биологически активные гетероциклические соединения. Нуклеиновые кислоты Кислоты
Кислоты Лиофильные и лиофобные дисперсные системы
Лиофильные и лиофобные дисперсные системы Алюміній: будова атома, поширення в природі. Фізичні і хімічні властивості алюмінію. Застосування алюмінію Підготував
Алюміній: будова атома, поширення в природі. Фізичні і хімічні властивості алюмінію. Застосування алюмінію Підготував  Познавательная игра. Химия!
Познавательная игра. Химия! Атомна одиниця маси. Відносна атомна маса хімічних елементів.
Атомна одиниця маси. Відносна атомна маса хімічних елементів.  Виробництво цукру Підготував: Учень 9 класу Лаврук Ігор
Виробництво цукру Підготував: Учень 9 класу Лаврук Ігор  Сложные эфиры
Сложные эфиры Особенности строения твердых тел
Особенности строения твердых тел Системы эвтектического типа
Системы эвтектического типа Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины
Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины Кремний
Кремний Каменный уголь Работа: Заривной Виктории 11 – Л класс
Каменный уголь Работа: Заривной Виктории 11 – Л класс  Проверка знаний по теме «Химическая организация клетки. Неорганические вещества»
Проверка знаний по теме «Химическая организация клетки. Неорганические вещества» Кислоты
Кислоты Студент − это не сосуд, который надо наполнить, а факел, который надо зажечь Л. Арцимович
Студент − это не сосуд, который надо наполнить, а факел, который надо зажечь Л. Арцимович  Великие химики России
Великие химики России Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Карбоновые кислоты
Карбоновые кислоты Уреидтер және оның маңызы
Уреидтер және оның маңызы Чистые вещества и смеси. Способы разделения смесей. Загадка
Чистые вещества и смеси. Способы разделения смесей. Загадка Презентация Фенолы
Презентация Фенолы Презентация по Химии "d — элементы" - скачать смотреть
Презентация по Химии "d — элементы" - скачать смотреть  Работа студентки II курса Козловой Екатерины
Работа студентки II курса Козловой Екатерины