Содержание
- 2. Сорбция - гетерогенный процесс самопроизвольного поглощения твердым телом или жидкостью веществ из окружающей среды, приводящий к
- 3. Явление сорбции было открыто во второй половине XVIII в. Адсорбцию газов углем наблюдал в 1773 г.
- 4. Классификация сорбционных процессов: I. В зависимости от степени связывания поглощаемого вещества сорбентом сорбция может быть: обратимой
- 5. В качестве адсорбентов используют пористые твердые вещества: активированный уголь, силикагель, цеолиты, иониты, оксид алюминия. По диаметру
- 6. Капиллярная конденсация - сжижение пара в порах твердого сорбента, вследствие понижения давления пара над вогнутым мениском
- 7. Количественные характеристики адсорбционных процессов Абсолютная адсорбция (А) - это количество вещества сорбата в поверхностном слое адсорбента
- 8. Важнейшей характеристикой адсорбционного процесса является зависимость А (а,Г) от равновесной концентрации или давления при постоянной температуре,
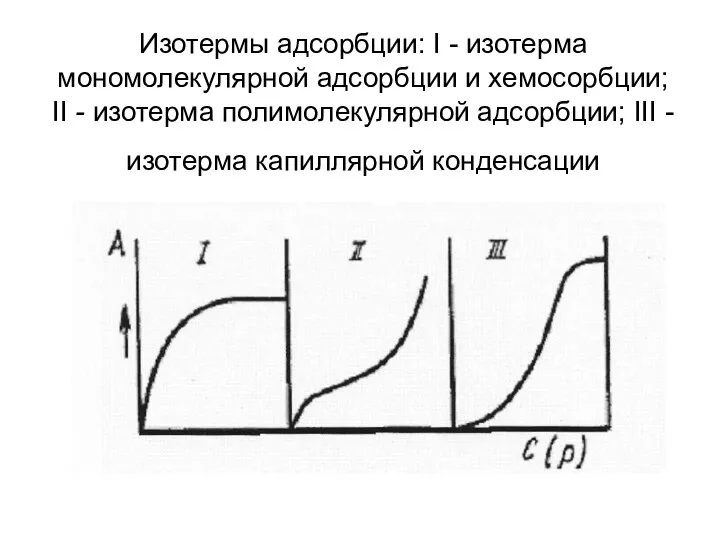
- 9. Изотермы адсорбции: I - изотерма мономолекулярной адсорбции и хемосорбции; II - изотерма полимолекулярной адсорбции; III -
- 10. Зависимость Г от концентрации и поверхностного натяжения была установлена Гиббсом (1876 г.) и названа уравнение избыточной
- 11. Из уравнения Гиббса ясно, что величина избыточной адсорбции зависит от поверхностной активности dσ/ dc если dσ/
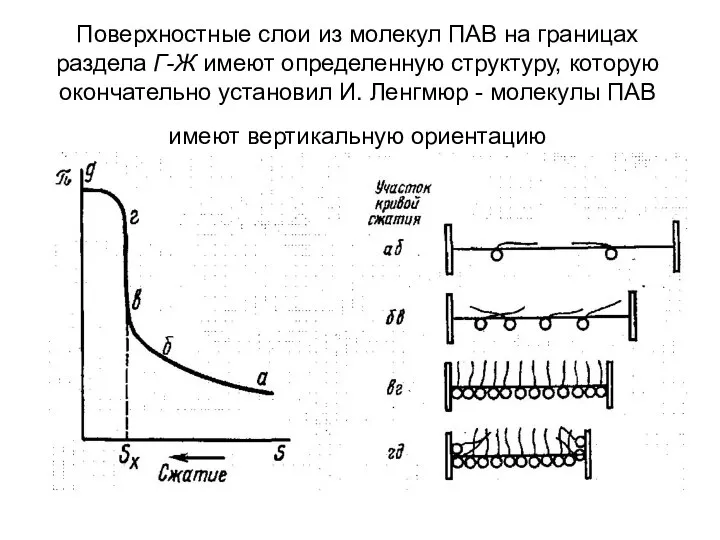
- 12. Поверхностные слои из молекул ПАВ на границах раздела Г-Ж имеют определенную структуру, которую окончательно установил И.
- 13. Для описания адсорбции на границе Т-Ж необходимо учитывать: Взаимодействие между молекулами растворенного вещества и растворителя; Сложное
- 14. Экспериментальное изучение адсорбции из растворов твердыми веществами: Определенные навески твердого адсорбента вносят в одинаковые объемы растворов
- 15. Величина удельной адсорбции для твердых сорбентов рассчитывается по формуле: а = х / m = (Со
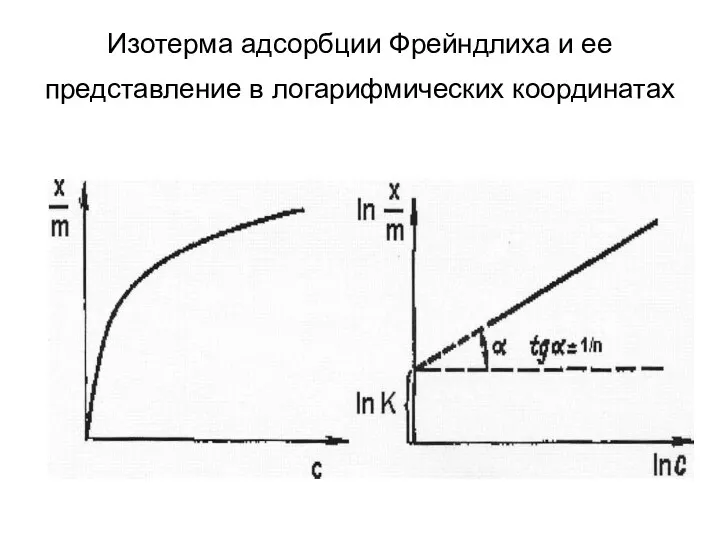
- 16. Изотерма адсорбции Фрейндлиха и ее представление в логарифмических координатах
- 17. Ход такой кривой для средних давлений или концентраций можно выразить эмпирическим уравнением Г. Фрейндлиха:
- 18. При логарифмировании уравнение Фрейндлиха переходит в линейную форму и изотерма имеет вид прямой
- 19. Линейная изотерма Фрейндлиха позволяет определить графически константы уравнения К и 1/n. Отрезок оси ординат, отсекаемый прямой,
- 20. В 1915 г Ленгмюр предложил теорию мономолекулярной адсорбции, которая справедлива для широкого интервала концентраций и для
- 21. Основные положения теории Ленгмюра: Адсорбционные силы подобны «валентным силам» действуют на малых расстояниях. Адсорбционной активностью обладает
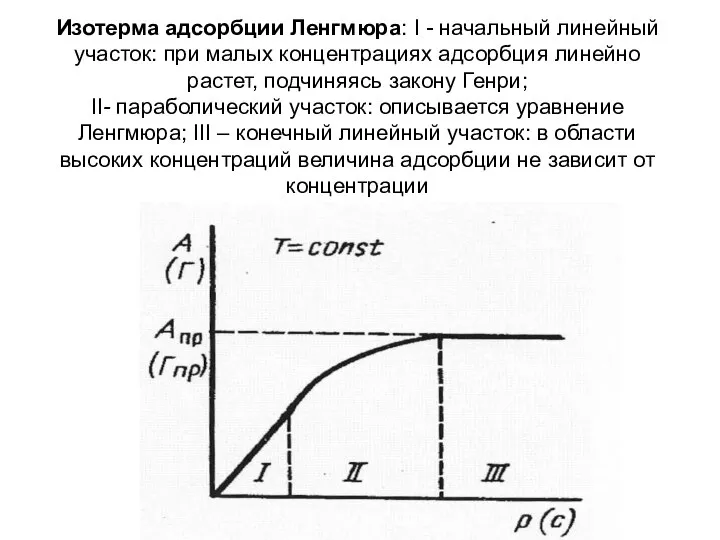
- 22. Изотерма адсорбции Ленгмюра: I - начальный линейный участок: при малых концентрациях адсорбция линейно растет, подчиняясь закону
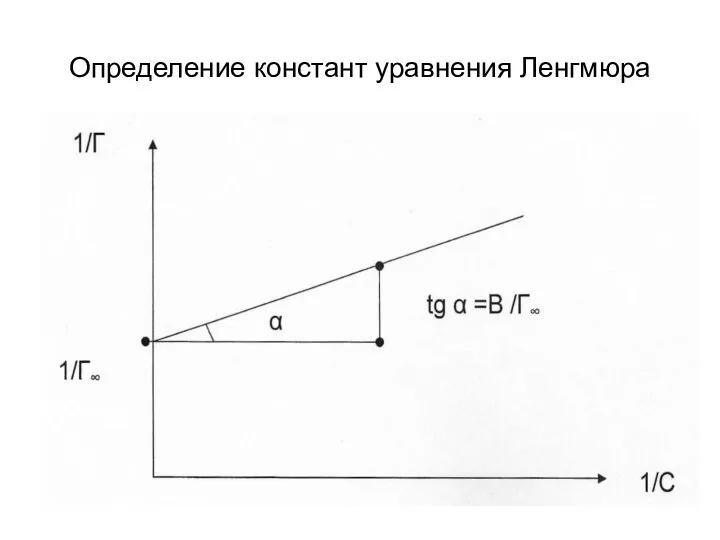
- 23. Уравнение Ленгмюра: Для определения констант необходимо привести уравнение к линейному виду где В – константа численно
- 24. Определение констант уравнения Ленгмюра
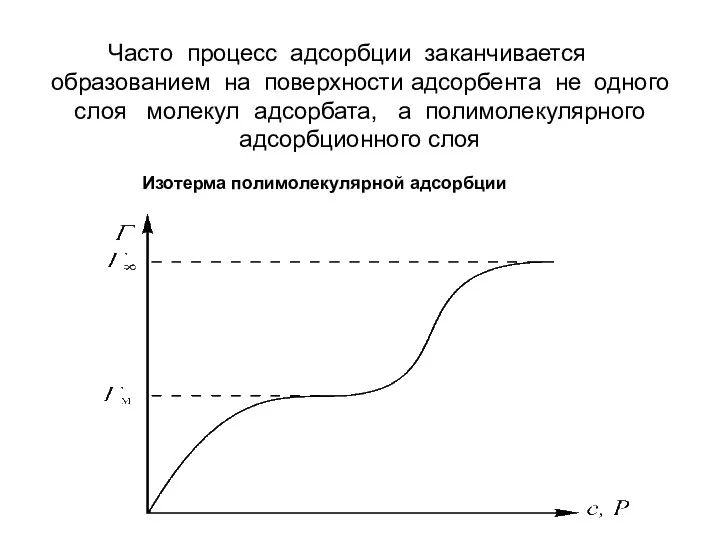
- 25. Часто процесс адсорбции заканчивается образованием на поверхности адсорбента не одного слоя молекул адсорбата, а полимолекулярного адсорбционного
- 26. Теория полимолекулярной адсорбции Поляни (1915 г.). Адсорбция обуславливается чисто физическими силами. На поверхности твердых адсорбентов нет
- 27. Теория Поляни не дала математического выражения изотермы адсорбции, однако ее представления положены в основу современной теории
- 28. Основные положения теории БЭТ: 1. На поверхности адсорбента имеется определенное число равноценных в энергетическом отношении активных
- 29. Авторы теории на основе уравнения изотермы адсорбции Ленгмюра получили приближенное уравнение полимолекулярной адсорбции - давление насыщенного
- 30. На теории БЭТ основан стандартный метод измерения удельной поверхности адсорбентов, катализаторов, порошков. Для этого используют уравнение
- 32. Скачать презентацию























 Глюконеогенез. Суммарное уравнение реакций глюконеогенеза
Глюконеогенез. Суммарное уравнение реакций глюконеогенеза Номенклатура алканов
Номенклатура алканов Углерод и его соединения Лекция.(§29 -30, с.172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода?
Углерод и его соединения Лекция.(§29 -30, с.172 -178). Цель: Какие соединения образует углерод? Какие свойства, связанные со строением атома углерода, характерны для углерода и его соединений? Где находят применение соединения углерода? Хлороформ. Методы его изолирования и обнаружения
Хлороформ. Методы его изолирования и обнаружения Автомобильные трансмиссионные масла
Автомобильные трансмиссионные масла Особенности химического состава клетки
Особенности химического состава клетки . Урок в 7 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна
. Урок в 7 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна  Презентация по Химии "Харчові добавки" - скачать смотреть бесплатно
Презентация по Химии "Харчові добавки" - скачать смотреть бесплатно Будова атома
Будова атома Обобщение
Обобщение Азотная кислота и её соли Автор: учитель химии и биологии МОУ СОШ №3 города Волгореченска Костромской области Звёздочкина С.А.
Азотная кислота и её соли Автор: учитель химии и биологии МОУ СОШ №3 города Волгореченска Костромской области Звёздочкина С.А.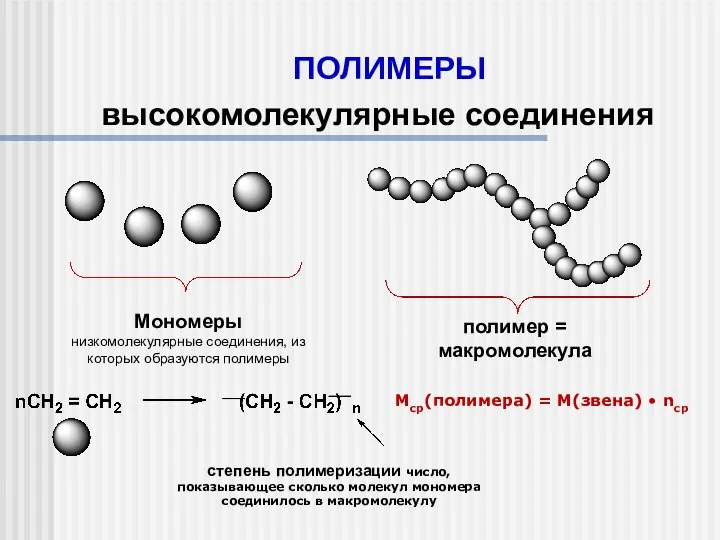 Полимеры. Высокомолекулярные соединения
Полимеры. Высокомолекулярные соединения Презентация по Химии "Инертные газы" - скачать смотреть
Презентация по Химии "Инертные газы" - скачать смотреть  Буферные растворы. (Лекция 5)
Буферные растворы. (Лекция 5) Основания и их свойства
Основания и их свойства Кремний. Химические свойства
Кремний. Химические свойства Почему протекают химические реакции Учитель химии ГОУ средняя общеобразовательная школа №10 с углубленным изучением химии
Почему протекают химические реакции Учитель химии ГОУ средняя общеобразовательная школа №10 с углубленным изучением химии  Презентация по Химии "Галогены и их соединения" - скачать смотреть
Презентация по Химии "Галогены и их соединения" - скачать смотреть  Формирование и развитие системы знаний о химической реакции
Формирование и развитие системы знаний о химической реакции Масла автомобильные
Масла автомобильные Презентация по Химии "Свойства неньютоновских жидкостей" - скачать смотреть
Презентация по Химии "Свойства неньютоновских жидкостей" - скачать смотреть  Буферные системы
Буферные системы Углеводы
Углеводы Химия - моя жизнь
Химия - моя жизнь Репликация ДНК
Репликация ДНК Степень окисления
Степень окисления Растворы
Растворы Особенности ионообменных реакций с участием биологически активных веществ. Ионообменная сорбция пептидов и белков
Особенности ионообменных реакций с участием биологически активных веществ. Ионообменная сорбция пептидов и белков