Содержание
- 2. Алкены Алкены – это ненасыщенные углеводороды общей формулы СnH2n, имеющие в своем составе одну двойную связь.
- 3. Способы получения алкенов Дегидрирование предельных углеводородов Дегалогенирование дигалогеналканов
- 4. Способы получения алкенов Дегалогенирование галогеналканов Дегидратация спиртов Правило Зайцева: при отщеплении от органического соединения молекулы типа
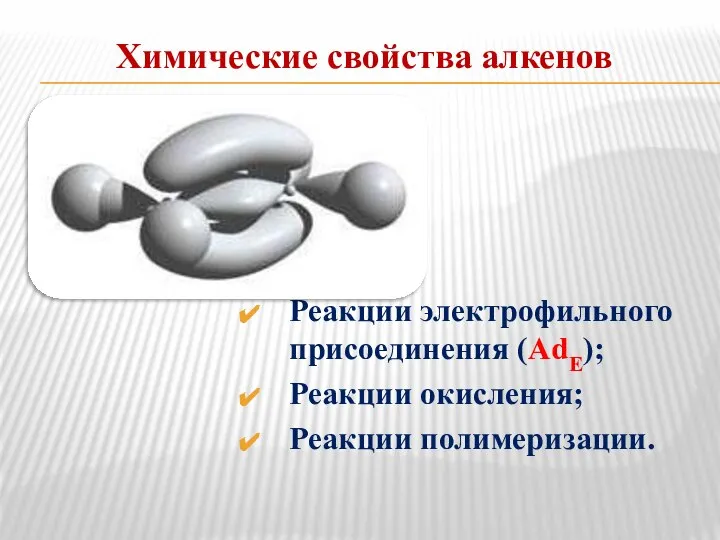
- 5. Химические свойства алкенов Реакции электрофильного присоединения (AdE); Реакции окисления; Реакции полимеризации.
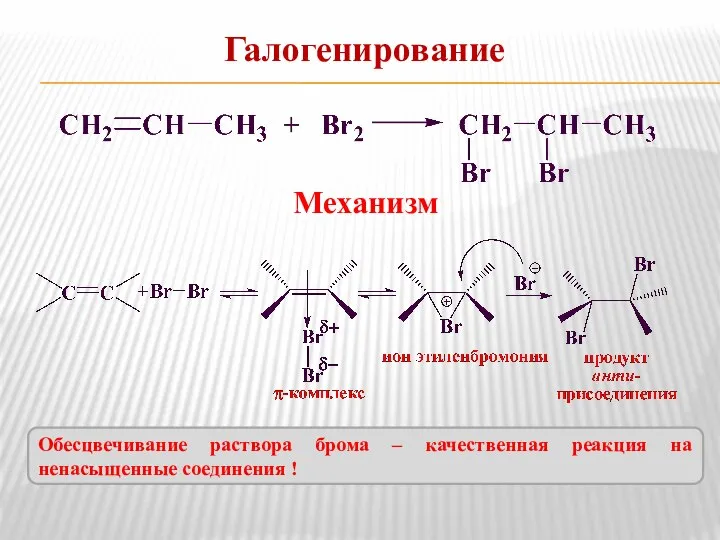
- 6. Галогенирование Механизм Обесцвечивание раствора брома – качественная реакция на ненасыщенные соединения !
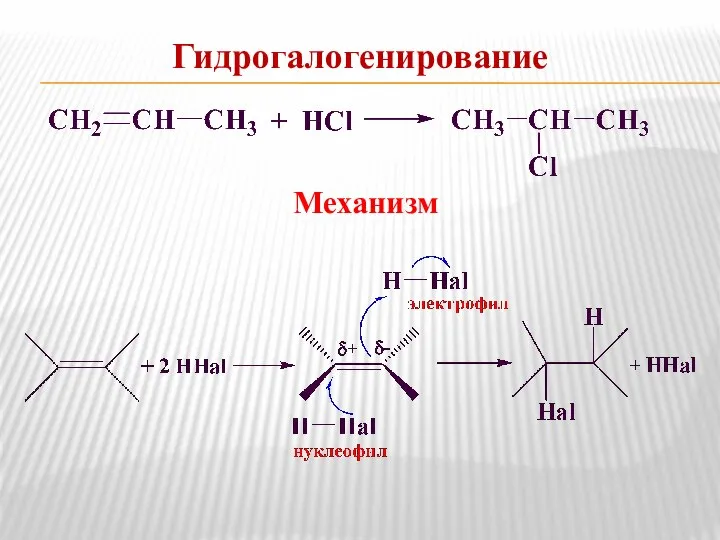
- 7. Гидрогалогенирование Механизм
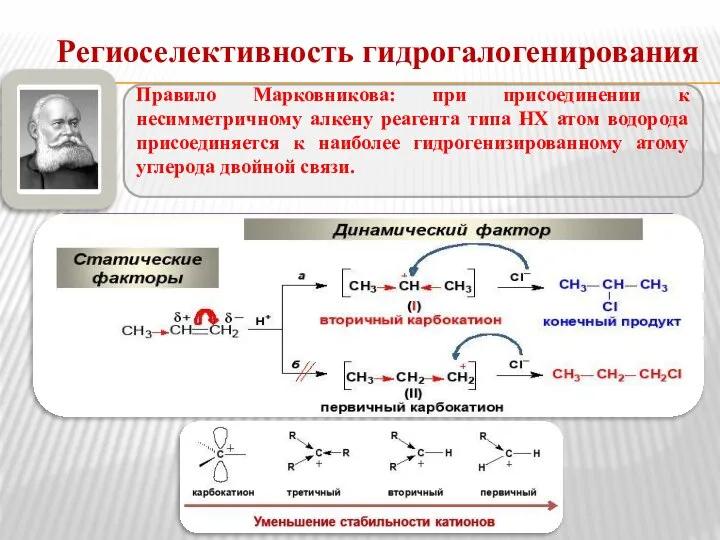
- 8. Региоселективность гидрогалогенирования Правило Марковникова: при присоединении к несимметричному алкену реагента типа НХ атом водорода присоединяется к
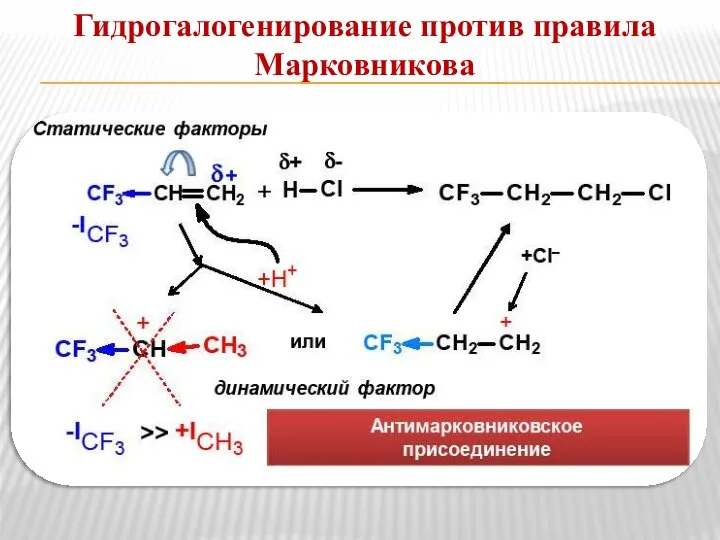
- 9. Гидрогалогенирование против правила Марковникова
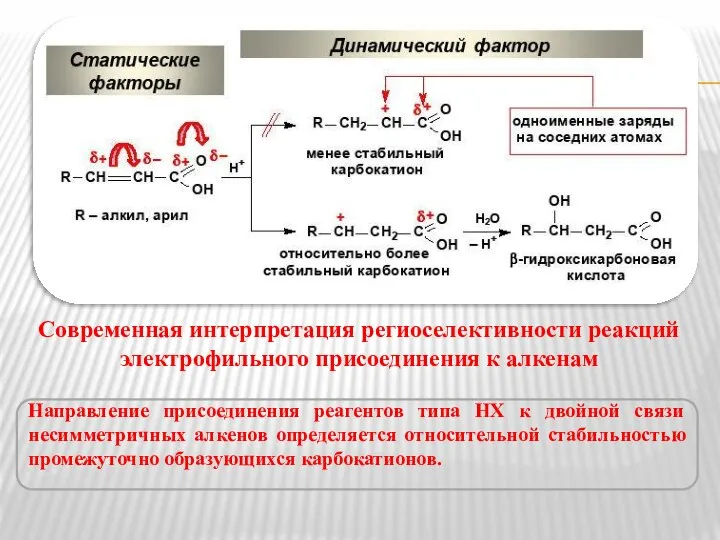
- 10. Современная интерпретация региоселективности реакций электрофильного присоединения к алкенам Направление присоединения реагентов типа НХ к двойной связи
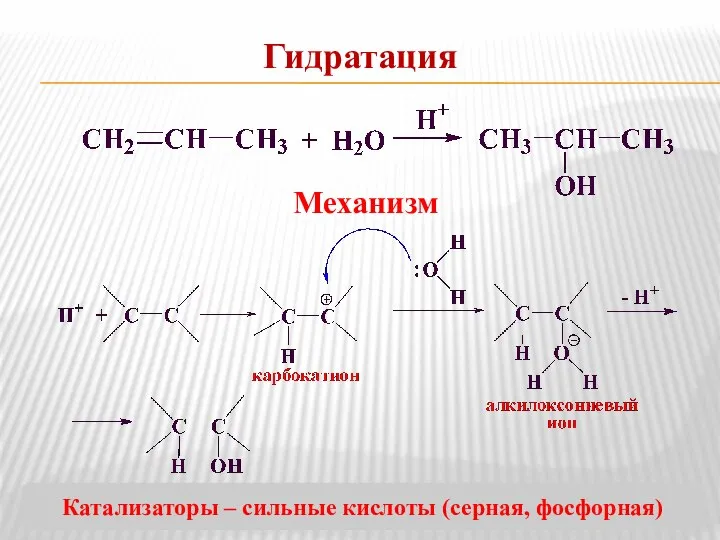
- 11. Гидратация Механизм Катализаторы – сильные кислоты (серная, фосфорная)
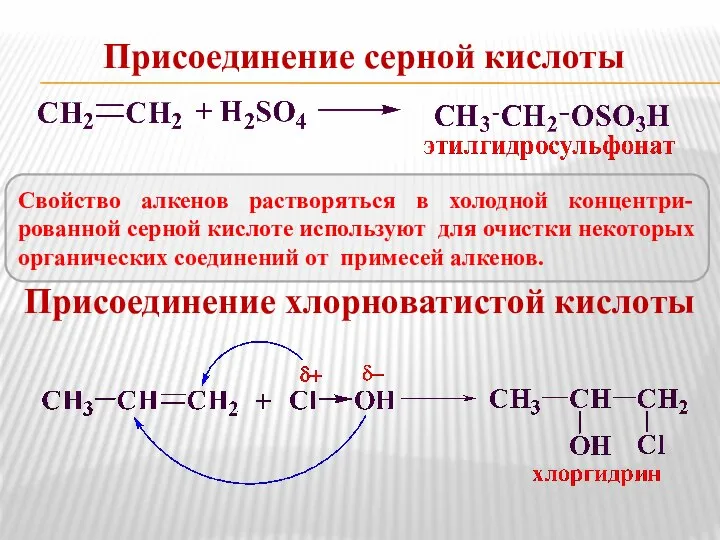
- 12. Присоединение серной кислоты Присоединение хлорноватистой кислоты Свойство алкенов растворяться в холодной концентри-рованной серной кислоте используют для
- 13. Сравнительная оценка реакционной способности алкенов в AdE-реакциях Чем больше электронная плотность между атомами углерода, образующими двойную
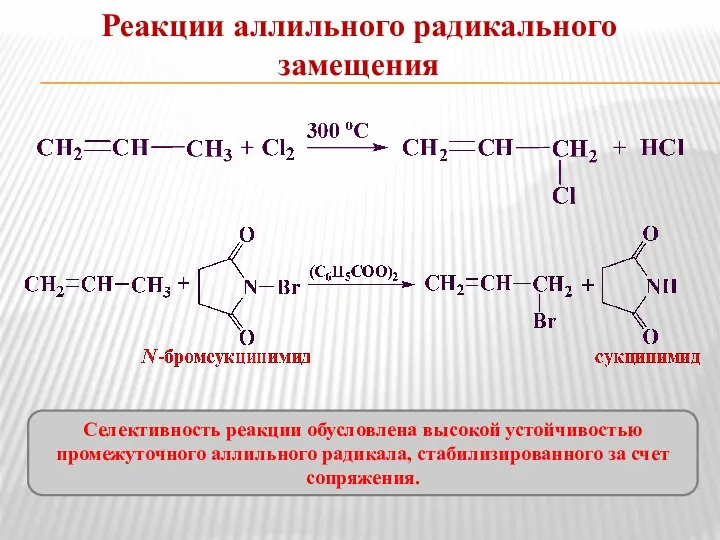
- 14. Реакции аллильного радикального замещения Селективность реакции обусловлена высокой устойчивостью промежуточного аллильного радикала, стабилизированного за счет сопряжения.
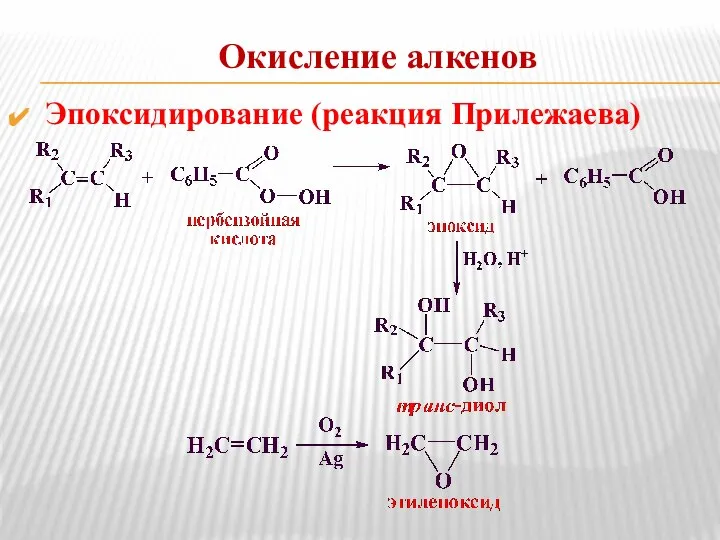
- 15. Окисление алкенов Эпоксидирование (реакция Прилежаева)
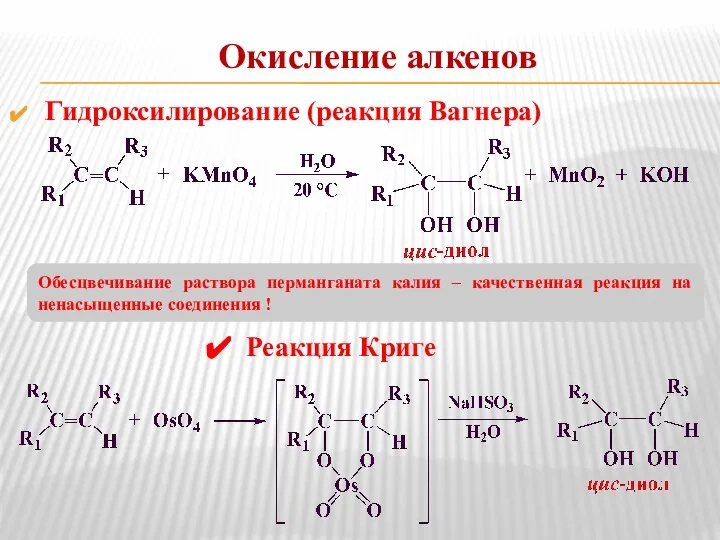
- 16. Окисление алкенов Гидроксилирование (реакция Вагнера) Обесцвечивание раствора перманганата калия – качественная реакция на ненасыщенные соединения !
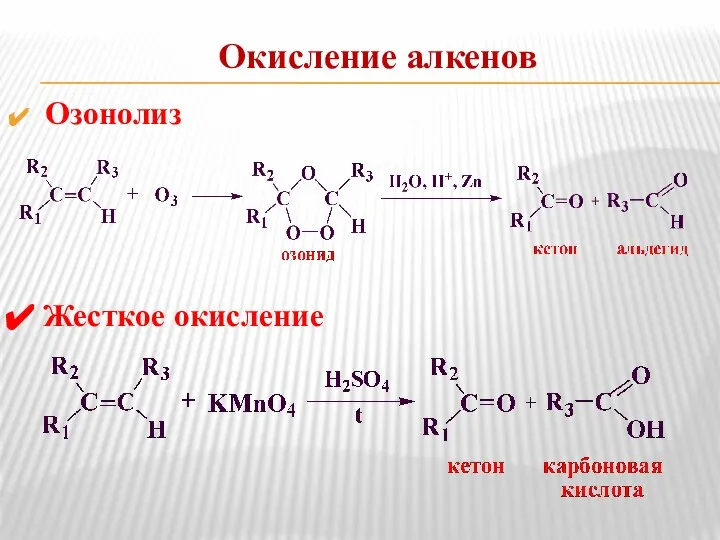
- 17. Окисление алкенов Озонолиз Жесткое окисление
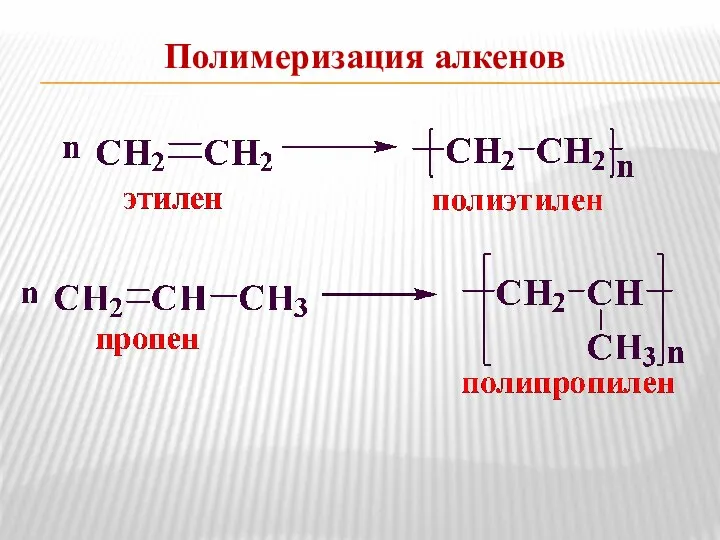
- 18. Полимеризация алкенов
- 19. Алкадиены Алкадиены – это ненасыщенные углеводоро-ды общей формулы СnH2n-2, имеющие в своем составе две двойные связи.
- 20. Способы получения алкадиенов Реакции элиминирования (дегидрогалогенирование, дегидратация) Реакция Лебедева (получение бутадиена-1,3)
- 21. Химические свойства алкадиенов Сопряженные алкадиены более реакционноспособны в реакциях электрофильного присоединения. Эти реакции имеют некоторые особенности.
- 22. Реакции электрофильного присоединения Соотношение продуктов 1,2- и 1,4-присоединения определяется температурой реакции. При низких температурах (ниже 0оС)
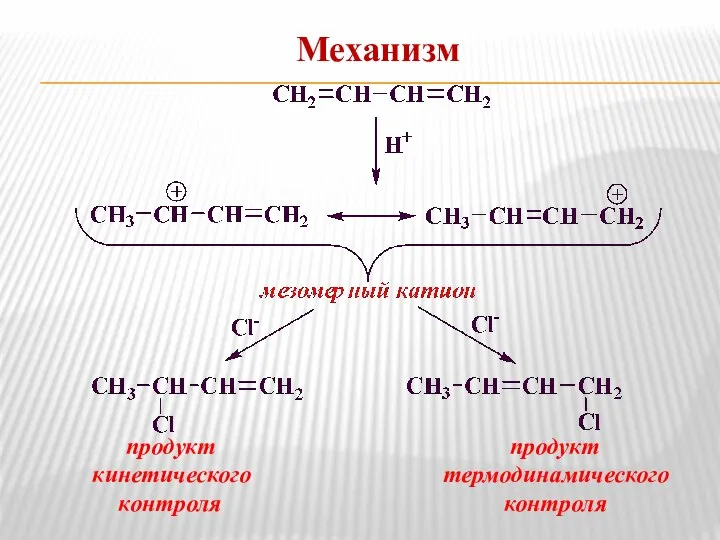
- 23. Механизм продукт продукт кинетического термодинамического контроля контроля
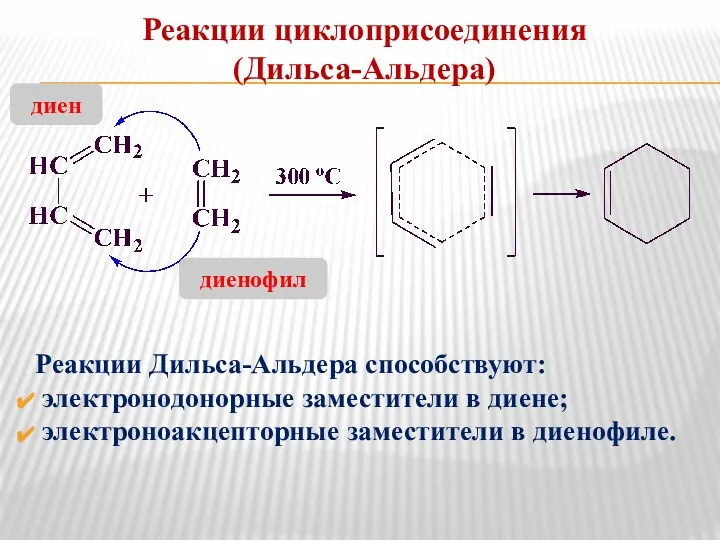
- 24. Реакции циклоприсоединения (Дильса-Альдера) Реакции Дильса-Альдера способствуют: электронодонорные заместители в диене; электроноакцепторные заместители в диенофиле. диен диенофил
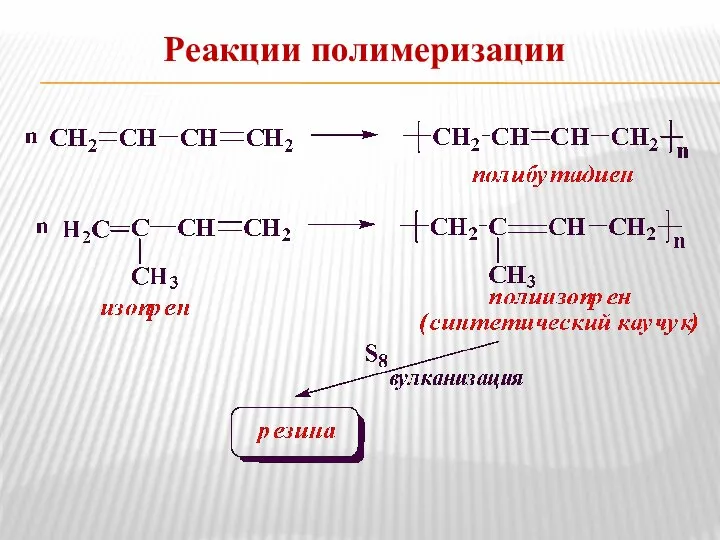
- 25. Реакции полимеризации
- 26. Алкины Алкины – это ненасыщенные углеводороды общей формулы СnH2n-2, имеющие в своем составе одну тройную связь.
- 27. Способы получения алкинов Гидролиз карбида кальция (получение ацетилена) Пиролиз метана (получение ацетилена) Дегидрогалогенирование дигалогеналканов
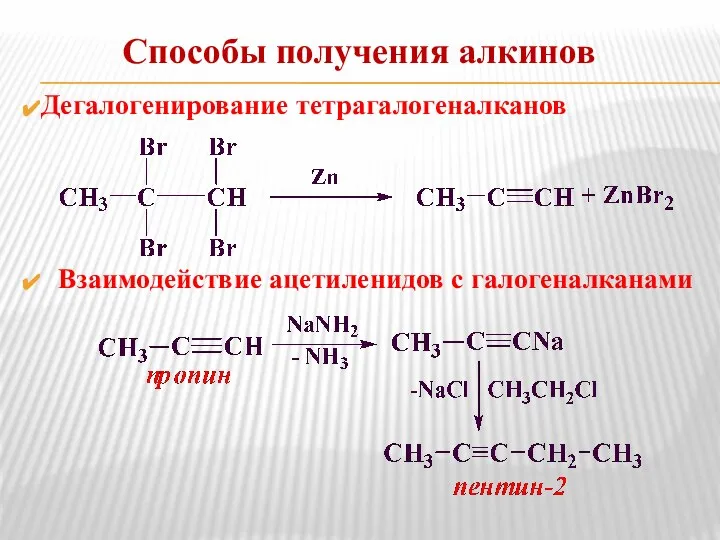
- 28. Способы получения алкинов Дегалогенирование тетрагалогеналканов Взаимодействие ацетиленидов с галогеналканами
- 29. Химические свойства алкинов Реакции электрофильного присоединения (AdE); Реакции замещения (для терминальных алкинов); Реакции окисления и восстановления.
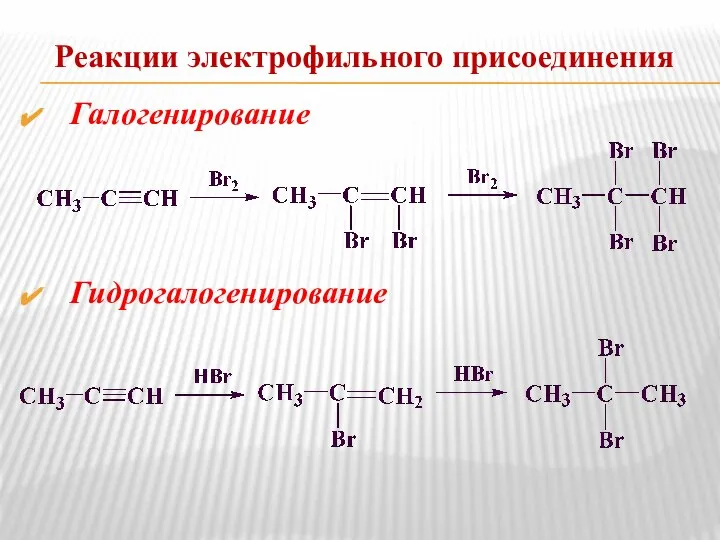
- 30. Реакции электрофильного присоединения Галогенирование Гидрогалогенирование
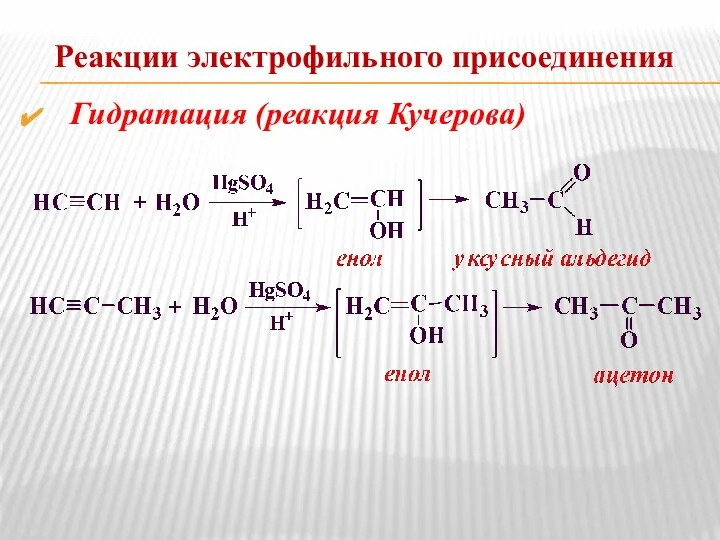
- 31. Реакции электрофильного присоединения Гидратация (реакция Кучерова)
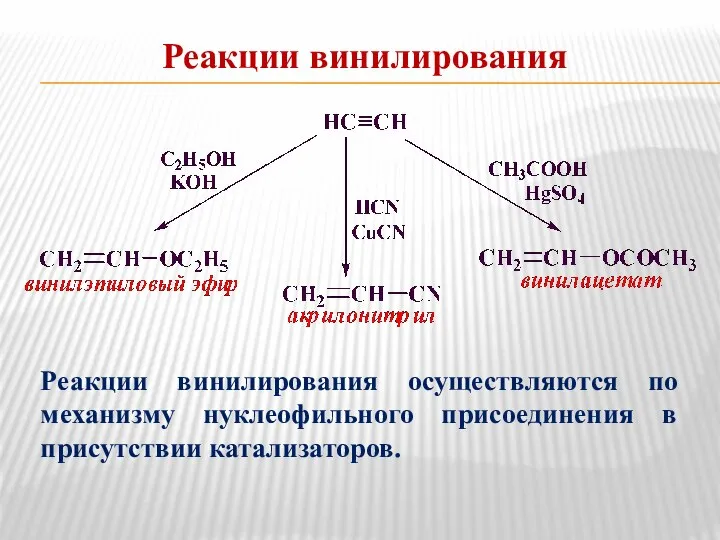
- 32. Реакции винилирования Реакции винилирования осуществляются по механизму нуклеофильного присоединения в присутствии катализаторов.
- 33. Реакции замещения Терминальные алкины обладают слабыми кислотными свойствами Реакции с комплексными соединениями серебра и меди (I)
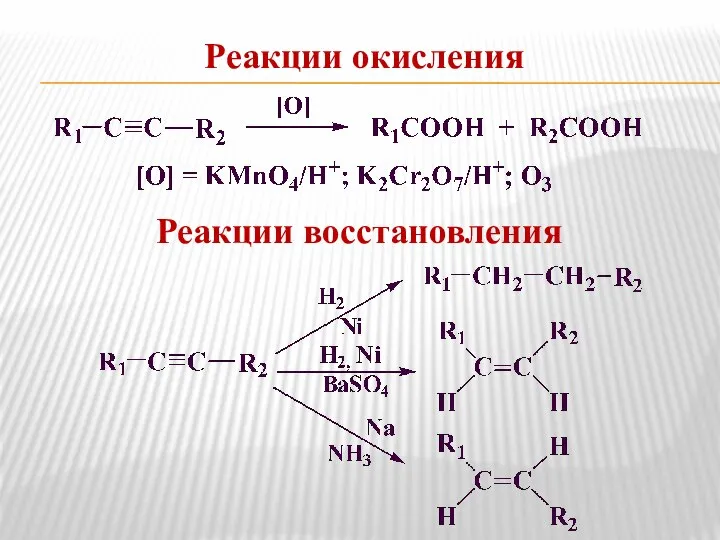
- 34. Реакции окисления Реакции восстановления
- 36. Скачать презентацию












 Аккредитованная образовательная программа бакалавриата Химия
Аккредитованная образовательная программа бакалавриата Химия Термодинамика химического равновесия
Термодинамика химического равновесия Основні класи неорганічних речовин
Основні класи неорганічних речовин Элементы третьего периода, периодической системы Д. И. Менделеева
Элементы третьего периода, периодической системы Д. И. Менделеева Проектная деятельность школьников в процессе обучения химии
Проектная деятельность школьников в процессе обучения химии Анализ пищевых добавок (маркировка Е) используемых в продуктовой линейке Витамакс
Анализ пищевых добавок (маркировка Е) используемых в продуктовой линейке Витамакс Химия ғажайыптары
Химия ғажайыптары Электрические свойства дисперсных систем. (Лекция 5)
Электрические свойства дисперсных систем. (Лекция 5) Ассортимент и свойства тканей из синтетических волокон (9 класс)
Ассортимент и свойства тканей из синтетических волокон (9 класс) Ionization Energy
Ionization Energy Особенности формирования естественно-научной картины мира на уроках географии и химии
Особенности формирования естественно-научной картины мира на уроках географии и химии Щелочной металл натрий
Щелочной металл натрий Кремний. Получение кремния. Свойства кремния
Кремний. Получение кремния. Свойства кремния Аттестационная работа. Влияние внеклассного мероприятия Неделя химии в школе на познавательную активность учащихся
Аттестационная работа. Влияние внеклассного мероприятия Неделя химии в школе на познавательную активность учащихся Ковалентная связь
Ковалентная связь Кремень. Нахождение в природе
Кремень. Нахождение в природе Химический состав клетки
Химический состав клетки Новые стеклообразные материалы и методы их синтеза. Аморфные и стеклообразные материалы
Новые стеклообразные материалы и методы их синтеза. Аморфные и стеклообразные материалы Классификация дисперсных систем. (Лекция 5)
Классификация дисперсных систем. (Лекция 5) Закономерности изменения свойств химических элементов в Периодической Системе Химических Элементов ( ПСХЭ)
Закономерности изменения свойств химических элементов в Периодической Системе Химических Элементов ( ПСХЭ) Углеводы (сахариды)
Углеводы (сахариды) Силикаты. Породообразующие минералы
Силикаты. Породообразующие минералы Простейшие операции с веществом
Простейшие операции с веществом Презентация по Химии "«Нитраты - минеральные удобрения»" - скачать смотреть
Презентация по Химии "«Нитраты - минеральные удобрения»" - скачать смотреть  Гигиена труда при работе с пестицидами и минеральными удобрениями
Гигиена труда при работе с пестицидами и минеральными удобрениями Важнейшие классы бинарных соединений – оксиды и водородные соединения
Важнейшие классы бинарных соединений – оксиды и водородные соединения Курсовая работа: синтез 3,5-диметилпиразола
Курсовая работа: синтез 3,5-диметилпиразола Подача питательной воды в парогенератор при запроектной аварии
Подача питательной воды в парогенератор при запроектной аварии