Содержание
- 2. Лекция №1 Введение.
- 3. ВВЕДЕНИЕ ЦЕЛИ КУРСА создать основу для дальнейшего изучения химических дисциплин, сформировать элементарные навыки работы в химической
- 4. План лекции: История химии. Роль отечественных и зарубежных ученых в развитии химии. Предмет и задачи химии.
- 5. Происхождение термина “химия” Есть несколько версий: от египетского слова "Хем" - арабского названия этой страны -
- 6. Периодизация истории химии Выделялют 2 основных основных периода: а) эмпирический (с древности до XVIIIв); процесс познания
- 7. Основные периоды в истории химии 1. Период алхимии - с древности до XVI в. нашей эры.
- 8. Античная атомистика V-IV в до н.э. Основателями первой древнегреческой атомистической теориеи считают Левкиппа и Демокрита. В
- 9. АЛХИМИЯ ЗАПАДНОЙ ЕВРОПЫ XVI в Оборудование алхимической лаборатории. Рисунки из книги А. Либавия «Алхимия». Франкфурт. 1606
- 10. Роберт Бойль Он положили начало рождению новой химической науки, отдельной от медицины. Систематизируя многочисленные цветные реакции
- 11. К концу XVIII в. в химии был накоплен большой объем экспериментальных данных, которые необходимо было систематизировать
- 12. Период научной химии XIX—XX вв За открытым Лавуазье законом сохранения массы последовал целый ряд новых количественных
- 13. М. В. ЛОМОНОСОВ - ОСНОВОПОЛОЖНИК НАУЧНОЙ ХИМИИ В РОССИИ М.В. Ломоносов - создатель школы российских химиков.
- 14. Й. Я. БЕРЦЕЛИУС вычислил относительные атомные массы всех известных к тому времени элементов (45). Берцелиус ввел
- 15. МОЛЕКУЛЯРНАЯ ТЕОРИЯ АВОГАДРО В 1814 г. итальянский физик и химик А. Авогадро сформулировал закон, который носит
- 16. МЕЖДУНАРОДНЫЙ СЪЕЗД ХИМИКОВ В КАРЛСРУЭ. РЕФОРМА АТОМНО-МОЛЕКУЛЯРНОЙ ТЕОРИИ В середине XIX в. у различных школ и
- 17. На рубеже XVIII - XIX вв. в России существовал по сути лишь единственный Московский университет. В
- 18. КАЗАНСКАЯ ХИМИЧЕСКАЯ ШКОЛА Н.Н. Зинин – химик-органик. Открыл метод получения ароматических аминов (реакция Зинина). Впервые синтезировал
- 19. Герман Иванович Гесс Герман Иванович Гесс занимался разработаткой русской химической номенклатуры. Которая затем была дополнена Д.И.
- 20. Дмитрий Иванович Менделеев Менделеев оставил свыше 500 печатных трудов, среди которых классические «Основы химии» — первое
- 21. Итак , какие же основные понятия и законы химии мы имеем на сегодняшний день благодаря замечательным
- 22. Основные понятия и законы химии.
- 23. Химия – это наука о составе, строении, свойствах и превращениях веществ. Вещество – один из видов
- 24. Задачи химии. Изучение веществ, их физических и химических свойств Изучение превращений веществ и процессов, сопровождающих эти
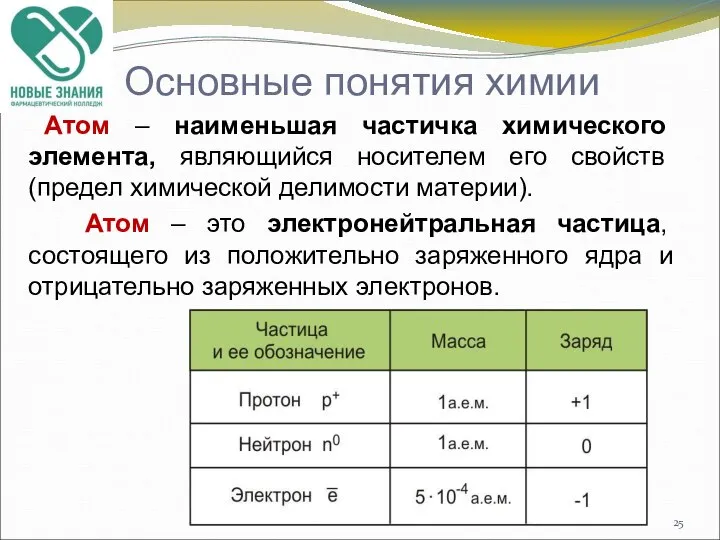
- 25. Основные понятия химии Атом – наименьшая частичка химического элемента, являющийся носителем его свойств (предел химической делимости
- 26. Химический элемент – это совокупность атомов с одинаковым зарядом ядра. Объектом изучения в химии являются химические
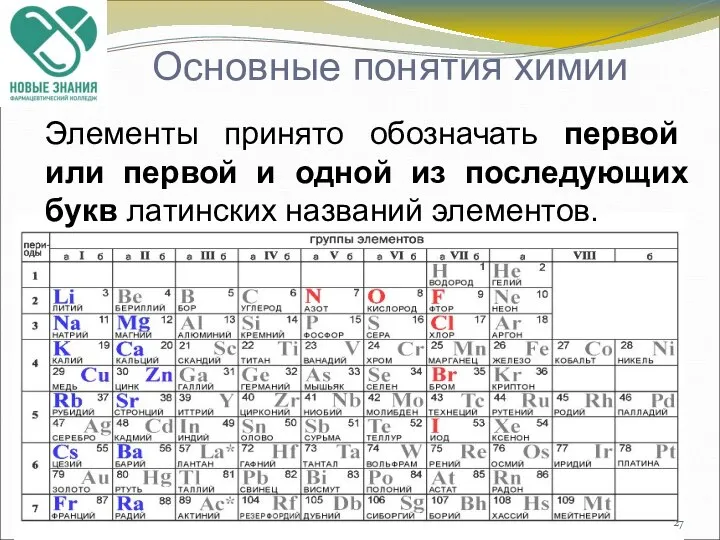
- 27. Основные понятия химии Элементы принято обозначать первой или первой и одной из последующих букв латинских названий
- 28. Химический знак (символ) – обозначает название элемента, один его атом, один моль атомов этого элемента. По
- 29. Основные понятия химии Химические элементы существуют в виде простых веществ, состоящих из атомов одного химического элемента
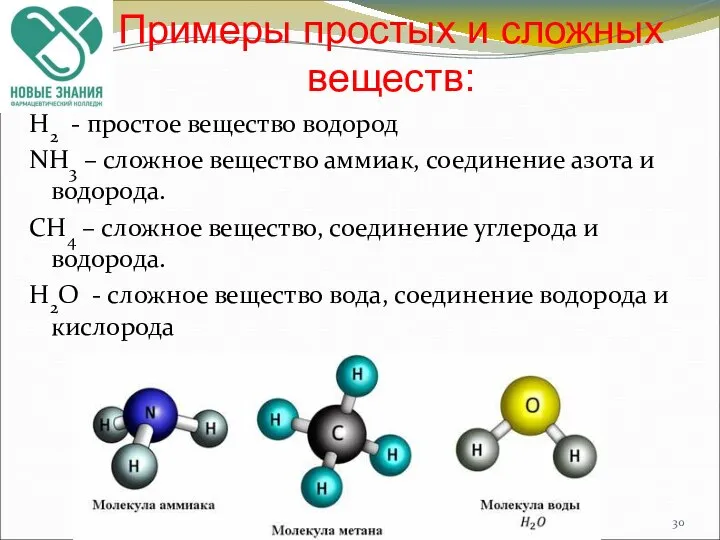
- 30. Примеры простых и сложных веществ: Н2 - простое вещество водород NH3 – сложное вещество аммиак, соединение
- 31. Аллотропия – способность химического элемента образовывать несколько простых веществ, называемых аллотропными модификациями Основные понятия химии
- 32. Аллотропные модификации углерода (С): алмаз, графит, фуллерен, графен, нанотрубки Основные понятия химии
- 33. Аллотропия Аллотропные модификации фосфора Р: белый (желтый), красный и черный
- 34. Основные понятия химии Молекула – это электронейтральная частица, образующаяся при возникновении ковалентных связей между атомами одного
- 35. Химическая формула - это условная запись качественного и количественного состава вещества при помощи химических знаков и
- 36. Широко используются несколько видов химических формул: Простейшая (эмпирическая) формула показывает качественный состав и соотношения, в которых
- 37. Что обозначают записи? H2- это одна молекула водорода, в её состав входят два атома водорода. 5O2
- 38. Масса атомов, молекул и ионов очень мала, 10-24 – 10-23 г Например, масса атома водорода m(H)
- 39. Атомная единица массы (а.е.м.) - внесистемная единица массы. Атомная единица массы – это единица массы, равная
- 40. Относительная атомная масса элемента Ar Относительная атомная масса элемента показывает во сколько раз масса его атома
- 41. Атомные массы элементов приведены в периодической системе элементов.
- 42. Найдите в ПСХЭ Д.И. Менделеева Относительную атомную массу элемента Ar Водорода Натрия Алюминия Кислорода Серы Хлора
- 43. Масса молекулы Относительная молекулярная масса Мr (молекулярная масса) Мr равна сумме относительных атомных масс всех атомов,
- 44. Количество вещества В Международной системе СИ за единицу количества вещества принят моль. МОЛЬ - это количество
- 45. В задачах : Р2O5 + 3H2O = 2H3РO4 1 моль 3 моль 2 моль
- 46. Основные понятия химии Постоянная Авогадро ( ) – число атомов или молекул (или других структурных единиц),
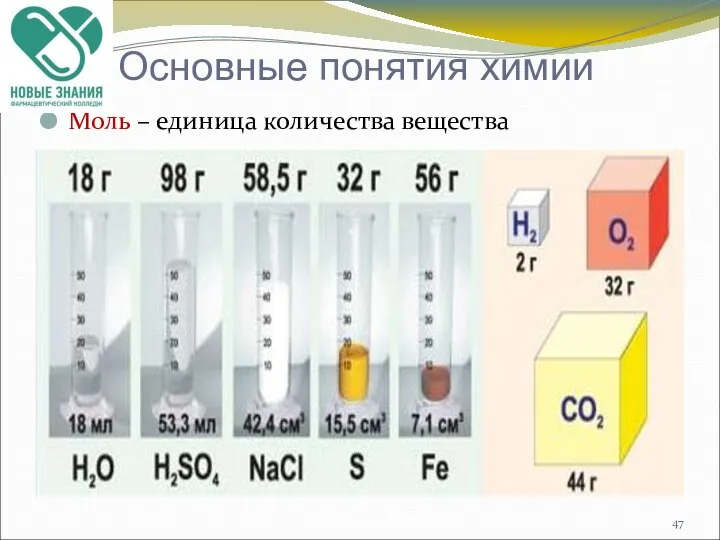
- 47. Моль – единица количества вещества Основные понятия химии
- 48. Молярная масса (М) – масса 1 моля вещества в граммах [М] = [г/моль] Молярная масса численно
- 49. Рассчитайте относительную молекулярную массу для следующих соединений: CaO, CO2, Н2SO4 56 г/моль 44 г/моль 98 г/моль
- 50. Основные законы химии Закон сохранения массы. Масса веществ, вступивших в реакцию, равна массе веществ, образовавшихся в
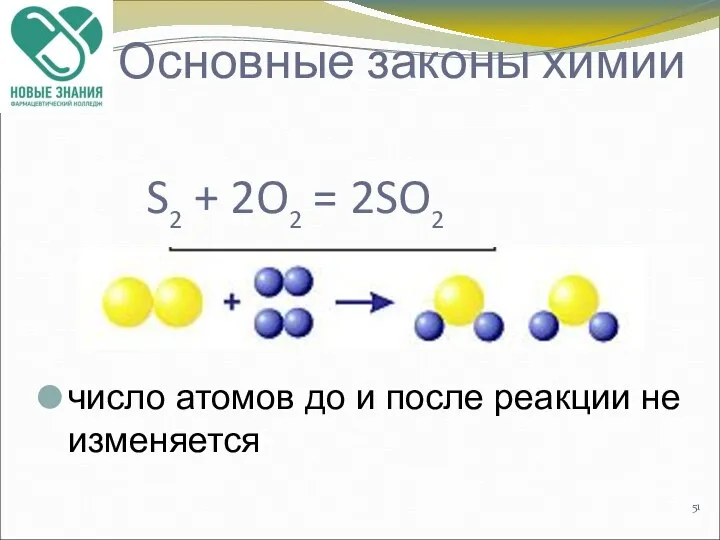
- 51. S2 + 2O2 = 2SO2 число атомов до и после реакции не изменяется Основные законы химии
- 52. Основные законы химии Закон объемных отношений Объемы газов, вступающих в химическую реакцию, и объемы газов, образующихся
- 53. Основные законы химии Закон объемных отношений Следствие. Стехиометрические коэффициенты в уравнениях химических реакций для газообразных веществ
- 54. Закон постоянства состава вещества. Сформулирован Ж.-Л. Прустом в 1799 г.. Всякое чистое вещество независимо от способа
- 55. Современная формулировка закона постоянства состава вещества таков: Состав соединений молекулярной структуры является постоянным независимо от способа
- 56. Соединения постоянного состава - дальтониды (в память английского химика и физика Дальтона). Состав выражается простыми формулами
- 57. Закон постоянства состава вещества Так, СО2 можно получить по любой из следующих реакций: С + О2
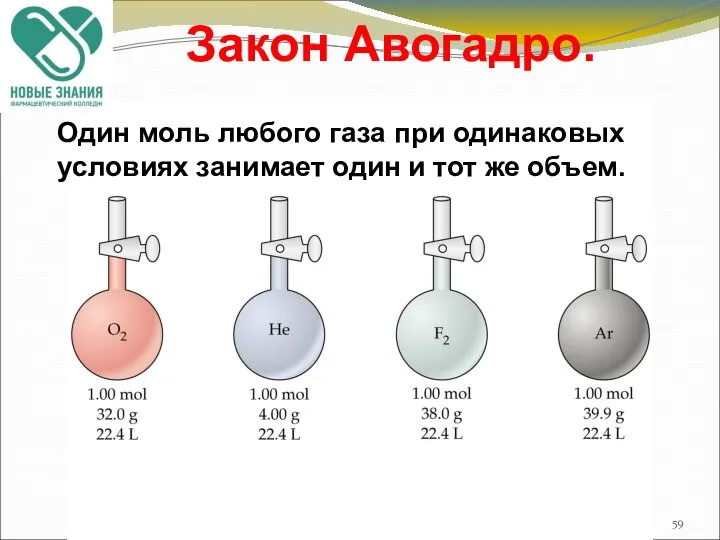
- 58. Основные законы химии Закон Авогадро. В равных объемах различных газов при одинаковых условиях (температура, давление и
- 59. Закон Авогадро. Один моль любого газа при одинаковых условиях занимает один и тот же объем.
- 60. Следствия из закона Авогадро : 1. Молярный объем газа VM – объем 1 моля газа при
- 61. Массы двух разных газов, занимающих одинаковый объем при одинаковых условиях, относятся между собой как их молярные
- 62. Количественные величины в химии
- 63. Примеры задач: 1.Какое количество вещества ( моль) содержит 12,04·10²³ атомов натрия? 2.Какова масса 2 моль азота?
- 64. Роль химии Роль химии в жизни современного общества очень велика. Она проникла во все сферы деятельности
- 65. Что дала людям химия
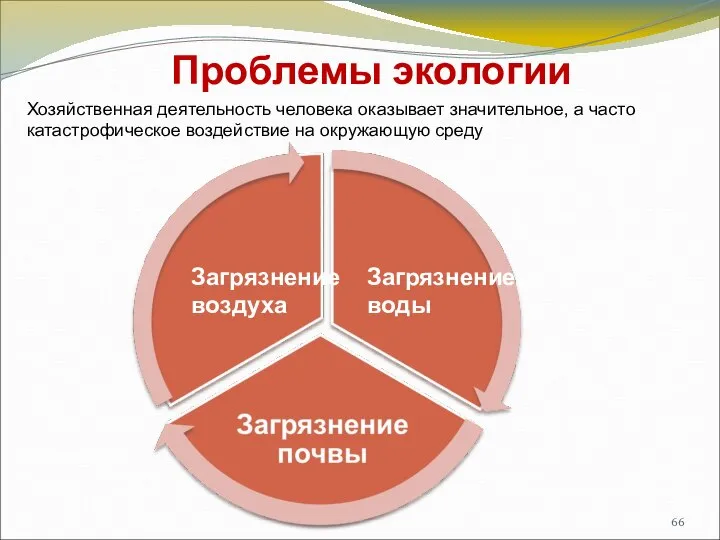
- 66. Проблемы экологии Загрязнение воды Загрязнение воздуха Хозяйственная деятельность человека оказывает значительное, а часто катастрофическое воздействие на
- 67. 1. Загрязнение атмосферы Естественное газы ,выделяющиеся в результате горения лесов, извержения вулканов, биохимических реакций атмосферная пыль,
- 68. 2. Основные источники загрязнения воды
- 69. 3. Проблема земельных ресурсов
- 70. Истинное положение дел Природную среду загрязняют разные отрасли хозяйства, помимо химической промышленности:
- 71. Выводы : Опасна не сама ХИМИЯ, а пренебрежение её законами или их неумелое использование Без ХИМИИ
- 72. Значение общей и неорганической химии В подготовке провизоров общая и неорганическая химия являются теоретической базой для
- 73. Рассчитайте молярную массу: 1 моль Fe2(SO3)3 2 моль Al(OH)3 3 моль CaO Примеры заданий:
- 75. Список используемой литературы О.С. Габриелян, И.Г. Остроумов, Е.Е. Остроумова, С.А. Сладков. Химия для профессий и специальностей
- 77. Скачать презентацию










































![Молярная масса (М) – масса 1 моля вещества в граммах [М]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396921/slide-47.jpg)






















 Осадочные горные породы
Осадочные горные породы Фізичні та хімічні властивості солей
Фізичні та хімічні властивості солей  Комплексные соединения
Комплексные соединения Total Syntheses of Trichorabdal A and Maoecrystal Z
Total Syntheses of Trichorabdal A and Maoecrystal Z Презентация по Химии "Кто хочет стать отличником" - скачать смотреть
Презентация по Химии "Кто хочет стать отличником" - скачать смотреть  Каталитический синтез нуклеозидов и других пребиотических производных формамида при протонном облучении метеоритов
Каталитический синтез нуклеозидов и других пребиотических производных формамида при протонном облучении метеоритов Тема урока "Основания" - презентация_
Тема урока "Основания" - презентация_ Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Урок по химии в 10 классе по теме Каучуки
Урок по химии в 10 классе по теме Каучуки Презентация по Химии "Основы" - скачать смотреть бесплатно
Презентация по Химии "Основы" - скачать смотреть бесплатно Органічні сполуки: ліпіди
Органічні сполуки: ліпіди Алкадиены. Состав и строение
Алкадиены. Состав и строение Химики на службе у дорог
Химики на службе у дорог Серная кислота и её свойства
Серная кислота и её свойства Презентация по Химии "РЕАКЦИИ АЛЬДЕГИДНОЙ ГРУППЫ" - скачать смотреть бесплатно
Презентация по Химии "РЕАКЦИИ АЛЬДЕГИДНОЙ ГРУППЫ" - скачать смотреть бесплатно Электродные потенциалы. Гальванические элементы. ЭДС
Электродные потенциалы. Гальванические элементы. ЭДС Роль ионов в неживой природе и в жизни людей
Роль ионов в неживой природе и в жизни людей ФКХ-Л2 2016
ФКХ-Л2 2016 Вода: фізичні та хімічні властивості. Поширеність в природі
Вода: фізичні та хімічні властивості. Поширеність в природі Соли «Na2SO4»
Соли «Na2SO4» Химическая реакция
Химическая реакция Атомы, молекулы и ионы
Атомы, молекулы и ионы Вещества по их способности проводить электрический ток в растворах
Вещества по их способности проводить электрический ток в растворах Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Исследование воздействия плазмы метана на свойства оксида графена
Исследование воздействия плазмы метана на свойства оксида графена Значення хімії у повсякденному житті Значення хімії у побуті
Значення хімії у повсякденному житті Значення хімії у побуті  Липиды. Классификация
Липиды. Классификация ХИМИЧЕСКОЕ РАВНОВЕСИЕ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯ.
ХИМИЧЕСКОЕ РАВНОВЕСИЕ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯ.