Содержание
- 2. «Продолжай успешно идти по дороге, на которой хорошо начал свой путь» (Из античной мудрости)
- 3. Взаимопроверка домашнего задания.
- 4. Взаимопроверка домашнего задания. Упражнение 2, с. 169. 2NaCl + H2SO4 = Na2SO4 + 2HCl (р. обмена)
- 5. Санатории Беларуси
- 6. Классная работа. Основания.
- 7. План изучения темы: Состав, названия и определение оснований. Классификация оснований. Физические свойства оснований. Химические свойства оснований.
- 8. Минута истории
- 9. Страна Оснований раздел Воспоминаний (состав, названия и определение оснований)
- 10. Основания – это сложные вещества, состоящие из атома металла и одной или нескольких гидроксогрупп.
- 11. Состав оснований: Назовите составные части оснований. Ме(ОН)х Валентность гидроксогруппы (ОН) – I Количество гидроксогрупп определяется валентностью
- 12. Выберите формулы оснований. Назовите их. НСl, NaOH, Na2O, Ca(OH)2, H2SO4, P2O5, Fe(OH)3, MgO, Cи(OH)2
- 13. Основания NaOH – гидроксид натрия Ca(OH)2 – гидроксид кальция Fe(OH)3 – гидроксид железа (III) Cи(OH)2 –
- 14. Страна Оснований раздел Классификаций
- 15. Классификация оснований NaOH KOH Ba(OH)2 LiOH Cu(OH)2 Al(OH)3 Ni(OH)2 Fe(OH)2 Fe(OH)3 Нерастворимые Растворимые (щелочи)
- 16. Таблица растворимости кислот, оснований, солей
- 18. По какому признаку основания разделены на группы? NaOH KOH LiOH СsOH Cu(OH)2 Ba(OH)2 Pb(OH)2 Fe(OH)2 Al(OH)3
- 19. Однокислотные NaOH, KOH Двухкислотные Pb(OH)2, Fe(OH)2 Трехкислотные Al(OH)3 Классификация оснований по числу гидроксогрупп. Основания
- 20. Выполните задание
- 21. Страна Оснований раздел Физический (свойства)
- 22. Физические свойства оснований Агрегатное состояние: Все твердые вещества Цвет кислот: Белого – КОН, Голубого - Cu(OH)2
- 23. Физкультминутка
- 24. Страна Оснований раздел Химический (свойства)
- 25. Самостоятельная работа с учебником с.172 (табл. 17).
- 26. Химические свойства нерастворимых оснований. 1). Разлагаются при нагревании. 2). Взаимодействуют с кислотами (реакция нейтрализации).
- 27. Смотрим видеофрагмент
- 28. 1. Термическое разложение нерастворимых оснований: Химические свойства оснований: t t
- 29. 2. Основание + кислота: Химические свойства оснований: Реакция нейтрализации – это…
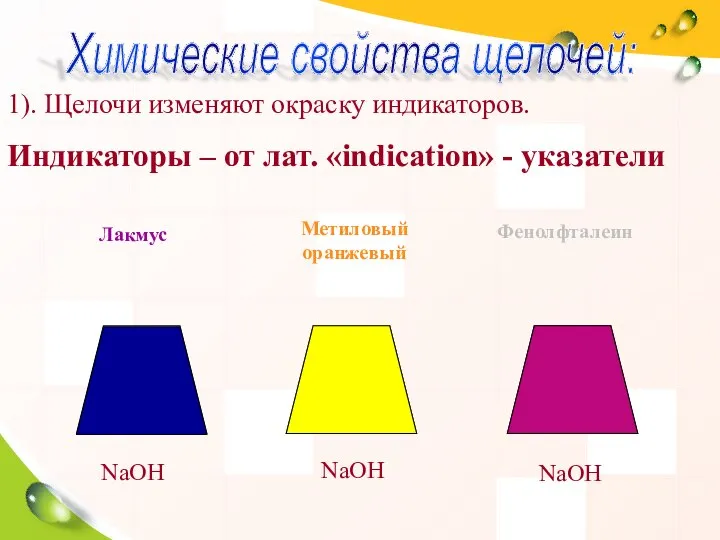
- 30. Химические свойства щелочей. 1). Изменяют окраску индикаторов. Взаимодействуют с: 2). кислотами (реакция нейтрализации), 3). кислотными оксидами,
- 31. ПРАВИЛА БЕЗОПАСНОСТИ Едкое вещество—щелочь! Разрушает и раздражает кожу, слизистые оболочки. Попавшие на кожу капли раствора щелочи
- 32. 1). Щелочи изменяют окраску индикаторов. Индикаторы – от лат. «indication» - указатели NaOH NaOH NaOH Лакмус
- 33. Щелочь + кислота : Ва(ОН)2 + 2НСl = ВаСl2 + 2Н2О хлорид бария Химические свойства щелочей:
- 34. 3. Щелочь + кислотный оксид: Химические свойства щелочей: ! В ходе реакции образуется соль и вода
- 36. 4. Щелочь + соль = Химические свойства щелочей: Условия протекания реакции: 1). исходные вещества должны быть
- 37. Минута истории Какие основания получили алхимики?
- 38. Выполните задание. Допишите уравнения реакций. Назовите вещества. 1 ВАРИАНТ 1). NaOH + H2SO4 = 2). NaOH
- 39. Кто может о своей работе на уроке сказать: «Я сегодня на уроке не работал, отдыхал!»?
- 40. Кто может о своей работе на уроке сказать: «Я сегодня на уроке не все понял, потому
- 41. Кто может о своей работе на уроке сказать: «Я сегодня на уроке хорошо поработал! Все понял,
- 42. Д/З § 39, у. 2, 5, 6, 11* с. 174-175.
- 44. Скачать презентацию








































 Кинетика химических реакций. (Лекция 12)
Кинетика химических реакций. (Лекция 12) Углеводороды. Природный газ. Алканы
Углеводороды. Природный газ. Алканы Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура соединений
Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура соединений Исследование химического состава шоколада и способов его приготовления
Исследование химического состава шоколада и способов его приготовления Природные источники углеводородов
Природные источники углеводородов Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ
Практическое занятие № 1. Техника безопасности при работе в химической лаборатории. Описание веществ Химические свойства карбокатионов
Химические свойства карбокатионов Аттестационная работа. Многогранники: от молекулы до кристалла
Аттестационная работа. Многогранники: от молекулы до кристалла Химия переходных элементов
Химия переходных элементов ОКСИДИ – це бінарні сполуки , що складаються з двох елементів , одним з яких є Оксиген . Загальна формула оксидів : E2On n – вале
ОКСИДИ – це бінарні сполуки , що складаються з двох елементів , одним з яких є Оксиген . Загальна формула оксидів : E2On n – вале Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие
Анализ смеси катионов первойтретьей аналитических групп по систематическому анализу. Химическое равновесие ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров
ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров Презентация по Химии "Азотная кислота" - скачать смотреть
Презентация по Химии "Азотная кислота" - скачать смотреть  Історія виникнення мила Розмаїтого Дмитра, 9-Б клас
Історія виникнення мила Розмаїтого Дмитра, 9-Б клас  Электрохимические методы анализа. Лекция 3
Электрохимические методы анализа. Лекция 3 Тривиальные названия неорганических соединений
Тривиальные названия неорганических соединений Структура аминокислот
Структура аминокислот Дифференцированный подход в обучении химии
Дифференцированный подход в обучении химии Физико-химические методы анализа
Физико-химические методы анализа Кинетические методы анализа
Кинетические методы анализа Полипропилен. Молекулалық құрылымы
Полипропилен. Молекулалық құрылымы Фенолы. Физические свойства. Получение
Фенолы. Физические свойства. Получение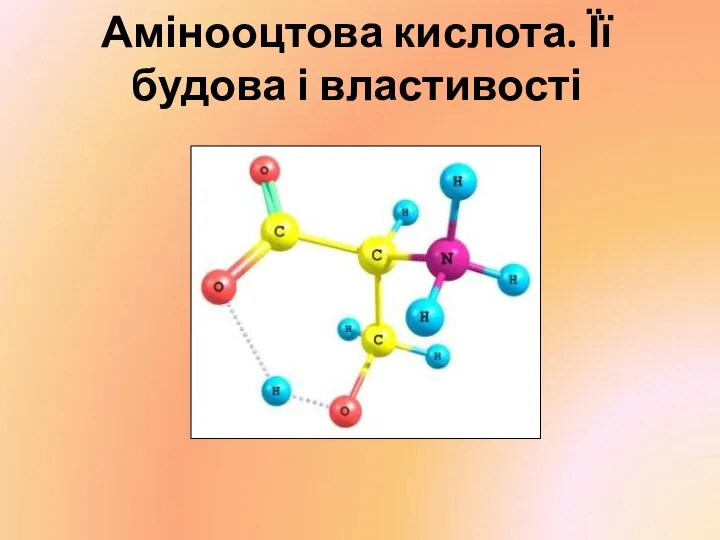 Амінооцтова кислота. Її будова і властивості
Амінооцтова кислота. Її будова і властивості Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері
Пестицидтердің қоршаған ортаға зиян-ын тигізбеу жүйесі. Пестицидтерді қолданудың физикалық-химиялық негіздері Пища, с точки зрения химика
Пища, с точки зрения химика Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией
Изомерия алкенов. Цель урока: закрепить понятие изомеры, познакомить с геометрической изомерией  Классификация минералов по химическому принципу
Классификация минералов по химическому принципу