Содержание
- 2. Основания- это сложные вещества, состоящие из ионов металла и одной или нескольких гидроксогрупп ОН⁻ (степень окисления
- 3. Ионы бывают Сложные - те, которые состоят из атомов двух и более химических элементов Например: Простые
- 4. Название оснований Гидроксид + Название металла в родительном падеже + Валентность римскими цифрами Пример: Fe(OH)3 Гидроксид
- 5. Степень окисления гидроксогруппы – Количество гидроксогрупп определяется валентностью металла, образующего основание. Например:
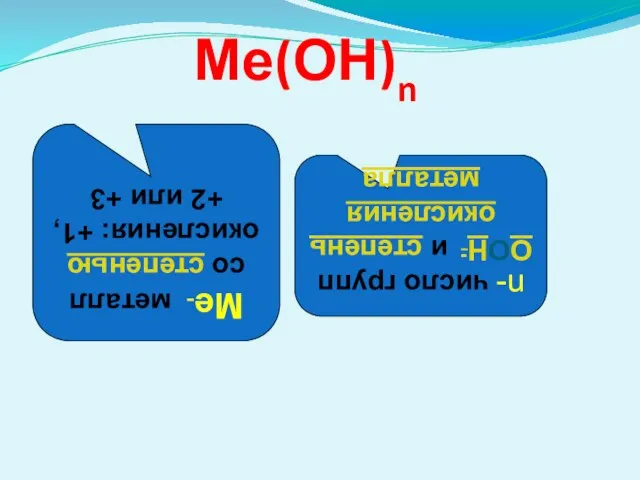
- 6. Ме(ОН)n Ме- металл со степенью окисления: +1, +2 или +3 n- число групп ООН- и степень
- 7. Если заряд иона металла равен +1, то формула гидроксида МеОН Если заряд иона металла равен +2
- 8. Классификация оснований Однокислотные Многокислотные NaOH КOH Al(OH)3 Сu(OH)2
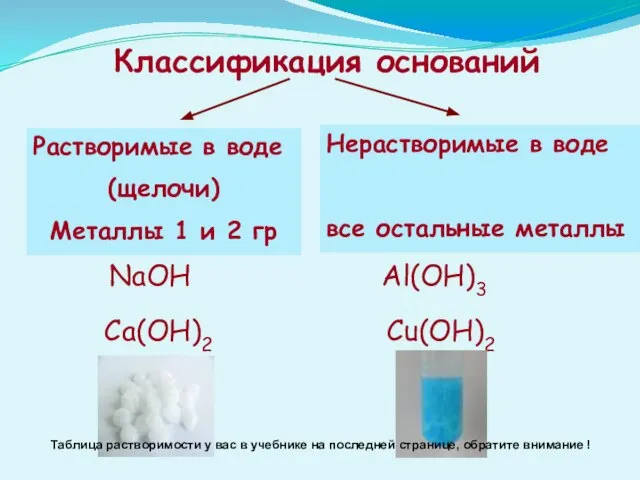
- 9. Классификация оснований Растворимые в воде (щелочи) Металлы 1 и 2 гр Нерастворимые в воде все остальные
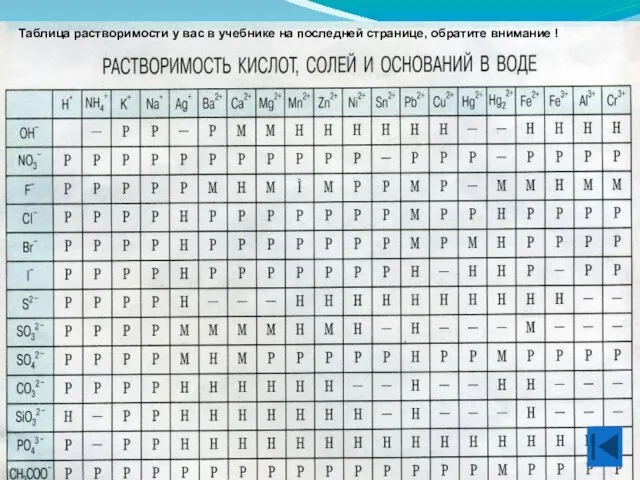
- 10. Таблица растворимости у вас в учебнике на последней странице, обратите внимание !
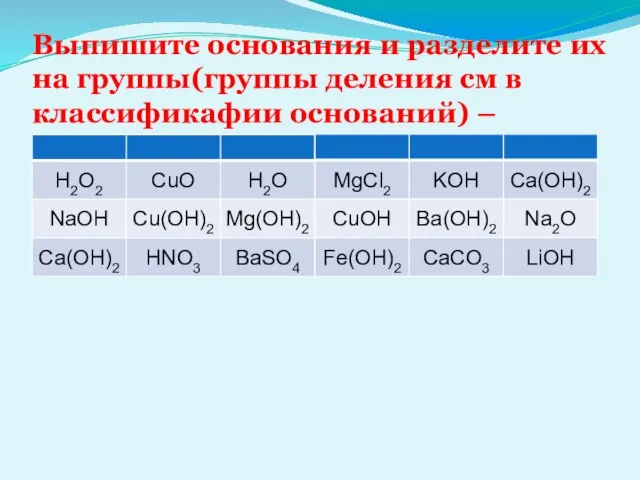
- 12. Выпишите основания и разделите их на группы(группы деления см в классификафии оснований) –
- 13. Гидроксид кальция (заполнить информацию)
- 14. Гидроксид натрия (заполнить информацию)
- 15. Гидроксид калия (заполнить информацию)
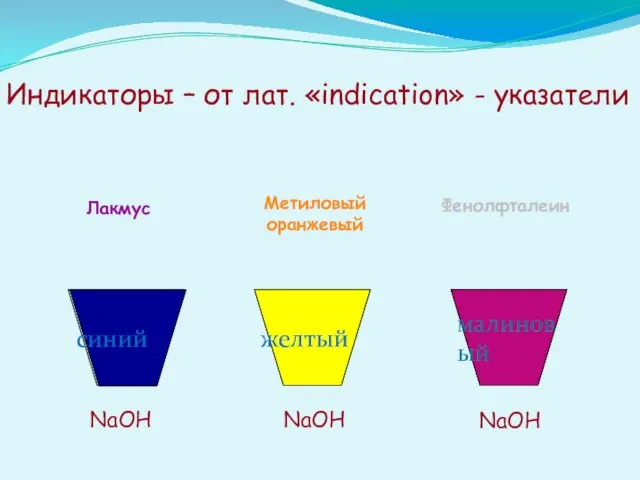
- 16. Изменение окраски индикатора в щелочной среде Бесцветный фенолфталеин—малиновый Метиловый оранжевый — желтый Лакмус — синий
- 17. Индикаторы – от лат. «indication» - указатели NaOH NaOH NaOH Лакмус Метиловый оранжевый Фенолфталеин желтый малиновый
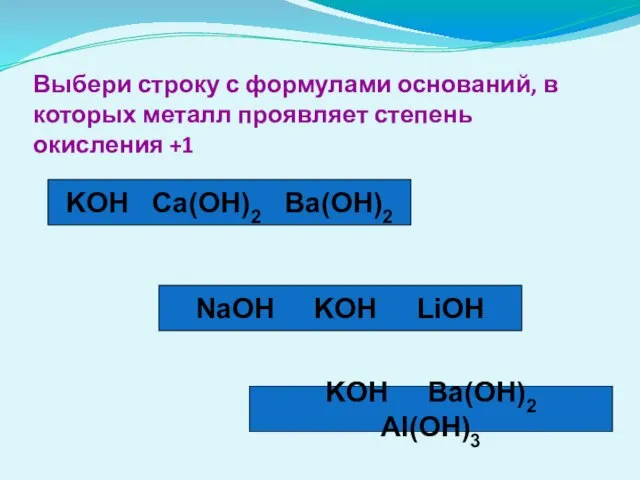
- 18. KOH Ca(OH)2 Ba(OH)2 Выбери строку с формулами оснований, в которых металл проявляет степень окисления +1 NaOH
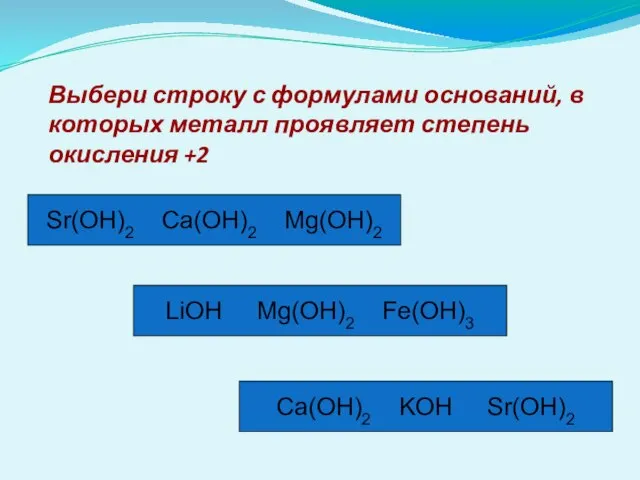
- 19. Выбери строку с формулами оснований, в которых металл проявляет степень окисления +2 Sr(OH)2 Ca(OH)2 Mg(OH)2 LiOH
- 20. Выбери строку с формулами оснований, в которых металл проявляет степень окисления +3 KOH Ba(OH)2 Al(OH)3 KOH
- 22. Скачать презентацию











 Требования к осадителю
Требования к осадителю Круговорот химических веществ в природе Выполнила: Подсыпанина Наташа Ученица: 10 «А» класса Учитель: Макарова Е. И.
Круговорот химических веществ в природе Выполнила: Подсыпанина Наташа Ученица: 10 «А» класса Учитель: Макарова Е. И. Будем знакомы -
Будем знакомы - Радиационная стойкость материалов
Радиационная стойкость материалов Гравиметрический метод анализа
Гравиметрический метод анализа Алкены (этиленовые углеводороды, олефины)
Алкены (этиленовые углеводороды, олефины) Самовосстанавливающиеся материалы
Самовосстанавливающиеся материалы Углеводы: моносахариды, олигосахариды и полисахариды
Углеводы: моносахариды, олигосахариды и полисахариды The ideal gas equation
The ideal gas equation Функции белков
Функции белков  Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В.
Применение алканов Работа Гончаровой Натальи Ученицы 11 «А» класса Учитель: Попова И.В. Общая и неорганическая химия
Общая и неорганическая химия Властивості газів
Властивості газів Кислые породы умеренно-щелочного ряда
Кислые породы умеренно-щелочного ряда Щелочные металлы
Щелочные металлы Презентация по Химии "Йод" - скачать смотреть
Презентация по Химии "Йод" - скачать смотреть  Синтез ультрадисперсного мела для различных эффективных использований
Синтез ультрадисперсного мела для различных эффективных использований Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Презентация по Химии "КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ" - скачать смотреть бесплатно
Презентация по Химии "КЛАССИФИКАЦИЯ ХИМИЧЕСКИХ РЕАКЦИЙ" - скачать смотреть бесплатно Щелочные металлы
Щелочные металлы Особенности течения кариеса во временных зубах
Особенности течения кариеса во временных зубах The phenomenon of radioactivity. Radioisotopes. The nuclear reaction
The phenomenon of radioactivity. Radioisotopes. The nuclear reaction Небелковые азотистые компаненты крови
Небелковые азотистые компаненты крови Презентация по Химии "Молочная кислота" - скачать смотреть _
Презентация по Химии "Молочная кислота" - скачать смотреть _ Презентация Соединения химических элементов 8 класс.
Презентация Соединения химических элементов 8 класс.  Щелочноземельные металлы
Щелочноземельные металлы 6 КАЗ Изохинолин туынд
6 КАЗ Изохинолин туынд Солі амонію
Солі амонію