Содержание
- 2. Что изучает химия? Химия – это наука о веществах, их составе, строении, свойствах и превращениях. Вещество
- 3. Что больше: атом или молекула? Атом – это мельчайшая, химически неделимая частица вещества. Атом является электронейтральным
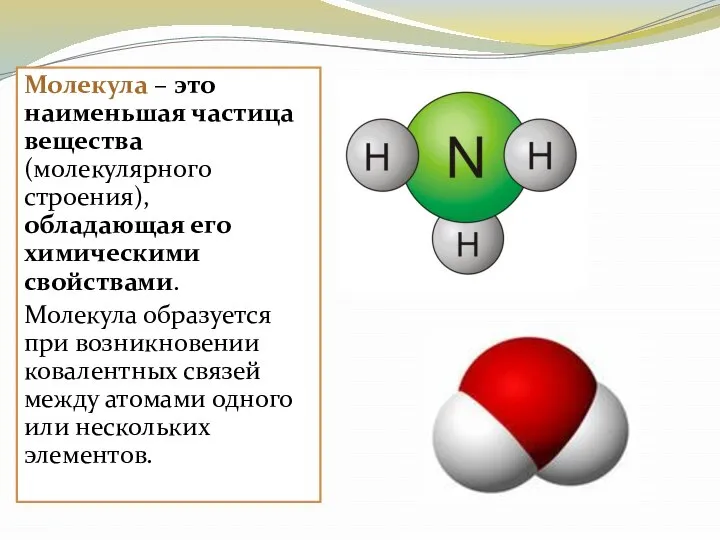
- 4. Молекула – это наименьшая частица вещества (молекулярного строения), обладающая его химическими свойствами. Молекула образуется при возникновении
- 5. Химический элемент или простое вещество? Химический элемент – это совокупность атомов с одинаковым зарядом ядра (числом
- 6. Для измерения атомных масс применяют атомную единицу массы (а. е. м.). Атомная единица массы – это
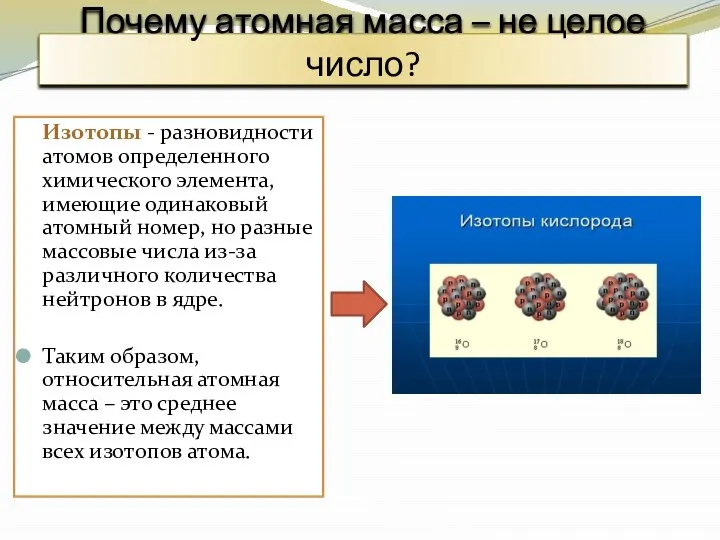
- 7. Почему атомная масса – не целое число? Изотопы - разновидности атомов определенного химического элемента, имеющие одинаковый
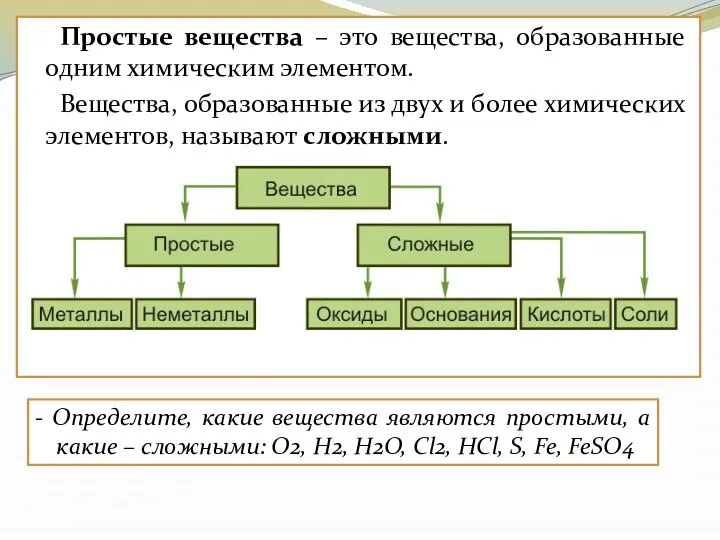
- 8. Простые вещества – это вещества, образованные одним химическим элементом. Вещества, образованные из двух и более химических
- 10. Пример: Al2O3 индексы, показывающие количество атомов алюминия и кислорода Качественный состав – это совокупность химических элементов
- 11. Закон постоянства состава вещества Сформулирован Ж.-Л. Прустом в 1799 г.: Всякое чистое вещество независимо от способа
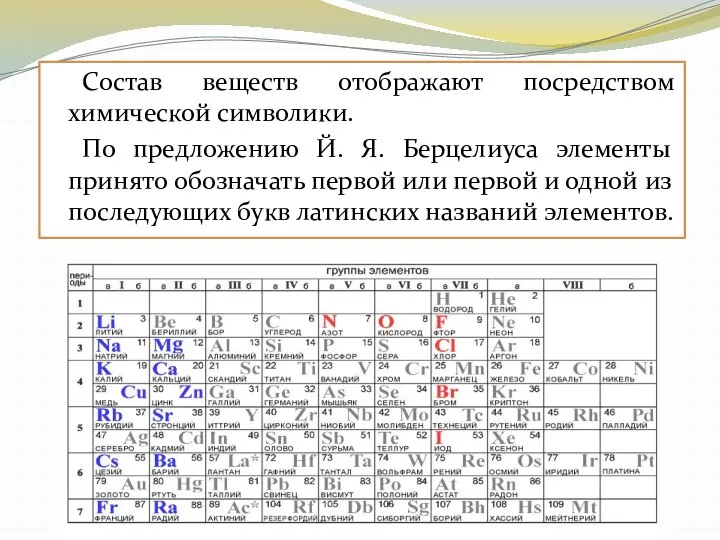
- 12. Состав веществ отображают посредством химической символики. По предложению Й. Я. Берцелиуса элементы принято обозначать первой или
- 13. Химические формулы Химическая формула – это способ отображения химического состава вещества. Она обозначает название вещества, одну
- 14. Формулы вещества составляют на основании важнейшего понятия в химии – валентности. Валентность – это способность атомов
- 15. Составьте формулы веществ: Оксида натрия Хлорида железа (III) Оксида углерода (IV) I II NaO → Na2O
- 16. Как определить массу молекулы? Относительная молекулярная масса ( ) равна сумме относительных атомных масс всех атомов,
- 17. Сколько кислорода в молекуле воды? Массовая доля элемента в веществе - ώ (омега) – это отношение
- 18. Химические реакции - Это явления, в результате которых из одних веществ образуются другие. Происходят ли изменения
- 19. Химическим уравнением называют запись химической реакции посредством химических знаков и формул. Уравнение реакции составляют на основе
- 20. Типы химических реакций 1) Соединение: Н2 + О2 → Н2О 2Н2 + О2 → 2Н2О 2)
- 21. Что такое количество вещества? По химическим уравнениям можно вести расчеты. Для этого нужно знать такие понятия
- 23. Один моль любого газа при одинаковых условиях занимает один и тот же объем. Этот объем, называемый
- 25. Был сформулирован в 1811 году итальянским физиком Амедео Авогадро (1776—1856) Закон основан на том факте, что
- 26. 1.Какое количество вещества (моль) содержит 12,04·10²³ атомов натрия? ν(Na) = N/NА = 12,04·10²³ / 6,02·10²³ =
- 28. Скачать презентацию




















 Диеновые углеводороды (алкадиены)
Диеновые углеводороды (алкадиены) Обмен углеводов
Обмен углеводов Натуральные и синтетические каучуки
Натуральные и синтетические каучуки Кобальт. Нахождение Co в природе
Кобальт. Нахождение Co в природе Викторина по химии
Викторина по химии Периодический закон. Периодическая система химических элементов
Периодический закон. Периодическая система химических элементов Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы амины 10 класс
амины 10 класс Золото Aurum
Золото Aurum Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23)
Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23)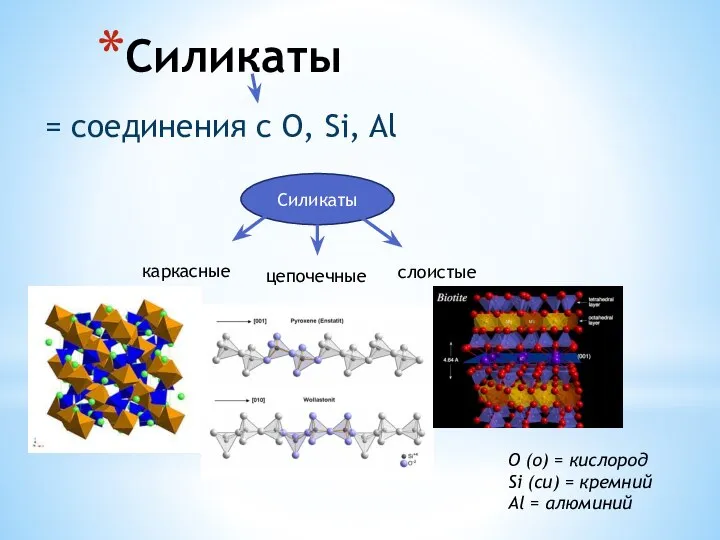 Силикаты. Гранат. Берилл
Силикаты. Гранат. Берилл Курс химии (Литвиновой Татьяны Николаевны)
Курс химии (Литвиновой Татьяны Николаевны) Клонирование генов, создание геномных и кДНК-библиотек, искусственный синтез генов
Клонирование генов, создание геномных и кДНК-библиотек, искусственный синтез генов Реология расплавов и растворов полимеров
Реология расплавов и растворов полимеров Презентация по Химии "Химические антонимы" - скачать смотреть
Презентация по Химии "Химические антонимы" - скачать смотреть  Побочная подгруппа VIII группы периодической системы
Побочная подгруппа VIII группы периодической системы Цикл Кальвина
Цикл Кальвина Белки. Классификация белков. (Тема 2)
Белки. Классификация белков. (Тема 2) Відносна молекулярна маса. Масова частка елемента в складній речовині
Відносна молекулярна маса. Масова частка елемента в складній речовині Презентация 30
Презентация 30 Фосфорные удобрения
Фосфорные удобрения МОУ Квитокская средняя общеобразовательная школа. УРОК ХИМИИ. 11 КЛАСС. Химия и производство. Учитель: Левицкая Лариса Виктор
МОУ Квитокская средняя общеобразовательная школа. УРОК ХИМИИ. 11 КЛАСС. Химия и производство. Учитель: Левицкая Лариса Виктор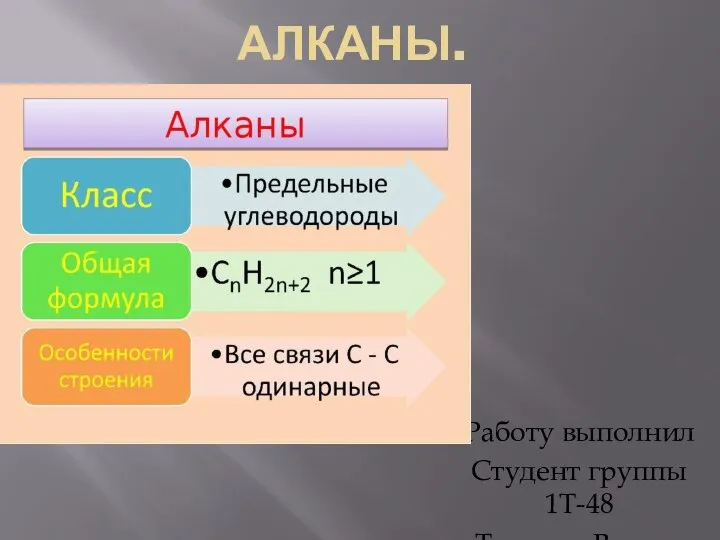 Алканы. Гомологический ряд и изомерия
Алканы. Гомологический ряд и изомерия Амины. Общая характеристика, номенклатура, изомерия. Получение. Физико-химические свойства. Отдельные представители
Амины. Общая характеристика, номенклатура, изомерия. Получение. Физико-химические свойства. Отдельные представители Гетерогенные и лигандообменные равновесия и процессы
Гетерогенные и лигандообменные равновесия и процессы Лекция 10. Химия s-элементов
Лекция 10. Химия s-элементов Оксиды
Оксиды Кислородсодержащие органические соединения
Кислородсодержащие органические соединения