Содержание
- 2. Если на систему, находящуюся в состоянии истинного равновесия, оказывается внешнее воздействие, то в системе возникает самопроизвольный
- 3. Л.5 Кинетика химических реакций Законы химической термодинамики позволяют определить направление и предел протекания возможного при данных
- 4. СКОРОСТЬ ХИМИЧЕСКОЙ РЕАКЦИИ Скорость химической реакции есть число элементарных актов химической реакции, происходящих в единицу времени
- 5. Наиболее часто в химии рассматривается зависимость концентрации реагентов от времени. В случае односторонних (необратимых) химических реакций
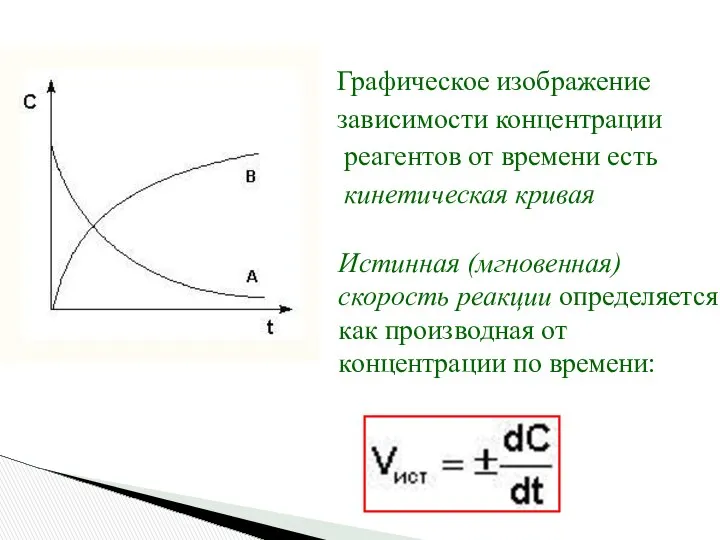
- 6. Графическое изображение зависимости концентрации реагентов от времени есть кинетическая кривая Истинная (мгновенная) скорость реакции определяется как
- 7. Истинную скорость реакции можно определить графически, проведя касательную к кинетической кривой. Истинная скорость реакции в данный
- 8. Если стехиометрические коэффициенты в уравнении химической реакции неодинаковы, величина скорости реакции будет зависеть от того, изменение
- 9. Скорость химической реакции зависит от множества факторов: природы реагирующих веществ, их концентрации, температуры, природы растворителя и
- 10. Кинетическое уравнение химической реакции. Порядок реакции. Одной из задач, стоящих перед химической кинетикой, является определение состава
- 11. Для реакции аА + bВ + dD + ... ––> еЕ + ... можно записать: Коэффициент
- 12. Зависимость скорости реакции от концентраций реагирующих веществ определяется экспериментально и называется кинетическим уравнением химической реакции. Для
- 13. Сумма показателей степени в кинетическом уравнении химической реакции (x + y + z) представляет собой общий
- 14. В химической кинетике принято классифицировать реакции по величине общего порядка реакции. Рассмотрим зависимость концентрации реагирующих веществ
- 15. Реакции нулевого порядка Для реакций нулевого порядка кинетическое уравнение имеет следующий вид: Скорость реакции нулевого порядка
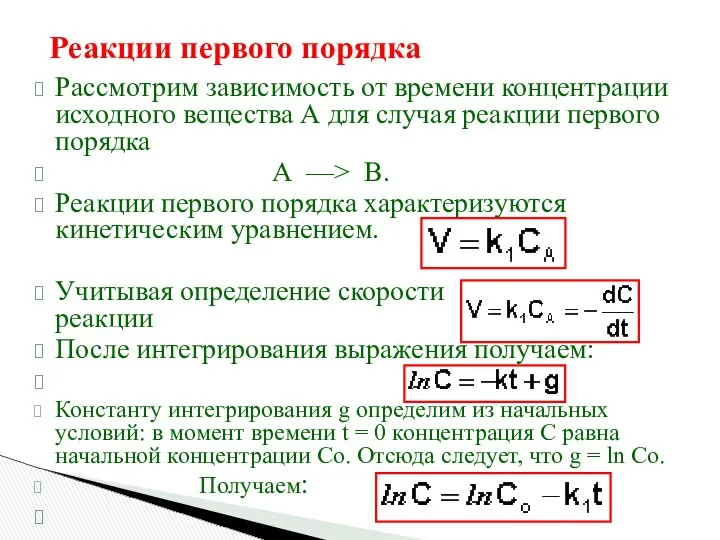
- 16. Реакции первого порядка Рассмотрим зависимость от времени концентрации исходного вещества А для случая реакции первого порядка
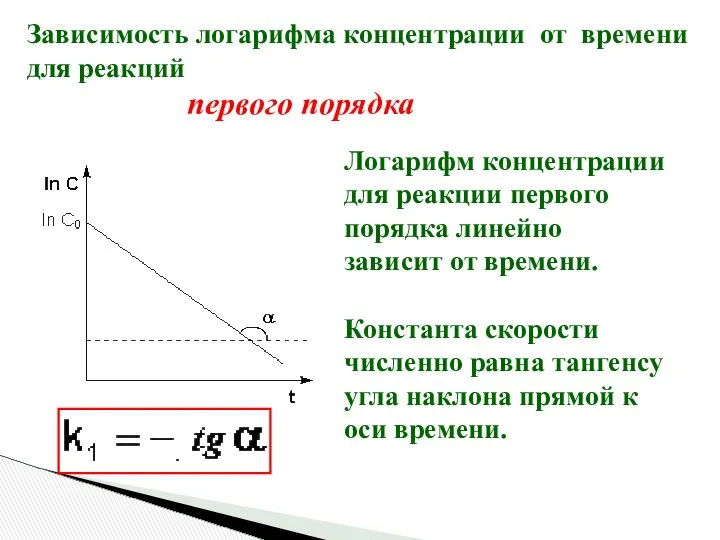
- 17. Зависимость логарифма концентрации от времени для реакций первого порядка Логарифм концентрации для реакции первого порядка линейно
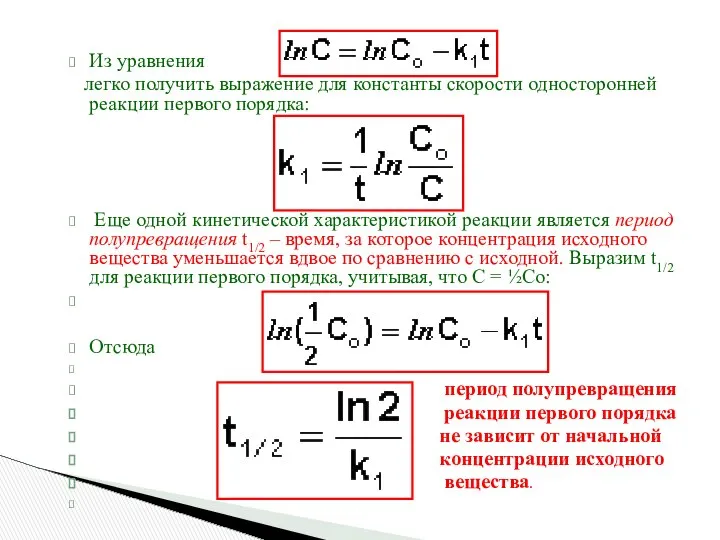
- 18. Из уравнения легко получить выражение для константы скорости односторонней реакции первого порядка: Еще одной кинетической характеристикой
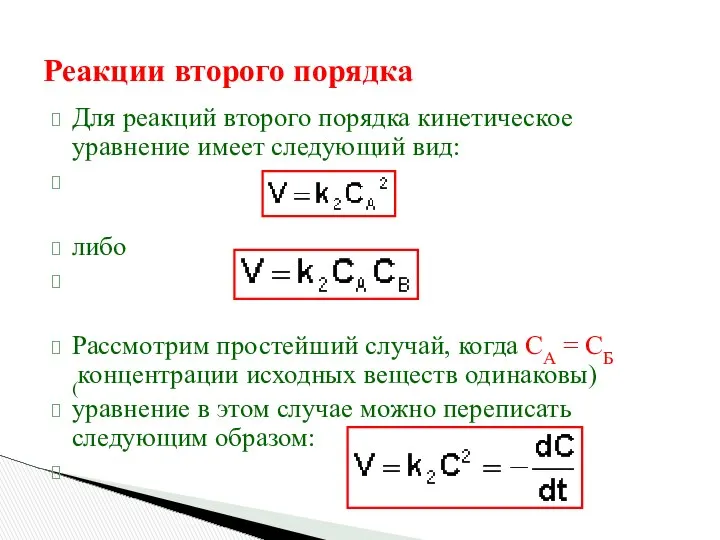
- 19. Реакции второго порядка Для реакций второго порядка кинетическое уравнение имеет следующий вид: либо Рассмотрим простейший случай,
- 20. После разделения переменных и интегрирования получаем: Постоянную интегрирования g, как и в предыдущем случае, определим из
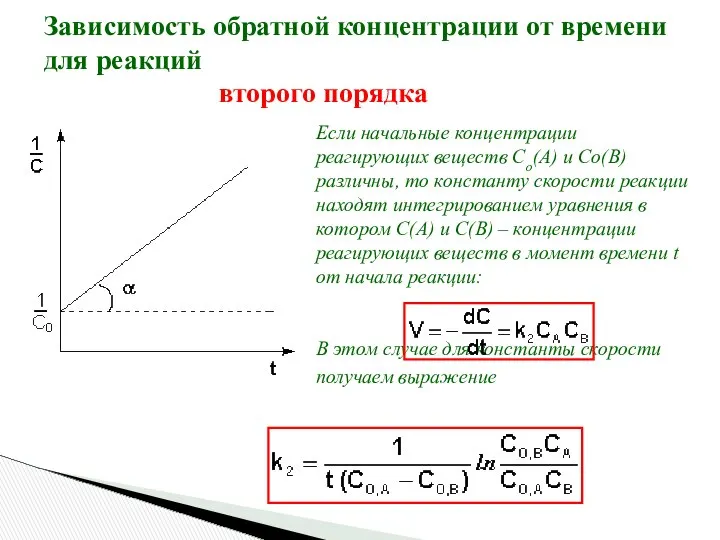
- 21. Зависимость обратной концентрации от времени для реакций второго порядка Если начальные концентрации реагирующих веществ Cо(А) и
- 23. Скачать презентацию














 Исследование защитного барьера зубных паст
Исследование защитного барьера зубных паст Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Прибор “октис-2”
Прибор “октис-2” Информационные технологии на уроках химии
Информационные технологии на уроках химии Нәруыз. Қасиеті және қызметі
Нәруыз. Қасиеті және қызметі Определение химии, как науки
Определение химии, как науки Пищевые жиры
Пищевые жиры  Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія
Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія  Буровые промывочные жидкости. Лекция 1
Буровые промывочные жидкости. Лекция 1 Решение задач по химической формуле
Решение задач по химической формуле Характеристика хімічного елемента Hg
Характеристика хімічного елемента Hg Презентация Аминокислоты и история их открытия
Презентация Аминокислоты и история их открытия Государственный медицинский университет г. Семей Кафедра химии и технологии лекарств СРС Тема: Аминоспирты и аминофенолы
Государственный медицинский университет г. Семей Кафедра химии и технологии лекарств СРС Тема: Аминоспирты и аминофенолы  Алкалоидтар. Алкалоидтар туралы жалпы түсінік
Алкалоидтар. Алкалоидтар туралы жалпы түсінік Закон сохранения массы веществ. Уравнения химических реакций
Закон сохранения массы веществ. Уравнения химических реакций Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Курс хімії за 11 клас
Курс хімії за 11 клас Презентация по Химии "Степень окисления" - скачать смотреть
Презентация по Химии "Степень окисления" - скачать смотреть  Скорость химических реакций
Скорость химических реакций Презентация по Химии "Коррозия металлов" - скачать смотреть
Презентация по Химии "Коррозия металлов" - скачать смотреть  Иодометрия. Перманганатометрия. Трилонометрия
Иодометрия. Перманганатометрия. Трилонометрия Патология углеводного обмена. (Тема 4)
Патология углеводного обмена. (Тема 4) «Неметаллы в жизни человека»
«Неметаллы в жизни человека» Электрохимия. Физико –химические свойства ионных систем. (Лекция 13)
Электрохимия. Физико –химические свойства ионных систем. (Лекция 13) Метаболизм углеводов
Метаболизм углеводов Топливо и топливосжигающие устройства
Топливо и топливосжигающие устройства Липидтер. Сабынданатын және сабынданбайтын липидтер
Липидтер. Сабынданатын және сабынданбайтын липидтер Минералы и их классификация
Минералы и их классификация