Содержание
- 2. * Термодинамика – это наука о взаимных превращениях различных видов энергии друг в друга, а также
- 3. * Система – это совокупность материальных объектов (тел), ограниченных мысленными или реально существующими границами от окружающей
- 4. * Системы бывают: открытые, в которых существует обмен энергией и веществом с окружающей средой; закрытые, в
- 5. * Две группы параметров характеризуют состояние любой т/д с-мы: Интенсивные т/д параметры (давление, температура, вязкость и
- 6. * Наряду с параметрами состояния используют функции состояния (энергию, энтальпию, энтропию…). Функции состояния рассчитывают исходя из
- 7. * Состояние с-мы характеризуется значением параметров и функций состояния (Т, р, V и т.д.), процесс характеризуется
- 8. * Для описания движения материи в живых организмах, используется: Энергия – общая количественная мера движения и
- 9. * Информация – мера организованности системы, т. е упорядоченности расположения и движения ее частиц.
- 10. * Первый закон т/д: 1) энергия не исчезает и не возникает из ничего, а только превращается
- 11. * 3) если к закрытой системе подвести теплоту Q, то эта энергия расходуется на увеличение внутренней
- 12. * Теплота Q – это форма беспорядочного (теплового) движения образующих тело частиц (в Дж или кал).
- 13. * При р,Т – const: А = р · ∆V, => Q = ∆U + A
- 14. * Энтальпия Н – это т/д функция, характеризующая энергетическое состояние системы при изобарно-изотермических условиях (р,Т –
- 15. * Экзотермические процессы сопровождаются выделением энергии из системы в окружающую среду, ∆Н Эндотермические процессы сопровождаются поглощением
- 16. * В т/д для оценки энергетического состояния веществ используются значения стандартных энтальпий образования этих веществ ∆Н0
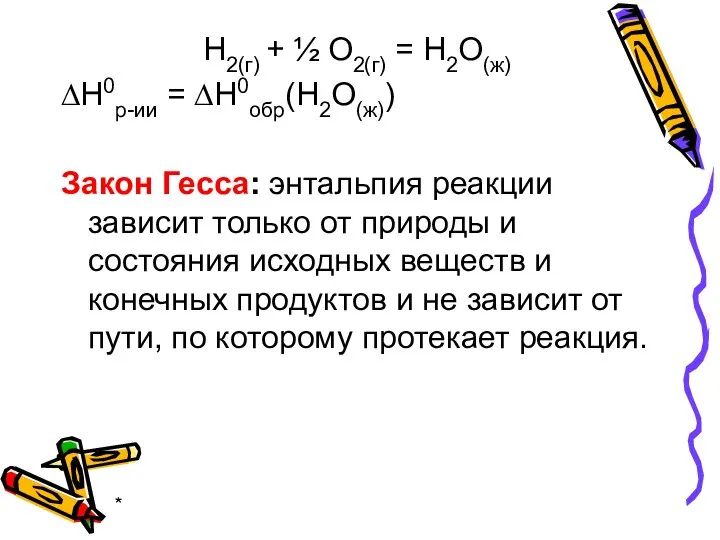
- 17. * Н2(г) + ½ О2(г) = Н2О(ж) ∆Н0р-ии = ∆Н0обр(Н2О(ж)) Закон Гесса: энтальпия реакции зависит только
- 18. * С(тв) + О2(г) = СО2(Г); ∆Н0 С(тв) + ½ О2(г) = СО(Г); ∆Н10 СО(г) +
- 19. * Первое следствие закона Гесса: энтальпия реакции равна разности алгебраической суммы ∆Н0обр всех продуктов реакции и
- 20. * Для реакции аА + вВ = dD + cC ∆Н0р-ии={d∆Н0(D)+c∆Н0(C)} – {a∆Н0(A)+b ∆Н0(B)}
- 21. * Второе следствие закона Гесса: энтальпия прямой реакции численно равна энтальпии обратной реакции, но с противоположенным
- 22. * В медицине энергетическую характеристику продуктов питания принято выражать в калориях (1 калория = 4,18 Дж)
- 23. * Для определения калорийности пищи пользуются выражением Q = Q(белка) + Q(жира) + Q(углеводов) и табличными
- 24. * обобщенной т/д функцией состояния системы, учитывающей энергетику и неупорядоченность системы при изобарно-изотермических условиях является энергия
- 25. * Изменение энергии Гиббса в результате любого процесса определяется только конечным и начальным состоянием системы, независимо
- 26. * Для реакции аА + вВ = dD + cC ∆G0р-ии={d∆G0(D)+с∆G0(С)} - {a∆G0(A)+b ∆G0(B)}
- 27. * ∆G для биохимических процессов в условиях, отличных от стандартных, можно рассчитать на основе экспериментальных значений
- 28. * Второй закон термодинамики: в системе при постоянной температуре и давлении самопроизвольно могут совершаться только такие
- 29. * Биохимические реакции, сопровождающиеся уменьшением энергии Гиббса, называют экзэргоническими реакциями, они могут совершаться самопроизвольно. Биохимические реакции,
- 30. * Чтобы в живых системах протекали эндэргонические реакции, необходимо, чтобы они были сопряжены с экзэргоническими реакциями.
- 31. * Например, эндэргоническая реакция глюкоза+фруктоза = сахароза +Н2О, ∆G>0 протекает только с экзэргонической реакцией гидролиза АТФ:
- 32. * особенности протекания обратимых биохимических реакций: стремление достичь динамического равновесия (равенства скоростей прямой и обратной реакций;
- 34. Скачать презентацию

















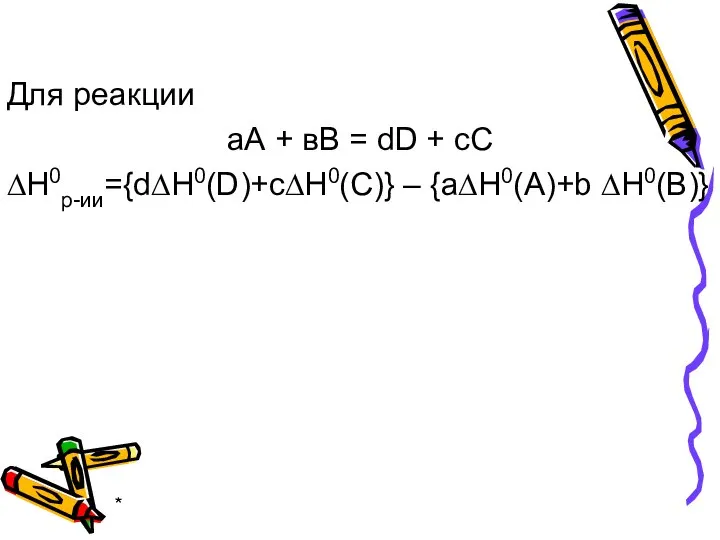












 Реакции при участии катализатора
Реакции при участии катализатора Диоксины и полихлорированные бифенилы: источники, распространение в окружающей среде, влияние на организм человека
Диоксины и полихлорированные бифенилы: источники, распространение в окружающей среде, влияние на организм человека Бактериалық жасушаның химиялық құрамы
Бактериалық жасушаның химиялық құрамы Создание косметических средств
Создание косметических средств Термодинамика и термохимия процессов горения и взрыва
Термодинамика и термохимия процессов горения и взрыва Шыны тәріздес фосфат
Шыны тәріздес фосфат Обобщение по теме неметаллы
Обобщение по теме неметаллы Хімія в медицині
Хімія в медицині  Получение металлов
Получение металлов  Химия в произведениях художественной литературы
Химия в произведениях художественной литературы Элементы группы галогенов
Элементы группы галогенов Степень окисления
Степень окисления Презентация по Химии "Вода как растворитель" - скачать смотреть
Презентация по Химии "Вода как растворитель" - скачать смотреть  Технологии, используемые в исследованиях лаборатории механизмов нейрохимической модуляции
Технологии, используемые в исследованиях лаборатории механизмов нейрохимической модуляции Реакции разложения и реакции соединения
Реакции разложения и реакции соединения Химические сюжеты в научно-фантастических произведениях
Химические сюжеты в научно-фантастических произведениях Простые и сложные эфиры
Простые и сложные эфиры Решение задач по уравнениям химических реакций
Решение задач по уравнениям химических реакций Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Білки. Властивості та функції
Білки. Властивості та функції Спирты. Классификация, номенклатура, изомерия. Спирты в природе
Спирты. Классификация, номенклатура, изомерия. Спирты в природе Реакции ионного обмена и условия их осуществления
Реакции ионного обмена и условия их осуществления Минералы земной коры
Минералы земной коры Электрохимические методы анализа: потенциометрия. Потенциометрическое титрование
Электрохимические методы анализа: потенциометрия. Потенциометрическое титрование Представники d-елементів (перехідних елементів) періодичної системи елементів
Представники d-елементів (перехідних елементів) періодичної системи елементів “Су. Ерітінділер” тарауын қорытындылау
“Су. Ерітінділер” тарауын қорытындылау Гетероциклические соединения
Гетероциклические соединения Снег и лед. Тайны твердой воды
Снег и лед. Тайны твердой воды