Содержание
- 2. Химический элемент – это… Атом – это ___________________ . Изотоп – это разновидность атома одного химического
- 3. Дмитрий Иванович Менделеев (1834-1907 ) Выдающийся русский химик, открывший периодический закон и создавший периодическую систему химических
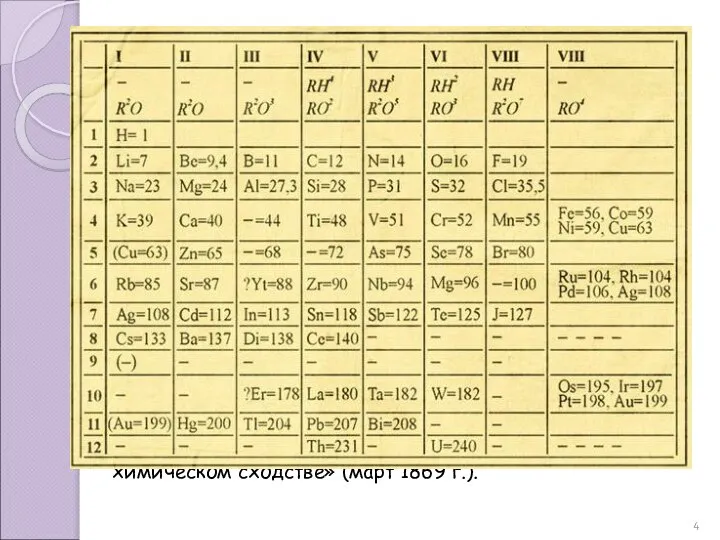
- 4. Первый вариант таблицы элементов, выражавшей периодический закон, Менделеев опубликовал в виде отдельного листка под названием «Опыт
- 5. * Современная периодическая таблица Д.И.Менделеева
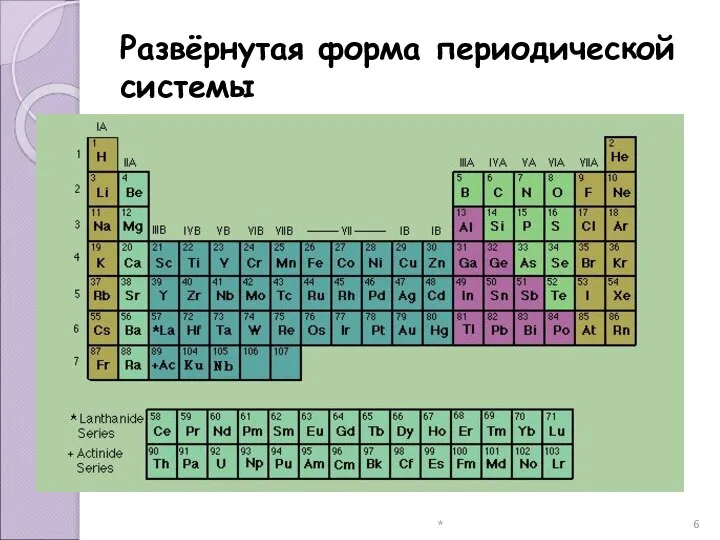
- 6. * Развёрнутая форма периодической системы
- 7. Структура периодической системы: Формулировка периодического закона «Свойства химических элементов и их соединений находятся в периодической зависимости
- 8. * Структура периодической системы: Понятие группы А) Группа – это расположение элементов по вертикали. Б) В
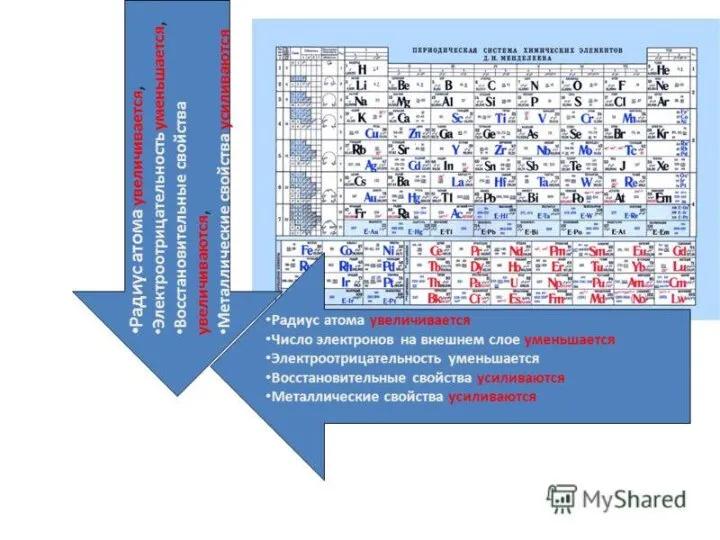
- 10. * Закономерности 1) В периодах степень окисления в высших оксидах и гидроксидах _ _ _ _
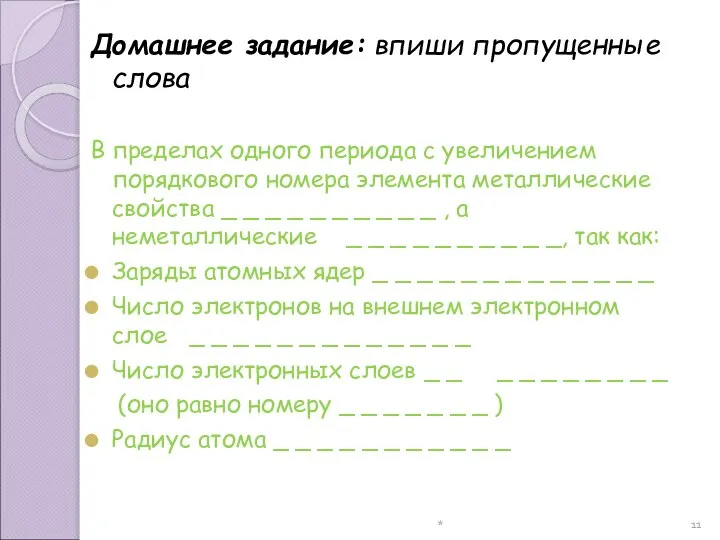
- 11. * Домашнее задание: впиши пропущенные слова В пределах одного периода с увеличением порядкового номера элемента металлические
- 12. * Домашнее задание: впиши пропущенные слова В пределах одной группы (главной подгруппы) с увеличением порядкового номера
- 13. * План характеристики химического элемента: 1. Положение в ПСХЭ: -Порядковый номер - Номер периода -Номер группы
- 14. ХАРАКТЕРИСТИКА ЭЛЕМЕНТА ПО ПОЛОЖЕНИЮ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ Д.И. МЕНДЕЛЕЕВА 3115 Р – 3 период, VA группа
- 15. * Задание: подчеркните символы химических элементов-металлов и расположите их в порядке ослабления металлических свойств: А) Cl;
- 16. * Задание: подчеркните символы химических элементов-неметаллов и расположите их в порядке усиления неметаллических свойств: А) Li;
- 17. * Задание. Расположи химические элементы в порядке возрастания - неметаллических свойств: а) P; S; Si. б)
- 18. * Задание: Сравните атомы поставив знаки ›, ‹ или = : А) заряд ядра: Al …
- 20. Скачать презентацию












 Законы химической термодинамики. Часть 1. Физическая и коллоидная химия
Законы химической термодинамики. Часть 1. Физическая и коллоидная химия Chemical Reactions and Stoichiometry
Chemical Reactions and Stoichiometry Азот Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов» Барсук
Азот Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов» Барсук 1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки
1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки  Наука плазмохимия
Наука плазмохимия Этимология названий химических элементов периодической системы Д.И. Менделеева
Этимология названий химических элементов периодической системы Д.И. Менделеева Основания. Гидроксид лития
Основания. Гидроксид лития Основы химической кинетики и химическое равновесие (лекция 5)
Основы химической кинетики и химическое равновесие (лекция 5) Глюкозаальдегидоспирт
Глюкозаальдегидоспирт Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения
Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения Строение вещества
Строение вещества Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Презентация по Химии "Свойства комплексных соединений" - скачать смотреть
Презентация по Химии "Свойства комплексных соединений" - скачать смотреть  Практикум по органической и биоорганической химии
Практикум по органической и биоорганической химии Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена
Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена Аттестационная работа. Образовательная программа кружка «Химия и жизнь»
Аттестационная работа. Образовательная программа кружка «Химия и жизнь» Признаки и условия протекания химических реакций
Признаки и условия протекания химических реакций Беймет алдар
Беймет алдар АЛЮМІНІЄВІ СПЛАВИ Підготувала учениця 10 класу Кисленко Єлизавета
АЛЮМІНІЄВІ СПЛАВИ Підготувала учениця 10 класу Кисленко Єлизавета  Коррозия металлов
Коррозия металлов The morphology and reactivity of model catalysts based on cobalt oxide
The morphology and reactivity of model catalysts based on cobalt oxide Классификация и номенклатура органических соединений
Классификация и номенклатура органических соединений Методы изготовления из резины и латекса
Методы изготовления из резины и латекса Чи шкідливі пральні порошки для здоров’я?
Чи шкідливі пральні порошки для здоров’я?  Виды химических реакций
Виды химических реакций Соединения химических элементов
Соединения химических элементов Concise asymmetric total synthesis of lycopodine
Concise asymmetric total synthesis of lycopodine