Содержание
- 2. А 1. По пять электронов на внешнем электронном слое находятся в в атоме каждого из химических
- 3. А 2. Радиус атомов увеличивается в ряду элементов 1. H, Li, Na 2. K, Na, Li
- 4. А 3. Ковалентная неполярная связь имеется в молекуле 1. молекуле воды 2. кристалле SO2 3. кристалле
- 5. А 4. Положительную степень окисления атом кислорода имеет в соединении 1. H2O 2. H2O2 3. F2O
- 6. А 5. К кислотным и соответственно основным оксидам относятся: 1. CO и Na2O 2. CO2 и
- 7. А 6. Водород массой 2 г полностью провзаимодействовал с 16 г кислорода. На основании закона сохранения
- 8. А 7. Взаимодействие гидроксида кальция с соляной кислотой относится к реакциям 1. соединения 2. обмена 3.
- 9. А 8. Сильным электролитом является 1. Угольная кислота 2. Сероводородная кислота 3. Серная кислота 4. сахароза
- 10. А 9. Сумма коэффициентов в уравнении электролитической диссоциации сульфата железа равна 1. 5 2. 2 3.
- 11. А 10. Вводном растворе практически полностью взаимодействуют между собой 1. BaCl2 и KOH 2. NaCl и
- 12. А 11. С каждым из веществ: H2O, Fe2O3, NaOH - будет взаимодействовать 1. алюминий 2. магний
- 13. А 12. Оксид алюминия реагирует с каждым из веществ: 1. CO и CO2 2. H2O и
- 14. А 13. Гидроксид кальция реагирует с: 1. углекислым газом 2. кислородом 3. водородом 4. поваренной солью
- 15. А 14. Разбавленная соляная кислота реагирует с каждым из веществ: 1. Cu и KOH 2. Na2CO3
- 16. А 15. Осуществить превращение Pb(NO3)2 → PbS можно с помощью 1. Сульфида натрия 2. Сульфита калия
- 17. А 16. К спиртам относятся все вещества в группе 1. CH3COOH, CH3OH, C2H2OH 2. C2H5OH, C3H7OH,
- 18. А 17. Чтобы на кухне отличить питьевую соду от поваренной соли, необходимо 1. Растворить вещества в
- 19. А 18. Наличие в растворе ионов серебра можно установить в результате реакции с 1. NaNO3 2.
- 20. А 19 Массовая доля кислорода в сульфате алюминия равна. 1. 4,7% 2. 12,8% 3. 56,1% 4.
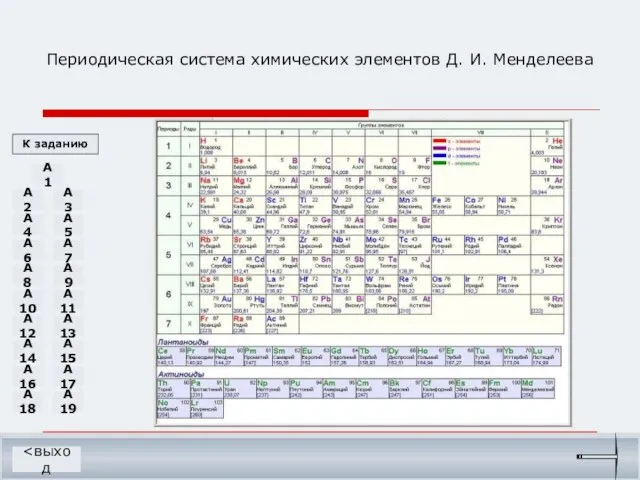
- 21. Периодическая система химических элементов Д. И. Менделеева К заданию A2 A3 A4 A5 A6 A7 A8
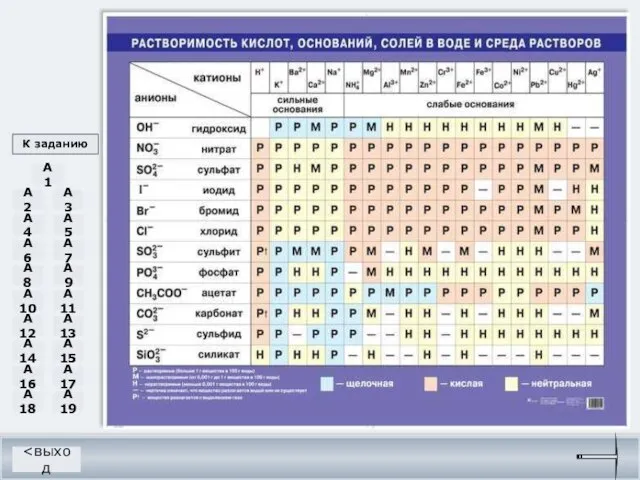
- 22. К заданию A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 A12 A13 A14 A15
- 23. Электрохимический ряд напряжения К заданию A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 A12
- 25. Скачать презентацию













 Цікаві факти про Харчові добавки Презентація Гладкіх Ксенії Учениці 11-В класу
Цікаві факти про Харчові добавки Презентація Гладкіх Ксенії Учениці 11-В класу  Кинетика сложных реакций
Кинетика сложных реакций Карбоновые кислоты
Карбоновые кислоты Аккумуляторы и их устройство
Аккумуляторы и их устройство Химическое равновесие. Протолитические равновесия и процессы в растворах электролитов
Химическое равновесие. Протолитические равновесия и процессы в растворах электролитов Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Оксиды. Определение, состав, номенклатура, классификация и структурные формулы
Оксиды. Определение, состав, номенклатура, классификация и структурные формулы Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Минералы. Значение минералов и задачи минералогии
Минералы. Значение минералов и задачи минералогии Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора
Взаимодействие плазмы с поверхностью. Проблемы термоядерного реактора Спирты. Классификация спиртов
Спирты. Классификация спиртов Лужні метали Підготувала: Анна Сідорова
Лужні метали Підготувала: Анна Сідорова  Загрязнение продуктов питания примесями, мигрирующими из оборудования, инвентаря, тары и упаковочных материалов
Загрязнение продуктов питания примесями, мигрирующими из оборудования, инвентаря, тары и упаковочных материалов Поліетелен. Застосування поліетилену
Поліетелен. Застосування поліетилену Химический элемент медь
Химический элемент медь Тема урока: Состав, переработка нефти и экологические проблемы связанные с ней.
Тема урока: Состав, переработка нефти и экологические проблемы связанные с ней. Диазины. Характеристика диазинов. (Лекция 8)
Диазины. Характеристика диазинов. (Лекция 8) Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Сульфат меди
Сульфат меди Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Понятие электродного потенциала и методы его измерения
Понятие электродного потенциала и методы его измерения Путешествие в мир углеводородов нефти
Путешествие в мир углеводородов нефти Звезды Лейденфроста
Звезды Лейденфроста Фотодыхание
Фотодыхание Уголь. Виды угля
Уголь. Виды угля Алюминий и его соединения
Алюминий и его соединения Растворы и их классификация
Растворы и их классификация МЫШЬЯК Презентацию подготовила Юдайханова Юлия Ученица 11 класса В
МЫШЬЯК Презентацию подготовила Юдайханова Юлия Ученица 11 класса В