Содержание
- 2. Слайд 2 ПАВ’ы – это полимерные вещества, у которых каждая молекула содержит два комплекта атомов или
- 3. Слайд 3 Границы раздела двух фаз; которые модифицируются ПАВ’ом (Примеры ПАВ в системах)
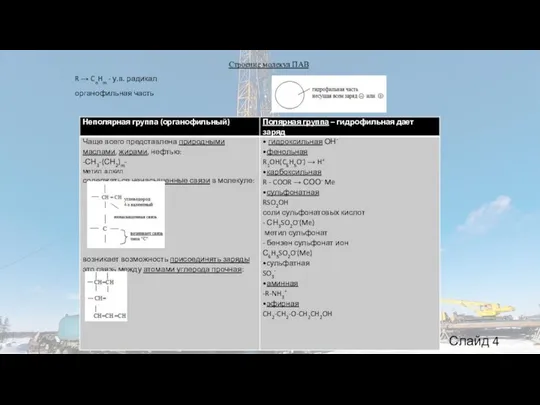
- 4. Строение молекул ПАВ R → CnHm - у.в. радикал органофильная часть Слайд 4
- 5. Cлайд 5 • алкильная группа в ПАВ’ах Унивалентный радикал, имеющий общую формулу: СnH2n+1 - Алкил (алкильная
- 6. Слайд 6 Классификация ПАВ 1 признак: характер водных растворов 1 группа: Спирты и жирные кислоты (низкие
- 7. Слайд 7 Классификация ПАВ по физико-химическому состоянию или по способности и характеру диссоциации в воде молекул
- 8. Слайд 8 Другие анионные ПАВ - Фторсодержащие – фтортензиды особые свойства: Высокая поверхностная активность; Хемо- и
- 9. Слайд 9 2 группа: неионогенные ПАВ не диссоциируют в водных растворах. Их молекулы проявляют поверхностную активность
- 10. Состав нефти. Нефть – сложная смесь углеводородов (различных классов) и неуглеводородных компонентов – кислородных, сернистых, азотных
- 11. Слайд 11 Виды ПАВ по происхождению: Природные ПАВ Нафтеновые кислоты (0,1-2%) в нефти: Низкомолекулярные нафтеновые кислоты
- 12. Синтетические ПАВ (СПАВ) - которые получены синтетическим путем и вводят в состав нефтей и др. процессах,
- 13. Основные свойства растворов ПАВ, определяющие параметры пен (ГЖС). К основным свойствам растворов ПАВ относят явления: Адсорбция
- 14. Влияние температуры на растворимость ПАВ 1) Ионогенные ПАВ – у большинства растворение сопровождается поглощением теплоты –
- 15. Растворимые в воде мыла (солей жирных кислот) RCOONa, RCOOK, RCOOCa и синтетические моющие средства (вещества) диссоциируют
- 16. В разбавленных водных растворах идет диссоциация: RCOONa, RCOOCa и СМВ диссоциируют: RCOONa + Н2О → NaOH
- 17. 2. Мицеллообразование Водные растворы ПАВ при определенной концентрации резко изменяют многие свойства Поверхностное натяжение Электропроводность Осмотическое
- 18. В водной среде: ассоциация дифильных молекул ПАВ происходит в результате гидрофобного взаимодействия углеводородных радикалов, которые образуют
- 19. При достижении определенной концентрации сферические мицеллы начинают взаимодействовать между собой , могут деформироваться и принимать цилиндрическую,
- 20. гидрофильно липофильный баланс – ГЛБ ГЛБ=Σ(ГЛБ)г - Σ(ГЛБ)л+7 Физический смысл - это отношение работы адсорбции ПАВ
- 21. К растворимости ПАВ о величине ГЛБ Метод растворимости ПАВ в воде (метод Гриффится) Слайд 21 ГЛБ
- 22. Самобилизация – коллоидное растворение низкомолекулярных веществ (масел, смол) в р-рах ПАВ - при наличии агрегатов (мицелл)
- 24. Скачать презентацию
Слайд 2
ПАВ’ы – это полимерные вещества, у которых каждая молекула
Слайд 2
ПАВ’ы – это полимерные вещества, у которых каждая молекула
одна группа – полярная, и следовательно притягивается к полярной поверхности – такой как вода ( + - ) т.е. это гидрофильная группа
другая группа – неполярная, гидрофобная-органофильная
это дает полимерная композиция, этих групп – получается целое семейство молекул симметрией гидрофобных и гидрофильных групп – меняющихся в рядах – повторяющихся.
Особые свойства молекул ПАВ: в растворах – это способность существовать (адсорбироваться) их на границе раздела гидрофобных и гидрофильных (например, М и В) поверхностей. Молекулы мостиком их (на поверхности) соединяют, снижая энергию системы (σ↓) граница раздела;
Нефть-вода ( углеводор. – вода), что позволяет получать капельки – эмульгирования: или неионообразования или газ-вода
Особые свойства ПАВ – способность молекул ПАВ: 1) существовать на границе раздела гидрофобных и гидрофильных поверхностей; 2) молекулы ПАВ, мостиком соединяющих эти поверхности; снижают поверхностное натяжение – энергию системы и делают ее стабильной
Слайд 3
Границы раздела двух фаз; которые модифицируются ПАВ’ом
(Примеры ПАВ в
Слайд 3
Границы раздела двух фаз; которые модифицируются ПАВ’ом
(Примеры ПАВ в
Строение молекул ПАВ
R → CnHm - у.в. радикал
органофильная часть
Слайд
Строение молекул ПАВ
R → CnHm - у.в. радикал
органофильная часть
Слайд
Cлайд 5
• алкильная группа в ПАВ’ах
Унивалентный радикал, имеющий общую формулу: СnH2n+1
-
Cлайд 5
• алкильная группа в ПАВ’ах
Унивалентный радикал, имеющий общую формулу: СnH2n+1
-
CH3 – метил
C2H5 – этил
CH3-(CH2)2 – пропил
(СH3)2 CH – изопропил
СН3 (СН2)3 – бутил
(СН3)2 СН СН2 – изобутил
Алкилирование – введение алкильной группы молекулы органического соединения, а так же получение алкильных производных химических элементов.
Или: алкилирование – введение в молекулы органических или неорганических соединений остатка насыщенного углеводорода алкила, например метила СН3 (метилированных), этила С2Н5 (этилированные) для получения высокооктанового топлива, ПАВ’ов, антиоксидантов (!)
Введения остатка ароматического углеводорода – арила напр фенила С6Н5 – это арилирование
Слайд 6
Классификация ПАВ
1 признак: характер водных растворов
1 группа: Спирты и
Слайд 6
Классификация ПАВ
1 признак: характер водных растворов
1 группа: Спирты и
Отражающие
- истинные молекулярные (10-7 – 10-8 см) дисперсные системы
- ПАВ раздроблены до отдельных молекул;
- адсорбционные слои не обладают особыми механическими свойствами, отличаются от свойств поверхности слоя;
- стабилизирующее действие обусловлено поверхностной активностью - Ϭ↓;
- ПАВ – препятствуют утончению пленки – замедляют ее разрыв – это стабилизаторы.
2 группа:
- растворимы в воде – с образованием коллоидных (10-5 – 10-7 см) и полуколлоидных (+ еще молекулярно дисперсные системы);
- высокодисперсные системы;
- состоят из агрегатов – множества молекул - мещеллярные агрегаты
- полуколлоидные растворы занимают промежуточное положение между истинным и коллоидным раствором;
- вызывают небольшое понижение Ϭ↓ воды;
- обладают высоким стабилизирующим действием – т.к адсорбционные слои имеют высокие механические свойства – покрывающих обе стороны двух сторонних пленок пузырьков (в эмульсиях) и пенах (ПГЖС)
- эти ПАВ – для получения устойчивых пен – в нефтепромысловой практике
- это в т.ч. эмульгаторы
Слайд 7
Классификация ПАВ по физико-химическому состоянию или по способности и
Слайд 7
Классификация ПАВ по физико-химическому состоянию или по способности и
1 группа – ионогенные ПАВ
- в растворах молекулы диссоциируют (распадаются) на два иона: анион и катион. Анион – большой и является носителем поверхностно – активных свойств;
- Представители:
- алкил сульфонаты – натриевая или калиевая соли ROSO2Me сульфо- эфиров высших жирных кислот (сульфоновой кислоты (ROSO2Н);
- натриевые и калиевые соли карбоновых кислот RCOO Me (мыла)
- Алкиларилсульфонаты RArSO2OMe;
Арил - общее название ароматических углеводородных остатков:
C6H5 – фенил; CH3C6H4 – толил; C10H7 – нартил
или : арильная группа:
остатков бензола C6H5
нафталина-нафтил C10H7
обозначают - Ar
алкиларил сульфонаты
C6H4OSO2Me
Me: Na+ или K+
C6H4OSO2Na соли сульфановых кислот
C6H4OSO2K
Фенил - ароматический углеводородный остаток - арил
Слайд 8
Другие анионные ПАВ
- Фторсодержащие – фтортензиды особые свойства:
Высокая поверхностная
Слайд 8
Другие анионные ПАВ
- Фторсодержащие – фтортензиды особые свойства:
Высокая поверхностная
Хемо- и термостойкость;
Высокая прочность связей C – F – через фтор-углеродные радикалы;
Обладают: низкой энергией межмолекулярного взаимодействия фторуглеродных цепей;
дорого стоят – не находят широкого применения;
Образуют устойчивые пены в углеводородных жидкостях;
Применяют для:
Удаления жидкости из газоконденсатных и нефтяных скважин;
КРС;
При добавлении к ПАВ’ам другим проявляют синергетический эффект- усиливается пенообразование.
Фторированные ПАВ – перфокарбоновые кислоты и их соли:
CnF2n+1 COOH
CnF2n+1 COOMe
- Фторалкилсульфонаты
CnF2n+1(CH2)mOSO2Na
- Перфтор соединения аммония
CnF2n+1(CF2)nCOONH4
- Высокомолекулярные (полимерные) ПАВ
Молекулы таких ПАВ состоят из большого числа повторяющихся звеньев, каждая из которых имеет полярные и неполярные группы
Молекулярная масса от 100000 до нескольких миллионов
Это (слабоанионные): - производные целлюлозы, КМЦ со полимеры аркиломида и акриловой кислоты
2 группа: катионные ПАВ
В растворах диссоциирует с образованием анионов и катионов поверхностной активностью обладает катионные группы
Представители Амины RNRlRllH+Х
и их первичные, вторичные и третичные алифатические и ароматические соли;
• моно и би четвертичные аммониевые соединения
RNRlRllRlll)+X
• оксиды аминов
RRlRllN+O-
Такие ПАВ:
- получают растворы на основе катионных ПАВ;
- это наиболее токсичные ПАВ;
- это наименее биологически разлагаемые ПАВ;
- применяют часто в качестве бактерицидов, дезинфицирующих веществ, ингибиторов коррозии;
- хорошие гидрофоби заторы горных пород;
- применяют в нефтедобыче;
- глинистые растворы коагулируются при определенной концентрации;
- уменьшают наработку глинистого раствора
Слайд 9
2 группа: неионогенные ПАВ
не диссоциируют в водных растворах. Их
Слайд 9
2 группа: неионогенные ПАВ
не диссоциируют в водных растворах. Их
К ним относятся:
- оксиэтилированные жирные
Спирты [RO(OCH2CH2)nH
и кислоты [R(OO(CH2CH2O)nH
- оксиэтилированные эфиры алкилфенолов ОП-4, ОП-7, ОП-10
- алкиламины и др.
n -степень оксиэтиллирования изменяется от нескольких единиц до 100 и выше
R- углеводородный (СnHm) радикал обычно содержит от 6 до 18 углеродных атомов (С6-С18)
Неионогенные ПАВ могут применяться в 1) любой среде кислой и щелочной, а так же 2) минерализованных растворах
Но: 1) наличие в составе ПАВ марки ОП полиоксиэтилированные эфира алкилфенолов, ароматического радикала (R) замедляет скорость разложения молекул, что ведет к накоплению их в обьектах ОПС
2) Однако неионогенные ПАВ с алкильными группами (CH2) биологически разлагаются быстро и полностью - оксиэтилированные жирные спирты RO(OCH2OH2)uH
3) Отсутствие ионогенных групп способствует повышению устойчивости вещества к действию солей, кислот и щелочей, как при нормальной так и при высокой температуре
Кроме того к этой группе относятся
- Кетоны RCORl
- Амины RNRlRll
-Эфиры ROR1
-уточнение - полиоксиэтиленовые эфиры алкилфенолов
СnH2n+1 C6H4OH(CH2CH2O)m где: С6Н4-фенил
(группа ОП-4, ОП-7, ОП-10) СН2 - алкил
Представители неионогенных ПАВ
-RCOOH - карбоновые кислоты
-ROH- спирты (например оксиэтилированные жирные спирты)
-полиоксиэтиленовые эфиры алкилфенолов
CnH2n+1C6H4OH(CH2CH2O)
к неионогенным ПАВ'ам
- в ПАВ (ОП)- (полиоксиэтилированных эфирах алкилфенолов) - есть ароматические радикалы R - замедляет скорость разложения и идет накопление в ОПС
R эфирный: CH2-CH2-O-CH2-CH2OH
- но в ПАВ'ах- оксиэтилированных спиртах и жирных кислотах
RO(OCH2CH2)nH
RCOO(OCH2CH2)nH
Состав нефти.
Нефть – сложная смесь углеводородов (различных классов) и неуглеводородных компонентов
Состав нефти.
Нефть – сложная смесь углеводородов (различных классов) и неуглеводородных компонентов
Элементный состав нефтей (min – max):
- углерод (83-87%);
-водород (12-14%);
-кислород
-сера (5-8%)
-азот
Сырые нефти – это неполярные и малополярные УВ:
-метановые – алканы или парафины;
-нафтеновые – цикланы;
-ароматические или гибридные УВ.
Кроме неполярных и малополярных УВ в нефтях содержатся полярные компоненты:
-определяют поверхностные и эмульгирующие свойства.
Слайд 10
Слайд 11
Виды ПАВ по происхождению:
Природные ПАВ
Нафтеновые кислоты (0,1-2%) в нефти:
Низкомолекулярные
Слайд 11
Виды ПАВ по происхождению:
Природные ПАВ
Нафтеновые кислоты (0,1-2%) в нефти:
Низкомолекулярные
- это карбоновые (RCOOH) кислоты с характерными для них реакциями замещения, в результате которых получаются соли:
Нафтенаты;
Комплексные соединения с аминами (амиды);
Сложные – это маслорастворимые ПАВ.
Смолы - молекулярно диспергированы в нефти, образуют ассоциаты молекул (не дают каллоидные структуры);
Асфальтены – коллоидная система в нефтях – это лиофильные коллоиды.
Для них характерно:
-сложная структура;
-низкая стабильность;
-высокая реакционная стабильность;
-полярность – т.е. ионогенный;
-поверхностная активность.
Синтетические ПАВ (СПАВ)
- которые получены синтетическим путем и вводят в состав
Синтетические ПАВ (СПАВ)
- которые получены синтетическим путем и вводят в состав
Применяют для:
-совершенствования процесса бурения;
-вскрытия продуктивных пластов;
-увеличения нефтеотдачи;
-обработки ПЗП;
-борьбы с осложнениями парафина;
-подготовки нефти;
-борьбы с последствиями аварийных разливов нефтей.
СПАВ – органические вещества, содержащие в молекуле УВ радикал и одну или несколько активных (полярных) групп. Чаще всего УВ радикал представлен:
Алкин CnH2n+1
Алкен CnH2n+1 – CHCnH2n
Алкинол
И др.
Функциональная в составе СПАВ (полярная) группа представлена:
-сульфогруппой SO3H
-нитрогруппой NO2
-карбоксильной COOH
-аминогруппой NH2
Роль функциональных групп могут выполнять также металлы (Me), галогены, кислород, азот, сера.
Слайд 12
Основные свойства растворов ПАВ, определяющие параметры пен (ГЖС).
К основным свойствам растворов
Основные свойства растворов ПАВ, определяющие параметры пен (ГЖС).
К основным свойствам растворов
Адсорбция
Поверхностное натяжение эти свойства определяют их
Мицеллообразование применяемость, например для ГЖС.
Эти свойства определяются растворимостью ПАВ.
Растворение – физико-химический процесс, который зависит в основном от следующих факторов:
- природы и местоположения гидрофильной группы – соотношениями между ГЛ и ГФ
- длины гидрофобной УВ цепи
- природы и положения группы гетероатомов: азот, кислород, сера с гидрофобной части молекул
-температура
-входящих в состав молекул катионов
Слайд 13
Влияние температуры на растворимость ПАВ
1) Ионогенные ПАВ – у большинства растворение
Влияние температуры на растворимость ПАВ
1) Ионогенные ПАВ – у большинства растворение
2) Неионогенные ПАВ – при увеличении температуры растворимость снижается – идет помутнение раствора – очевидно теплота (энергия) расходуется на образование агрегатов молекул – прозрачность уменьшается
-при увеличении длины углеводородной цепи растворимость снижается
-они диссоциируют, слабее взаимодействуют с молекулами воды, растворимость значительно ниже, чем у ионогенных.
Слайд 14
Растворимые в воде мыла (солей жирных кислот)
RCOONa, RCOOK, RCOOCa
и синтетические моющие
Растворимые в воде мыла (солей жирных кислот)
RCOONa, RCOOK, RCOOCa
и синтетические моющие
-образуют с ионом воды (например Н+) малодиссоциированную молекулу с частичным распадом в результате гидролиза на основание и кислоту:
RCOONa (мыло) + Н2О →(гидролиз)→NaOH + RCOOH (слабодис. жирная кислота)
В результате гидролиза удаляется Н+ , то остаются свободные гидроксилы ОН- - дает щелочную реакцию (Н+ - уменьшается в растворе)
Гидролиз – для мыла в водных растворах – важнейшая реакция, в результате которой образуются слабодиссоциированные молекулы RCOOH – жидкой кислоты.
В отличие от мыла синтетические моющие вещества (СМВ) являются солями сильной кислоты и сильного основания, поэтому либо вовсе не гидролизуются, либо гидролизуются при повышенной температуре и в сильно кислой среде.
Слайд 15
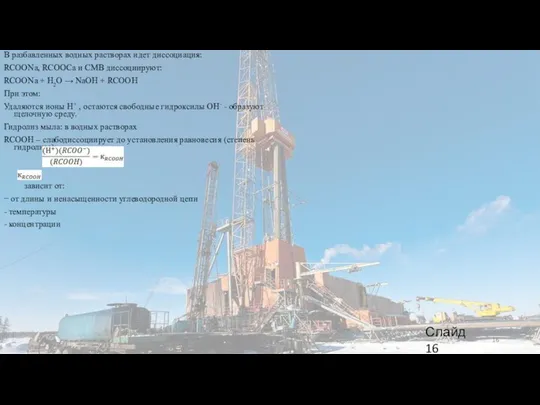
В разбавленных водных растворах идет диссоциация:
RCOONa, RCOOCa и СМВ диссоциируют:
RCOONa +
В разбавленных водных растворах идет диссоциация:
RCOONa, RCOOCa и СМВ диссоциируют:
RCOONa +
При этом:
Удаляются ионы Н+ , остаются свободные гидроксилы ОН- - образуют щелочную среду.
Гидролиз мыла: в водных растворах
RCOOH – слабодиссоциирует до установления равновесия (степень гидролиза):
зависит от:
− от длины и ненасыщенности углеводородной цепи
- температуры
- концентрации
Слайд 16
2. Мицеллообразование
Водные растворы ПАВ при определенной концентрации резко изменяют многие
2. Мицеллообразование
Водные растворы ПАВ при определенной концентрации резко изменяют многие
Поверхностное натяжение
Электропроводность
Осмотическое давление
Плотность
Моющая способность
Пенообразующие свойства
Эмульгирующие свойства и др.
СККМ концентрация, при которой происходит резкое изменение свойств растворов, соответствует критической концентрации мицелообразования ККМ, выше которой в растворе самопроизвольно протекают процессы образование мицелл и истинный раствор переходит в ультранней
гетерогенную систему – золь (изменение структуры растворов в них наряду с простыми ионами и молекулами истинный р-ра образуются коллоидные агрегат – мицеллы.
Слайд 17
В водной среде: ассоциация дифильных молекул ПАВ происходит в результате гидрофобного
В водной среде: ассоциация дифильных молекул ПАВ происходит в результате гидрофобного
В неполярной (углеводородной) среде происходит формирование обращенных мицелл с гидрофобным поверхностным слоем.
Слайд 18
При достижении определенной концентрации сферические мицеллы начинают взаимодействовать между собой ,
При достижении определенной концентрации сферические мицеллы начинают взаимодействовать между собой ,
Введение электролитов в раствор ионогенных ПАВ способствует снижению ККМ↓ и облегчает мицеллообразование Сккм↓
В растворах неионогенных ПАВ’ах из-за электронейтральных молекул добавки солей слабо влияют на ККМ.
Слайд 19
гидрофильно липофильный баланс – ГЛБ
ГЛБ=Σ(ГЛБ)г - Σ(ГЛБ)л+7
Физический смысл - это отношение
гидрофильно липофильный баланс – ГЛБ
ГЛБ=Σ(ГЛБ)г - Σ(ГЛБ)л+7
Физический смысл - это отношение
Молекула ПАВ - содержит УВ радикал и одну или несколько активных (полярных) групп.
УВ радикал – чаще всего представлен;
Алкин СnH2n+1
Алкен СnH2n+1-CHCnH2n
Алкин и др.
метод определения ГЛБ числа – метод Гриффится – основан на сравнении способность ПАВ образовывать устойчивые эмульсии типа В/М или М/В чем выше число ГЛБ, тем выше гидрофильность
Слайд 20
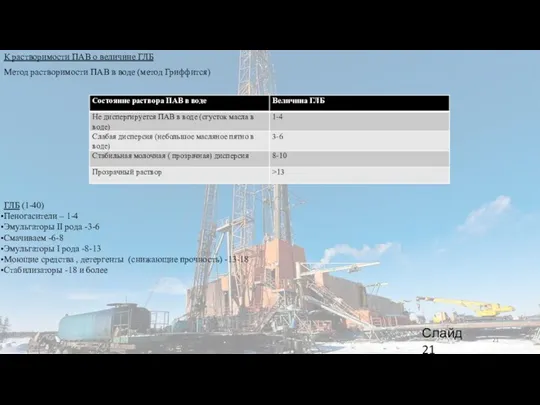
К растворимости ПАВ о величине ГЛБ
Метод растворимости ПАВ в воде (метод
К растворимости ПАВ о величине ГЛБ
Метод растворимости ПАВ в воде (метод
Слайд 21
ГЛБ (1-40)
Пеногасители – 1-4
Эмульгаторы II рода -3-6
Смачиваем -6-8
Эмульгаторы I рода -8-13
Моющие средства , детергенты (снижающие прочность) -13-18
Стабилизаторы -18 и более
Самобилизация – коллоидное растворение низкомолекулярных веществ (масел, смол) в р-рах ПАВ
Самобилизация – коллоидное растворение низкомолекулярных веществ (масел, смол) в р-рах ПАВ
- при наличии агрегатов (мицелл) из молекул ПАВ
- молекулы масла проникают внутри мицелаучных агрегатов – взаимоидействуя с липофильной частью молекул ПАВ – растворения масла в водном р-ре ПАВ
- признак растворения (солюбилизации) – прозрачный раствор.
самобилизация – самопроизвольный и обратимое проникновение какого-либо низкомолекулярных веществ, слаборастворимый в данной среде внутри мицеллярных агрегатов.
Слайд 22


















 Історія створення і виробництво мила
Історія створення і виробництво мила  Введение в нефтепереработку. Переработка нефти и газа
Введение в нефтепереработку. Переработка нефти и газа Веселый химический КВН
Веселый химический КВН Фотохимические процессы
Фотохимические процессы Углерод и 4 группа
Углерод и 4 группа Цеолиты. Свойства и область применения
Цеолиты. Свойства и область применения Основные характеристики ковалентной связи
Основные характеристики ковалентной связи Растворы электролитов. Буферные растворы. Лекция 4
Растворы электролитов. Буферные растворы. Лекция 4 Соединения азота. Оксиды азота
Соединения азота. Оксиды азота Химическая физика горения
Химическая физика горения Условие фазового равновесия. Правило фаз Гиббса
Условие фазового равновесия. Правило фаз Гиббса Гидролиз
Гидролиз Кислородосодержащие органические соединения (2 часть)
Кислородосодержащие органические соединения (2 часть) Нанокомпозиционный материал на основе фенолоформальдегидной смолы, эпоксидной смолы, полистирола
Нанокомпозиционный материал на основе фенолоформальдегидной смолы, эпоксидной смолы, полистирола Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно
Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно Растворение. Растворяемость. Типы растворов
Растворение. Растворяемость. Типы растворов Основные типы химических реакций
Основные типы химических реакций Презентация по химии Классы неорганических веществ
Презентация по химии Классы неорганических веществ Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Свинец
Свинец Итоговая консультация. Формульный диктант
Итоговая консультация. Формульный диктант Изотопы Подготовила Кузнецова Даша
Изотопы Подготовила Кузнецова Даша  Ферменты в пищевой промышленности
Ферменты в пищевой промышленности Нітрати – токсичні речовини
Нітрати – токсичні речовини  Урок по химии в 10 классе: «Кислород и сера» подготовил учитель химии и биологии ГУО СШ №163 г.Минска Костюкевич Юрий Михайлович
Урок по химии в 10 классе: «Кислород и сера» подготовил учитель химии и биологии ГУО СШ №163 г.Минска Костюкевич Юрий Михайлович Визначення орбіталей та можливість їх існування
Визначення орбіталей та можливість їх існування Карбоновые кислоты. Гидрокси-, оксокислоты. Лекция 2
Карбоновые кислоты. Гидрокси-, оксокислоты. Лекция 2 Биохимия печени
Биохимия печени