Содержание
- 2. Для получения зачета и успешной сдачи экзамена следует Посещать лекции, конспектировать материал лекций и просматривать его
- 3. Основные положения рейтинговой системы Работа в семестре оценивается 50 баллами: Зачет получают студенты, отработавшие все лабораторные
- 4. 1. Глинка Л.Н. Общая химия, М., Интеграл - пресс, 2000 2. Глинка Л.Н. Задачи и упражнения
- 5. Предмет химии. Основные задачи курса Химия - наука о свойствах веществ и их превращениях. Она включает
- 6. Тема 1. Основные понятия химии. Стехиометрические законы
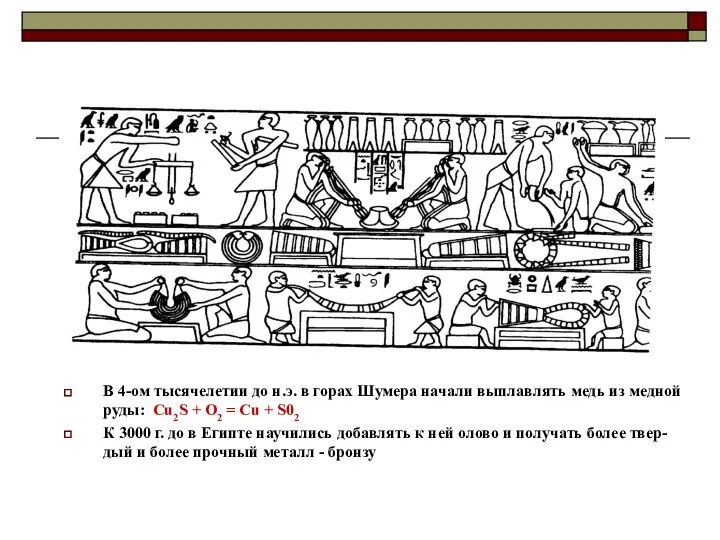
- 7. В 4-ом тысячелетии до н.э. в горах Шумера начали выплавлять медь из медной руды: Cu2S +
- 8. Примерно к 1500 г. до н.э. В малой Азии был открыт секрет плавки железа: 2С +
- 9. Главной задачей средневековых алхимиков было превращение неблагородных металлов в золото
- 10. Антуан Лоран Лавуазье (1743 -1794) 1772 г. -открыл кислород 1789 г. - открыл закон сох-ранения массы
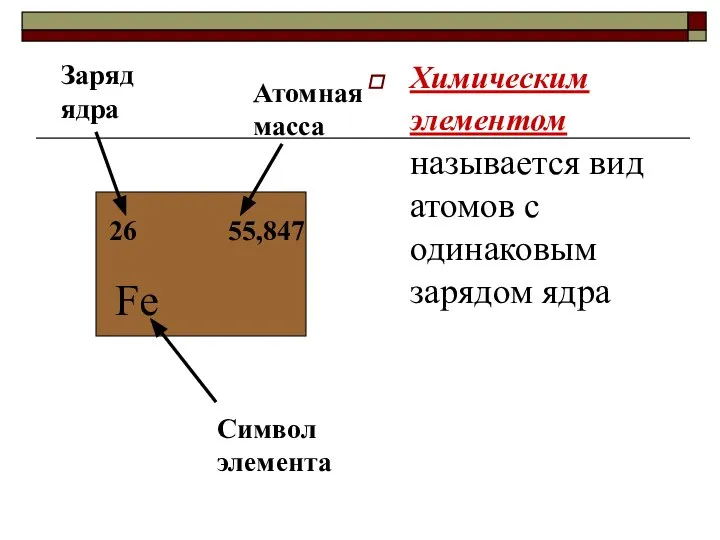
- 11. Химическим элементом называется вид атомов с одинаковым зарядом ядра 26 Fe 55,847 Атомная масса Заряд ядра
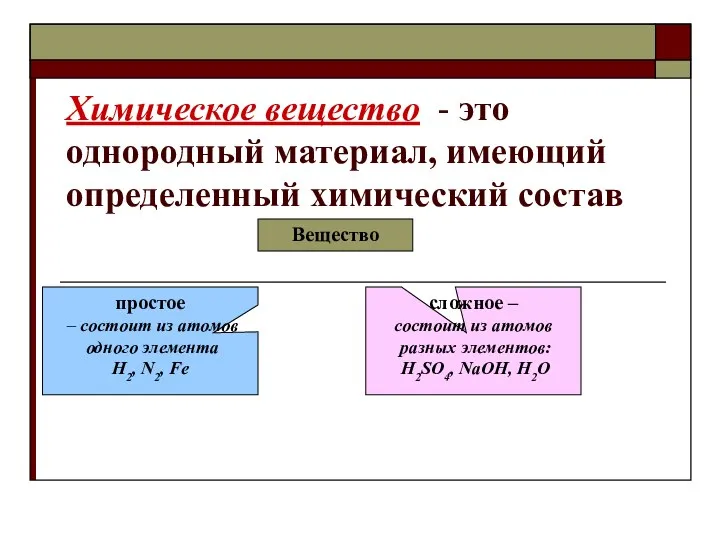
- 12. Химическое вещество - это однородный материал, имеющий определенный химический состав Вещество простое – состоит из атомов
- 13. Михаил Васильевич Ломоносов (1711 - 1765) 1741 г.-сформулировал ос-новные положения корпус-кулярной теории строения вещества 1748 г
- 14. Закон сохранения массы вещества (Ломоносов - Лавуазье, 1756 - 1789) Fe + O2 → Fe2O3 56
- 15. Закон постоянства состава (Жозеф Луи Пруст, 1799) Каждое химическое соединение независимо от способа его получения имеет
- 16. Закон кратных отношений (Дж. Дальтон, 1803 г.) Если два элемента образуют друг с другом несколько химических
- 17. Атом - мельчайшая частица элемента, являющаяся носителем его химических свойств. Атомная масса - масса одного атома.
- 18. Молекула - мельчайшая частица химического вещества, обладающая его химическими свойствами Молекулы всех газов, кроме инертных, и
- 19. Моль - количество вещества, которое содержит столько молекул (атомов), сколько атомов содержится в 12 г изотопа
- 20. Эквивалент - количество вещества, которое химически равноценно 1 молю атомов или ионов водорода, то есть которое
- 21. Закон эквивалентов (В. Рихтер, 1783 г) Вещества взаимодействуют друг с другом и образуются в результате реакций
- 22. Закон объемных отношений (Ж.Гей-Люссак, 1805 г) При одинаковых условиях объемы вступающих в реакцию газов, относятся друг
- 24. Скачать презентацию


















 Законы химической термодинамики. Часть 1. Физическая и коллоидная химия
Законы химической термодинамики. Часть 1. Физическая и коллоидная химия Chemical Reactions and Stoichiometry
Chemical Reactions and Stoichiometry Азот Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов» Барсук
Азот Составил: учитель химии МОУ «Средняя общеобразовательная школа №92 с углубленным изучением отдельных предметов» Барсук 1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки
1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки  Наука плазмохимия
Наука плазмохимия Этимология названий химических элементов периодической системы Д.И. Менделеева
Этимология названий химических элементов периодической системы Д.И. Менделеева Основания. Гидроксид лития
Основания. Гидроксид лития Основы химической кинетики и химическое равновесие (лекция 5)
Основы химической кинетики и химическое равновесие (лекция 5) Глюкозаальдегидоспирт
Глюкозаальдегидоспирт Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения
Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения Строение вещества
Строение вещества Полимеры. Классификация полимеров
Полимеры. Классификация полимеров Презентация по Химии "Свойства комплексных соединений" - скачать смотреть
Презентация по Химии "Свойства комплексных соединений" - скачать смотреть  Практикум по органической и биоорганической химии
Практикум по органической и биоорганической химии Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена
Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена Аттестационная работа. Образовательная программа кружка «Химия и жизнь»
Аттестационная работа. Образовательная программа кружка «Химия и жизнь» Признаки и условия протекания химических реакций
Признаки и условия протекания химических реакций Беймет алдар
Беймет алдар АЛЮМІНІЄВІ СПЛАВИ Підготувала учениця 10 класу Кисленко Єлизавета
АЛЮМІНІЄВІ СПЛАВИ Підготувала учениця 10 класу Кисленко Єлизавета  Коррозия металлов
Коррозия металлов The morphology and reactivity of model catalysts based on cobalt oxide
The morphology and reactivity of model catalysts based on cobalt oxide Классификация и номенклатура органических соединений
Классификация и номенклатура органических соединений Методы изготовления из резины и латекса
Методы изготовления из резины и латекса Чи шкідливі пральні порошки для здоров’я?
Чи шкідливі пральні порошки для здоров’я?  Виды химических реакций
Виды химических реакций Соединения химических элементов
Соединения химических элементов Concise asymmetric total synthesis of lycopodine
Concise asymmetric total synthesis of lycopodine