Содержание
- 2. За кількістю функціональних груп: моноаміномонокарбоновие діаміномонокарбоновие С-С-С-С-С -СООН ׀ ׀ NH2 NH2 лизин За взаємною розташуванням
- 3. Властивості : 1) Розчинність у воді N+H3 – CH – COOH N+H3 – CH – COO
- 4. лабораторний оцтова кислота → хлоруксусна кислота → амінооцтова кислота СН3-СООН + Сl2 → СН2-СООН | Cl
- 6. Скачать презентацию
Слайд 2
За кількістю функціональних груп:
моноаміномонокарбоновие
діаміномонокарбоновие С-С-С-С-С -СООН
׀ ׀
NH2 NH2 лизин
За
моноаміномонокарбоновие
діаміномонокарбоновие С-С-С-С-С -СООН
׀ ׀
NH2 NH2 лизин
За
взаємною розташуванням функціональних груп :
α , β , γ…
С – С- С – С – СООН С – С- С – С – СООН С – С- С – С – СООН
| | |
NH2 NH2 NH2
α , β , γ…
С – С- С – С – СООН С – С- С – С – СООН С – С- С – С – СООН
| | |
NH2 NH2 NH2
2, 6 – діаміногексанова кислота
моноамінодікарбонові НООС-С-С-С-СООН
|
NH2
глутамінова
2-амінопентандіова кислота
Слайд 3
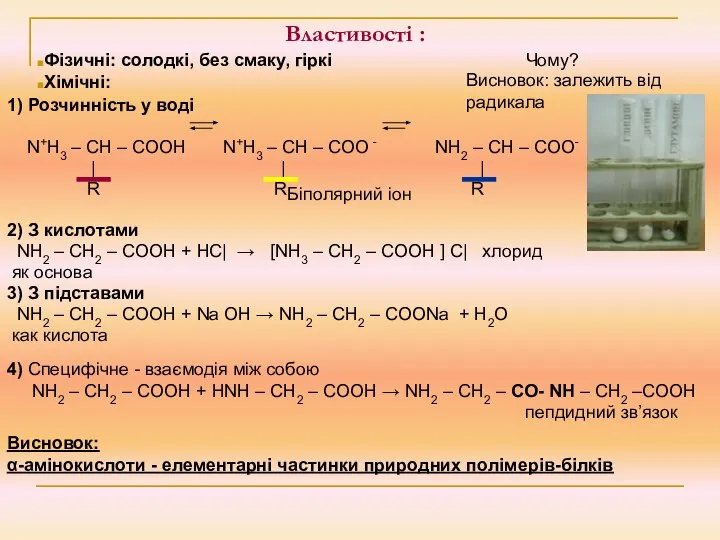
Властивості :
1) Розчинність у воді
N+H3 – CH – COOH
Властивості :
1) Розчинність у воді
N+H3 – CH – COOH
N+H3 – CH – COO - NH2 – CH – COO-
| | |
R R R
2) З кислотами
NH2 – CH2 – COOH + НС| → [NH3 – CH2 – COOH ] С| хлорид
як основа
3) З підставами
NH2 – CH2 – COOH + Na OH → NH2 – CH2 – COONa + H2O
как кислота
| | |
R R R
2) З кислотами
NH2 – CH2 – COOH + НС| → [NH3 – CH2 – COOH ] С| хлорид
як основа
3) З підставами
NH2 – CH2 – COOH + Na OH → NH2 – CH2 – COONa + H2O
как кислота
Фізичні: солодкі, без смаку, гіркі
Чому?
Висновок: залежить від радикала
4) Специфічне - взаємодія між собою
NH2 – CH2 – COOH + НNH – CH2 – COOH → NH2 – CH2 – CO- NH – CH2 –COOH
пепдидний зв’язок
Висновок:
α-амінокислоти - елементарні частинки природних полімерів-білків
Біполярний іон
Хімічні:
Слайд 4
лабораторний
оцтова кислота → хлоруксусна кислота → амінооцтова кислота СН3-СООН +
лабораторний
оцтова кислота → хлоруксусна кислота → амінооцтова кислота СН3-СООН +
Сl2 → СН2-СООН
|
Cl
СН2-СООН + NH3 → СН2-СООН
| |
Сl NH2
|
Cl
СН2-СООН + NH3 → СН2-СООН
| |
Сl NH2
способи отримання
гідроліз білків
промисловий :


 Органічні сполуки в побуті
Органічні сполуки в побуті  защита от коррозии
защита от коррозии Аттестационная работа. Групповой урочный проект Кислородсодержащие органические вещества
Аттестационная работа. Групповой урочный проект Кислородсодержащие органические вещества Железо как химический элемент. Нахождение в природе и применение железа
Железо как химический элемент. Нахождение в природе и применение железа Ионообменная хроматография: классический и высокоэффективные методы
Ионообменная хроматография: классический и высокоэффективные методы Избранные главы органической стереохимии
Избранные главы органической стереохимии Углеводы
Углеводы Синтез оксида меди и йодида меди для формирования буферных слоев для ГОНП
Синтез оксида меди и йодида меди для формирования буферных слоев для ГОНП Непредельные углеводороды.
Непредельные углеводороды.  Натрийуретические пептиды
Натрийуретические пептиды Ионный обмен. Хроматография
Ионный обмен. Хроматография Химический элемент Алюминий
Химический элемент Алюминий Использование газового топлива
Использование газового топлива Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Определение химии, как науки
Определение химии, как науки Графен. Нобелевская премия 2016
Графен. Нобелевская премия 2016 Адсорбция
Адсорбция Комплексные соединения
Комплексные соединения Побочная подгруппа VIII группы периодической системы
Побочная подгруппа VIII группы периодической системы Практическое применение метанола
Практическое применение метанола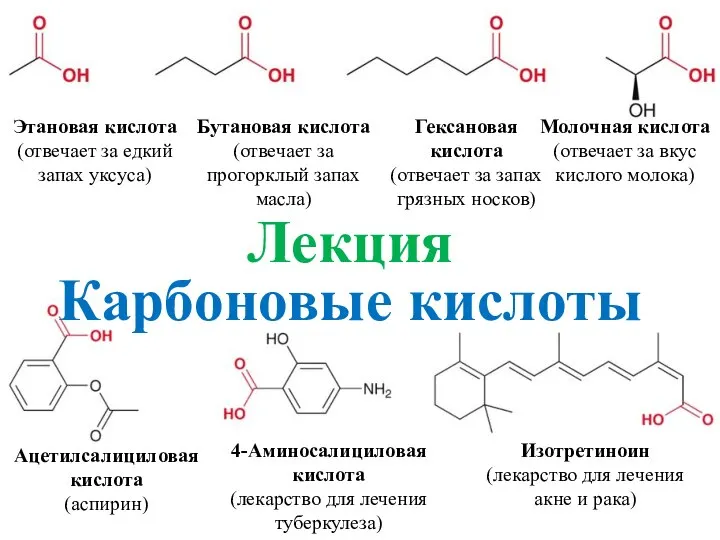 Этановая кислота Бутановая кислота
Этановая кислота Бутановая кислота Этилен. Углеводороды ряда этилена
Этилен. Углеводороды ряда этилена Общая геохимия. Атомная и молекулярная масса. Представление результатов аналитических исследований
Общая геохимия. Атомная и молекулярная масса. Представление результатов аналитических исследований Алкины Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна
Алкины Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна Автор: Ким Н. В. учитель химии МОУСОШ №6 г. Нягани
Автор: Ким Н. В. учитель химии МОУСОШ №6 г. Нягани Оксиген як хімічний елемент
Оксиген як хімічний елемент Растворы. Способы выражения состава раствора
Растворы. Способы выражения состава раствора Функциональная роль p53 в регуляции окислительного стресса
Функциональная роль p53 в регуляции окислительного стресса