Итоги исследований
В результате исследований Ф. Габеру удалось обобщить сведения об
этой реакции и подобрать условия для ее промышленного проведения.
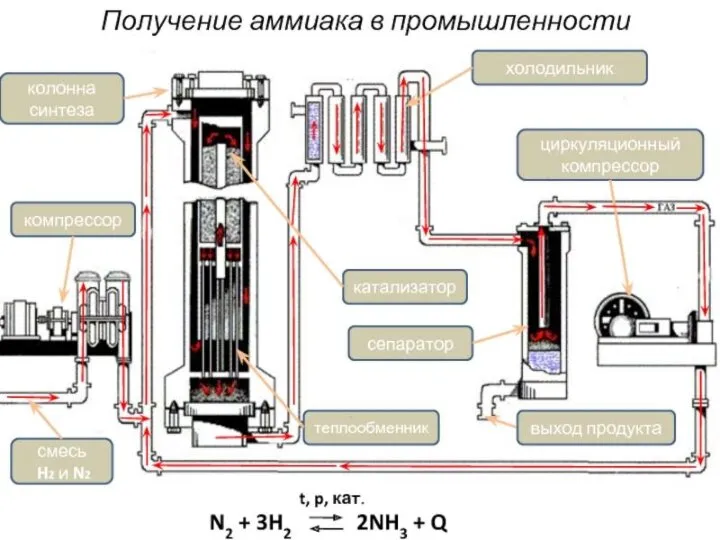
Массовое производство аммиака началось в канун первой мировой войны благодаря К. Бошу, химику – технологу предприятия «BASF». На первых установках синтез проводили под давлением 20 МПа, при температуре 5000C на осмиевом (Оs) катализаторе. А чтобы повысить выход аммиака, было предложено возвращать не прореагировавшею азотоводородную смесь обратно в реакционный аппарат.
Установка для промышленного производства аммиака, разработанная Ф. Габером и К. Бошем.







 Гидролиз. Сущность процесса гидролиза
Гидролиз. Сущность процесса гидролиза Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения Кругообіг Нітрогену
Кругообіг Нітрогену  Химические реактивы
Химические реактивы Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М
Спирты: классификация, изомерия, номенклатура Подготовила учитель химии Несмеянова М.В. МОУ «Сытьковская СОШ»Рузский район М Сложные эфиры. 10 класс
Сложные эфиры. 10 класс Алканы. Алкены. Алкины. Задачи урока:
Алканы. Алкены. Алкины. Задачи урока:  Теория резонанса в неорганической химии
Теория резонанса в неорганической химии Пищевые красители
Пищевые красители Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_
Презентация по Химии "Классификация реакций в неорганической химии." - скачать смотреть бесплатно_ «Уксусная кислота»
«Уксусная кислота»  Физико-химическая и механическая миграция
Физико-химическая и механическая миграция Титан. Структура, применение, свойства (11 класс)
Титан. Структура, применение, свойства (11 класс)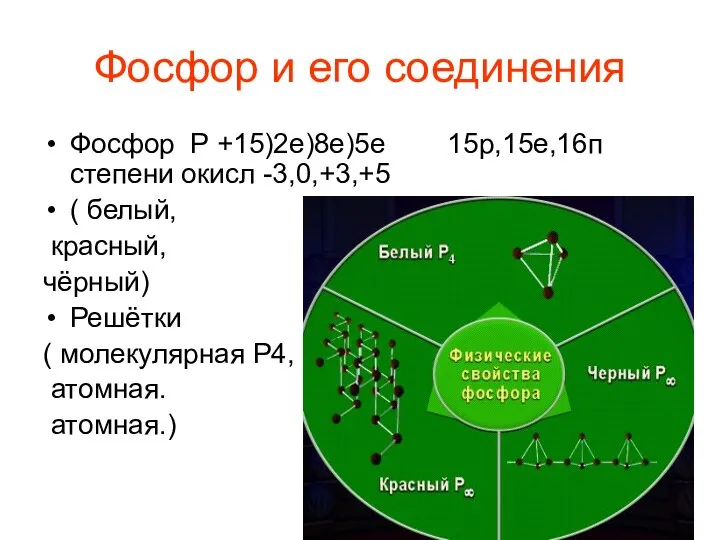 Фосфор и его соединения
Фосфор и его соединения Исследование процесса диффузии на примере движения частиц в жидкостях и газах
Исследование процесса диффузии на примере движения частиц в жидкостях и газах Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Электрометрические методы анализа ЛВ. Термографические методы
Электрометрические методы анализа ЛВ. Термографические методы Янтарь – солнечный камень. Рассказ об удивительном минерале
Янтарь – солнечный камень. Рассказ об удивительном минерале Фармацевтические суспензии и эмульсии
Фармацевтические суспензии и эмульсии Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Галогены: Хлор, бром, иод
Галогены: Хлор, бром, иод Классификация и номенклатура органических соединений
Классификация и номенклатура органических соединений Введение в обмен веществ. Метаболические пути
Введение в обмен веществ. Метаболические пути Залежність фізичних властивостей речовин від типу кристалічних ґраток
Залежність фізичних властивостей речовин від типу кристалічних ґраток Тема урока "Круговорот углерода в природе и последствия его нарушения« Учитель биологии Рабаданова Светлана Ивановна МОУ Лиц
Тема урока "Круговорот углерода в природе и последствия его нарушения« Учитель биологии Рабаданова Светлана Ивановна МОУ Лиц Қызықты химия
Қызықты химия Основы химической кинетики
Основы химической кинетики Трансформация энергии в процессе оксигенного фотосинтеза
Трансформация энергии в процессе оксигенного фотосинтеза