Содержание
- 2. Растворы – это гомогенные (однородные) системы, состоящие из двух и более компонентов и продуктов их взаимодействия.
- 3. Растворы подразделяются: Молекулярные – водные растворы неэлектролитов ( спиртовой раствор иода, раствор глюкозы). Молекулярно-ионные – растворы
- 4. Растворение – физико – химический процесс, в котором наряду с образованием обычной механической смеси веществ идет
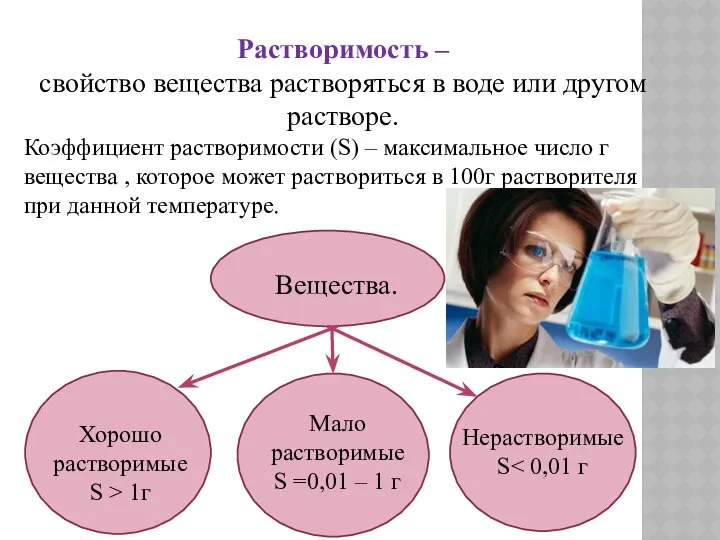
- 5. Растворимость – свойство вещества растворяться в воде или другом растворе. Коэффициент растворимости (S) – максимальное число
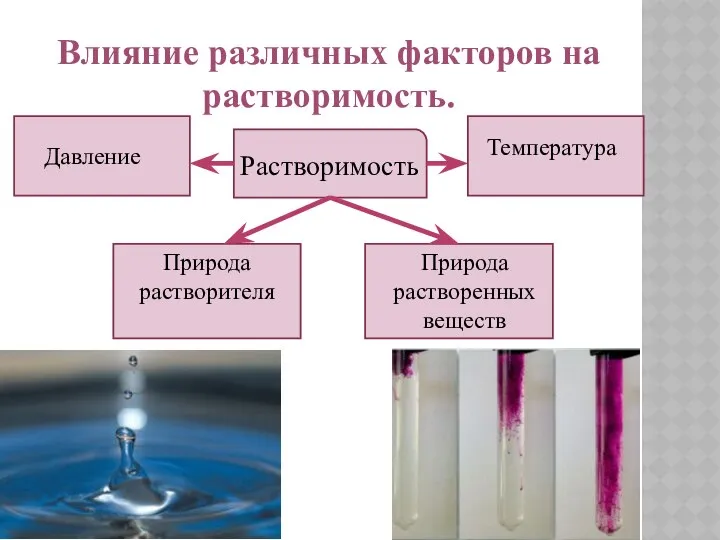
- 6. Влияние различных факторов на растворимость. Растворимость Температура Давление Природа растворенных веществ Природа растворителя
- 7. Концентрация раствора – это содержание вещества в определенной массе или объеме раствора.
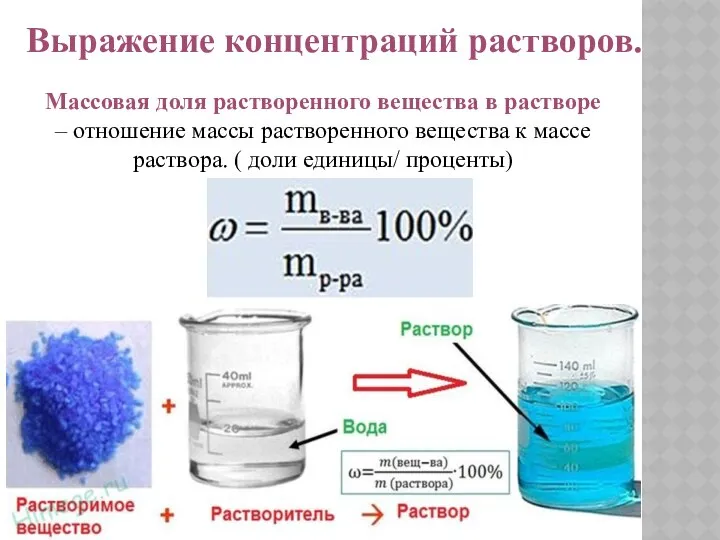
- 8. Выражение концентраций растворов. Массовая доля растворенного вещества в растворе – отношение массы растворенного вещества к массе
- 9. Выражение концентраций растворов. Молярность - число молей растворенного вещества в 1 л раствора. ʋ - количество
- 10. Выражение концентраций растворов. Эквивалентная концентрация (нормальность) – число эквивалентов растворенного вещества в 1л раствора. ʋ экв.
- 11. Выражение концентраций растворов. Моляльная концентрация (моляльность) – число молей растворенного вещества на 1000 г растворителя.
- 12. Природные растворы. Минеральная вода. Кровь животных. Морская вода.
- 14. Скачать презентацию








 Изопроцессы в идеальном газе
Изопроцессы в идеальном газе Технологія жирів і жирозамінників
Технологія жирів і жирозамінників Смеси и растворы
Смеси и растворы Термодинамика поверхностных явлений. (Часть 2)
Термодинамика поверхностных явлений. (Часть 2) Ароматические соединения. Галогенпроизводные
Ароматические соединения. Галогенпроизводные Химическое образование в современной средней (полной) общеобразовательной школе
Химическое образование в современной средней (полной) общеобразовательной школе معطر الجو(الهواء) يستعمل معطر الجو لتلطيف الرائحة االستعمال للحمامات او الغرف
معطر الجو(الهواء) يستعمل معطر الجو لتلطيف الرائحة االستعمال للحمامات او الغرف Промышленный биокатализ
Промышленный биокатализ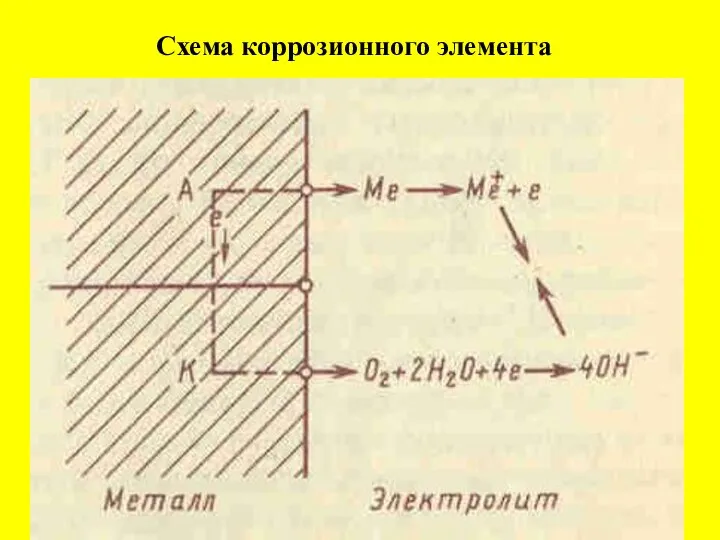 Схема коррозионного элемента
Схема коррозионного элемента Строение атома фосфора. Строение оксида фосфора (V) и его физические свойства
Строение атома фосфора. Строение оксида фосфора (V) и его физические свойства Физические основы методов анализа вещества
Физические основы методов анализа вещества Ванадатты фосфаттар. Орынбасар фосфаттар. Төменгі оксоқышқылдар
Ванадатты фосфаттар. Орынбасар фосфаттар. Төменгі оксоқышқылдар Мұнай
Мұнай Всем известно, всем понятно, что здоровым быть приятно!
Всем известно, всем понятно, что здоровым быть приятно! Алкины. Ацетилен
Алкины. Ацетилен Периодический закон Менделеева и периодическая система химических элементов
Периодический закон Менделеева и периодическая система химических элементов  Предмет и задачи фармацевтической химии. Общие методы анализа лекарственных средств неорганической природы согласно ГФУ
Предмет и задачи фармацевтической химии. Общие методы анализа лекарственных средств неорганической природы согласно ГФУ Поливинилацетат
Поливинилацетат Анализ физико-химических свойств синтетических моющих средств (СМС) и их значение в жизни человека
Анализ физико-химических свойств синтетических моющих средств (СМС) и их значение в жизни человека Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым Изменения, происходящие с белками в процессах технологической переработки сырья
Изменения, происходящие с белками в процессах технологической переработки сырья Карбоновые кислоты. Гидрокси-, оксокислоты. Лекция 2
Карбоновые кислоты. Гидрокси-, оксокислоты. Лекция 2 Интегрированный урок История+Химия
Интегрированный урок История+Химия Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? Термодинамика. 2 закон термодинамики. Энтропия
Термодинамика. 2 закон термодинамики. Энтропия Элективный курс по химии «Лаборатория юных химиков» Для учащихся 8 класса Разработала учитель химии МОУ СОШ №3 Звёздочкина С.А.
Элективный курс по химии «Лаборатория юных химиков» Для учащихся 8 класса Разработала учитель химии МОУ СОШ №3 Звёздочкина С.А. Электрохимические методы. (Лекция 3)
Электрохимические методы. (Лекция 3) «Соединения химических элементов»
«Соединения химических элементов»