Содержание
- 2. 1. Предмет электрохимии. Электролиты Электрохимия – раздел физической химии, который рассматривает законы взаимного превращения химической и
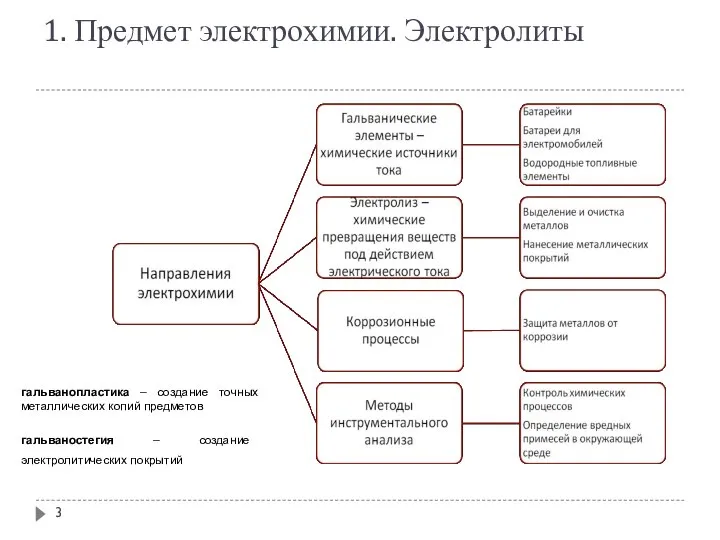
- 3. 1. Предмет электрохимии. Электролиты гальванопластика – создание точных металлических копий предметов гальваностегия – создание электролитических покрытий
- 4. 1.1 Особенности электрохимических систем Электрохимические системы (электрохимические цепи) – системы, в которых протекают электрохимические реакции. Электрический
- 5. 1.1 Особенности электрохимических систем
- 6. 29.01.17
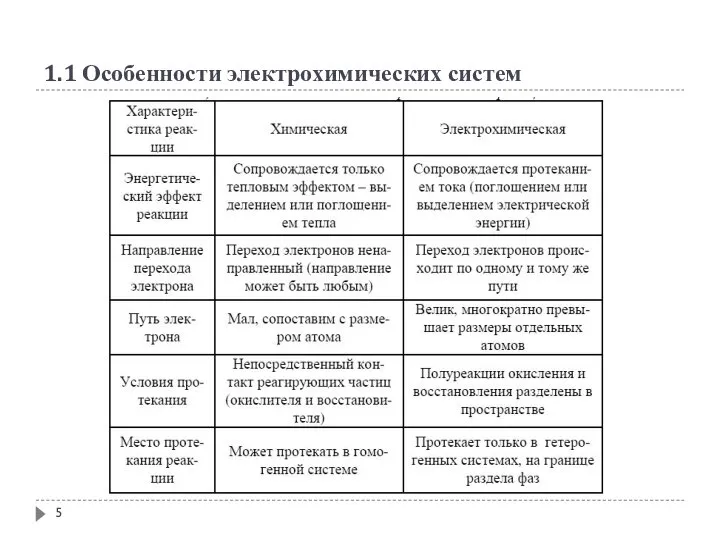
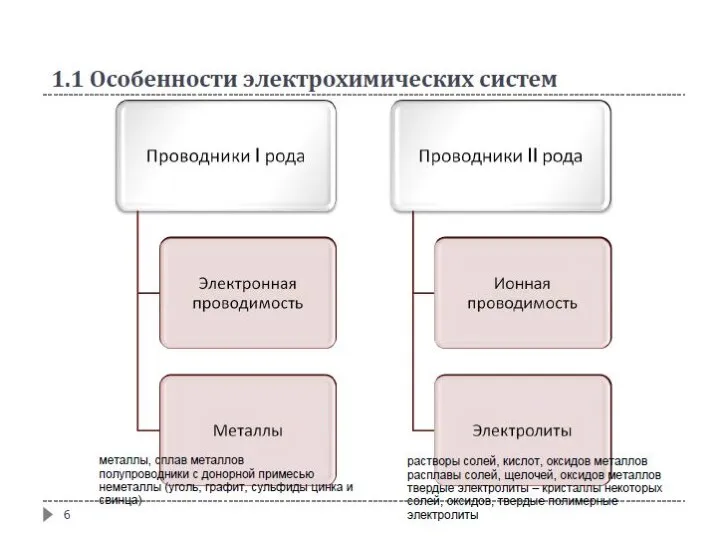
- 7. 1.1 Особенности электрохимических систем
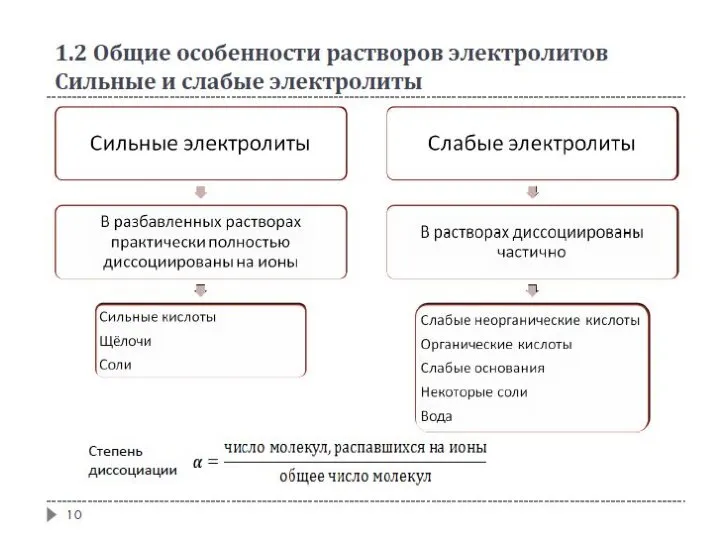
- 8. 1.2 Общие особенности растворов электролитов Электролиты - вещества или системы, содержащие в заметных количествах ионы и
- 9. 1.2 Общие особенности растворов электролитов
- 11. 1.2 Общие особенности растворов электролитов Изотонический коэффициент Вант-Гоффа Расчёт коллигативных свойств растворов электролитов Изотонический коэффициент -
- 13. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Влияние характеристик вещества
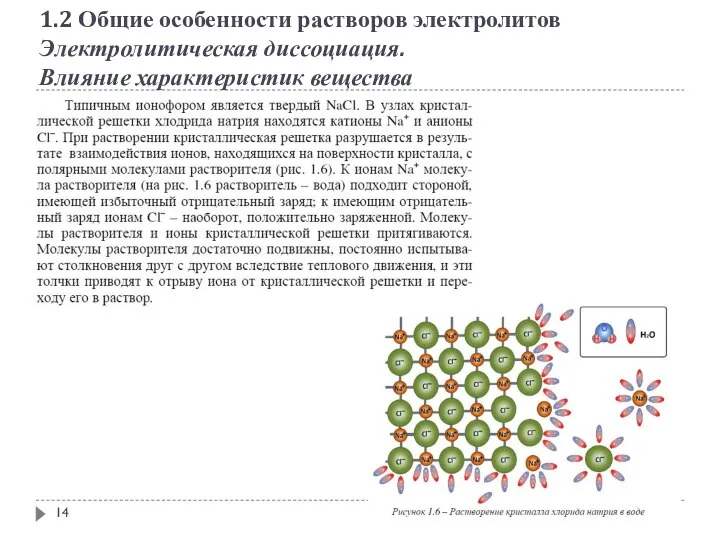
- 14. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Влияние характеристик вещества
- 15. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Влияние характеристик вещества
- 16. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Влияние характеристик растворителя
- 17. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Влияние характеристик растворителя
- 18. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Сольватация (гидратация)
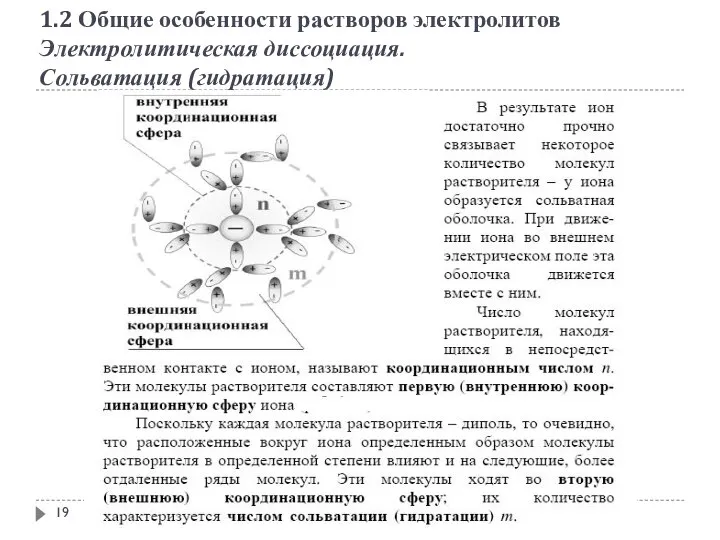
- 19. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Сольватация (гидратация)
- 20. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Термины электрохимии Электролиты разделяют на бинарные, молекула которых диссоциирует
- 21. 1.2 Общие особенности растворов электролитов Электролитическая диссоциация. Термины электрохимии
- 22. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины
- 23. В растворах электролитов происходит электростатическое взаимодействие между ионами, а также ионов и молекул электролита с молекулами
- 24. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины Активность
- 25. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины
- 26. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины
- 27. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины
- 28. Средняя моляльная концентрация Если диссоциацию электролита выразить уравнением то средняя моляльная концентрация ионов электролита определится как
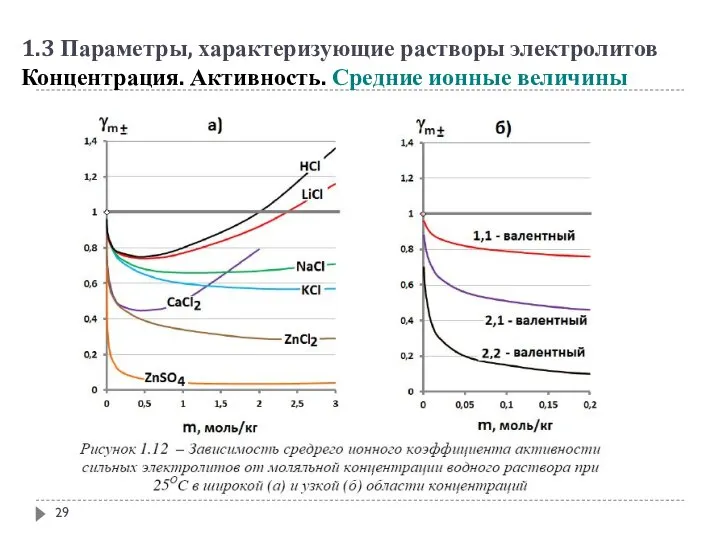
- 29. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины
- 30. 1.3 Параметры, характеризующие растворы электролитов Концентрация. Активность. Средние ионные величины
- 31. 1.3 Параметры, характеризующие растворы электролитов Ионная сила. Правило ионной силы
- 32. 1.3 Параметры, характеризующие растворы электролитов Ионная сила. Правило ионной силы
- 33. 1.3 Параметры, характеризующие растворы электролитов Ионная сила. Правило ионной силы
- 34. 1.3 Параметры, характеризующие растворы электролитов Изотонический коэффициент
- 35. 1.3 Параметры, характеризующие растворы электролитов Изотонический коэффициент
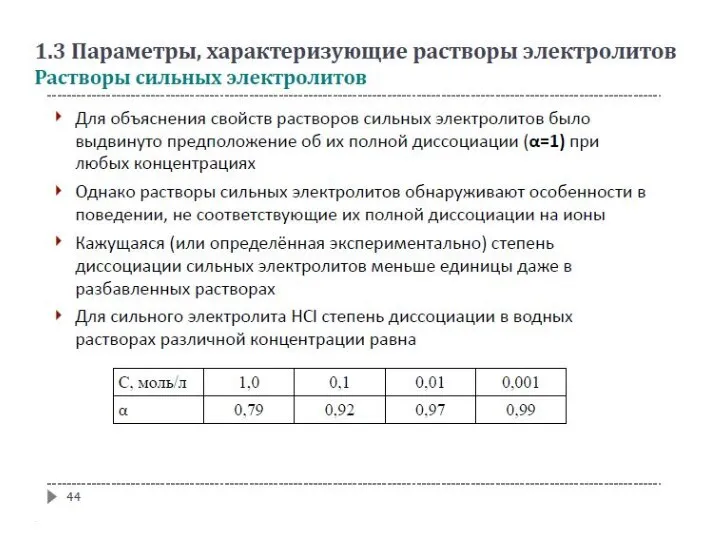
- 36. 1.3 Параметры, характеризующие растворы электролитов Степень диссоциации. Сильные и слабые электролиты
- 37. 1.3 Параметры, характеризующие растворы электролитов Теория слабых электролитов (Теория Аррениуса)
- 38. 1.3 Параметры, характеризующие растворы электролитов Теория слабых электролитов. Константа диссоциации
- 39. 1.3 Параметры, характеризующие растворы электролитов Теория слабых электролитов. Константа диссоциации
- 40. 1.3 Параметры, характеризующие растворы электролитов Теория слабых электролитов. Закон разведения Оствальда Для бинарных электролитов концентрация анионов
- 41. 1.3 Параметры, характеризующие растворы электролитов Теория слабых электролитов. Закон разведения Оствальда
- 42. Принцип Ле Шателье-Брауна При введении в раствор электролита ионов произойдёт сдвиг равновесия диссоциации влево (т.е. в
- 43. Константа диссоциации меняется при изменении температуры согласно уравнению изобары химической реакции: 1.3 Параметры, характеризующие растворы электролитов
- 46. Уравнение предельного закона Дебая-Хюккеля Z+ и Z- - заряды катиона и аниона (по абсолютной величине) I
- 47. 1.3 Параметры, характеризующие растворы электролитов Теория сильных электролитов Дебая-Хюккеля Уравнение применим для растворов с концентрацией не
- 48. 1.3 Параметры, характеризующие растворы электролитов Теория сильных электролитов Дебая-Хюккеля
- 50. 1.4 Электропроводность растворов электролитов Факторы, влияющие на скорость движения иона в электрическом поле Размер иона: чем
- 51. 1.4 Электропроводность растворов электролитов Скорость движения иона в электрическом поле Отношение скорости иона к напряженности электрического
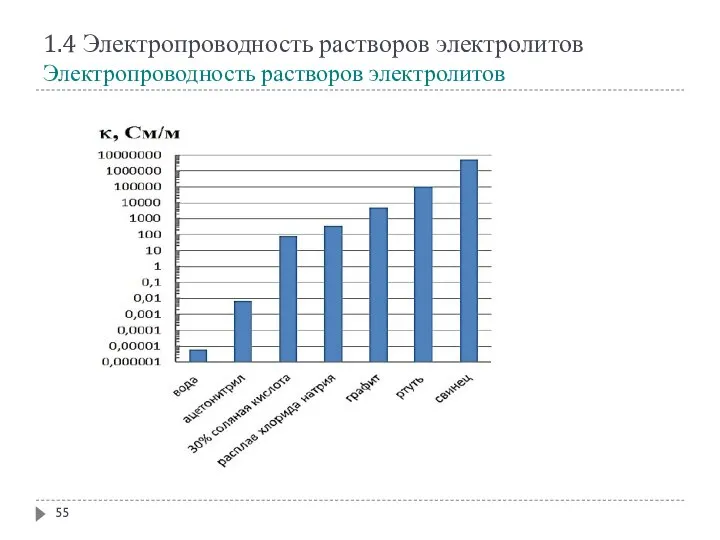
- 53. 1.4 Электропроводность растворов электролитов Электропроводность растворов электролитов Мерой способности раствора электролита проводить электрический ток является электропроводность
- 54. Удельная электропроводность (каппа) раствора электролита - это электрическая проводимость объёма раствора, заключённого между двумя параллельными электродами
- 55. 1.4 Электропроводность растворов электролитов Электропроводность растворов электролитов
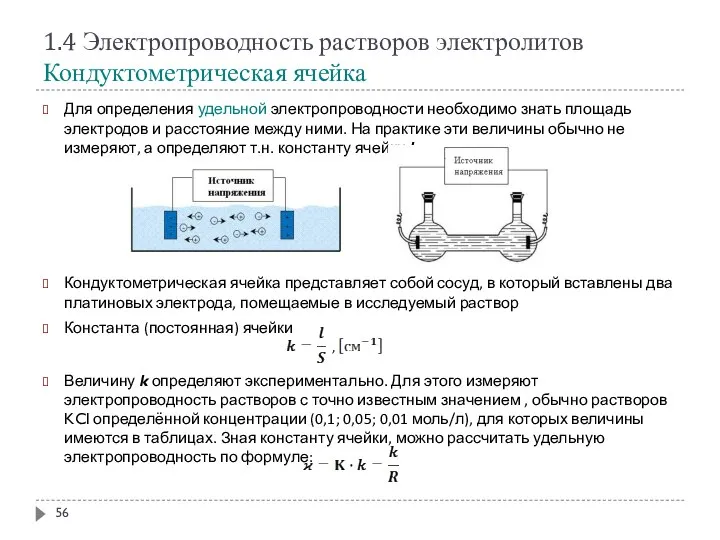
- 56. 1.4 Электропроводность растворов электролитов Кондуктометрическая ячейка Для определения удельной электропроводности необходимо знать площадь электродов и расстояние
- 57. 1.4 Электропроводность растворов электролитов Электропроводность растворов электролитов Удельная электропроводность зависит от: природы электролита и растворителя концентрации
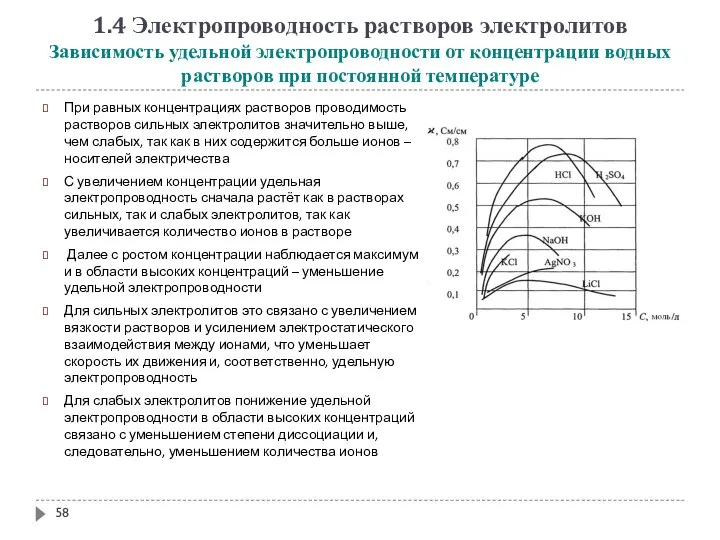
- 58. 1.4 Электропроводность растворов электролитов Зависимость удельной электропроводности от концентрации водных растворов при постоянной температуре При равных
- 59. 1.4 Электропроводность растворов электролитов Зависимость удельной электропроводности от температуры При повышении температуры удельная электропроводность растворов электролитов
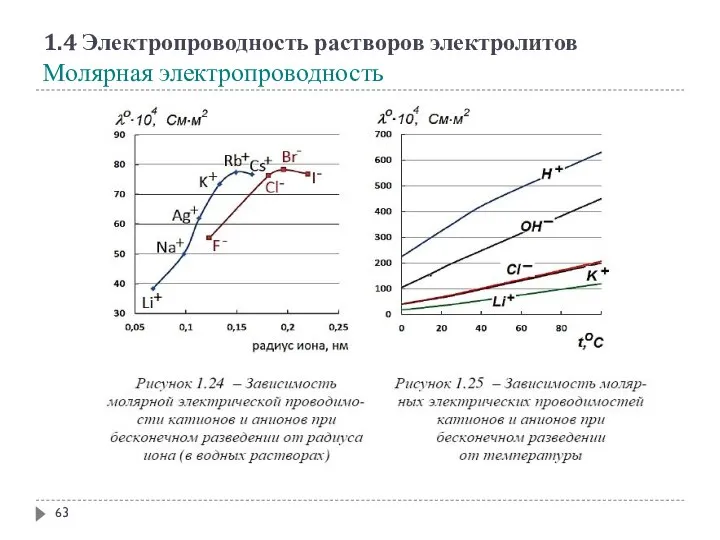
- 60. 1.4 Электропроводность растворов электролитов Молярная электропроводность Молярная электропроводность λ (лямбда) – это проводимость раствора, содержащего 1
- 61. 1.4 Электропроводность растворов электролитов Молярная электропроводность
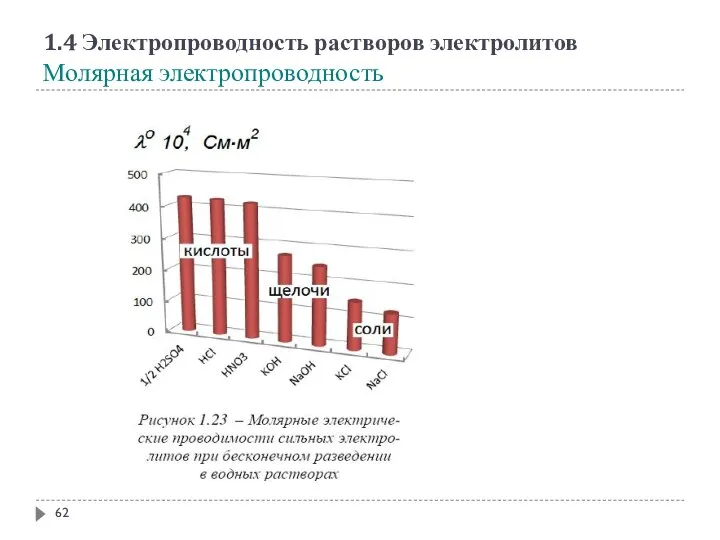
- 62. 1.4 Электропроводность растворов электролитов Молярная электропроводность
- 63. 1.4 Электропроводность растворов электролитов Молярная электропроводность
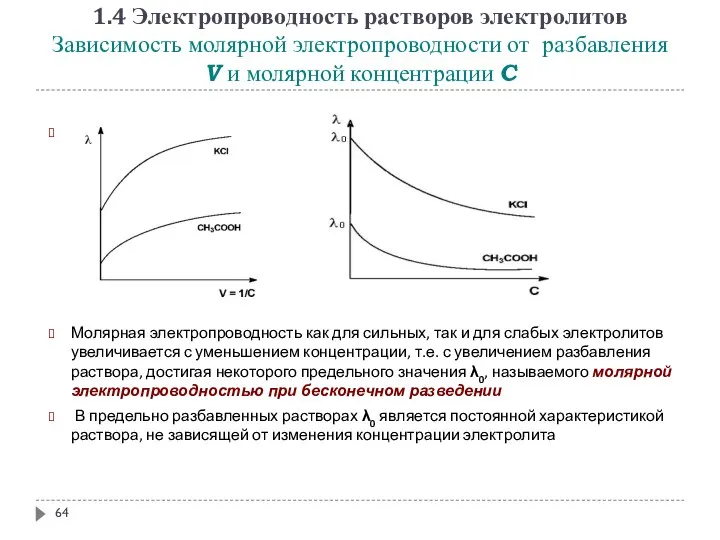
- 64. 1.4 Электропроводность растворов электролитов Зависимость молярной электропроводности от разбавления V и молярной концентрации C Молярная электропроводность
- 65. 1.4 Электропроводность растворов электролитов Эквивалентная электропроводность Эквивалентная электропроводность λэ определяется, если в формуле молярной электропроводности вместо
- 67. 1.4 Электропроводность растворов электролитов Закон Кольрауша
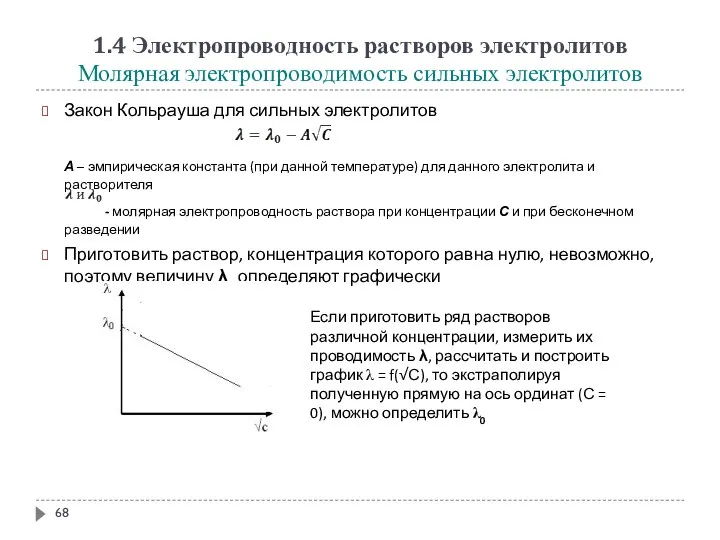
- 68. 1.4 Электропроводность растворов электролитов Молярная электропроводимость сильных электролитов Закон Кольрауша для сильных электролитов А – эмпирическая
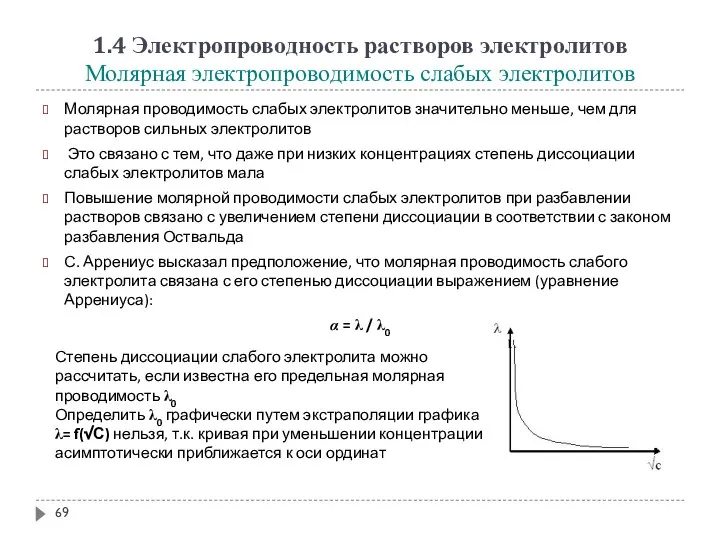
- 69. 1.4 Электропроводность растворов электролитов Молярная электропроводимость слабых электролитов Молярная проводимость слабых электролитов значительно меньше, чем для
- 70. 1.4 Электропроводность растворов электролитов Связь между константой диссоциации и молярной электропроводностью Для бинарного электролита закон Оствальда
- 73. Скачать презентацию






















































 Структурный тип
Структурный тип ГИА-9 Химия. А1
ГИА-9 Химия. А1 Анализ углеводов в пищевых продуктах
Анализ углеводов в пищевых продуктах Полиэтилен — термопластичный полимер этилена
Полиэтилен — термопластичный полимер этилена Ароматические углеводороды. Арены
Ароматические углеводороды. Арены Альдегиды и кетоны
Альдегиды и кетоны Генетические ряды М и НеМ
Генетические ряды М и НеМ Соединения галогенов
Соединения галогенов Аміак Прищепчук Надiя
Аміак Прищепчук Надiя  Основания
Основания Анодные реакции коррозионного процесса
Анодные реакции коррозионного процесса Отримання нанопорошків. Класифікація. Фізичні методи отримання нанопорошків. . Хімічні методи отримання наноматеріалів
Отримання нанопорошків. Класифікація. Фізичні методи отримання нанопорошків. . Хімічні методи отримання наноматеріалів Липиды. Химия липидов. Переваривание липидов в ЖКТ. Нарушение переваривания и всасывания
Липиды. Химия липидов. Переваривание липидов в ЖКТ. Нарушение переваривания и всасывания Сұйықтардағы газ ерітінділері. Генри заңы. Сұйық-сұйық ерітінділердегі бу қысымы. Рауль заңынын ауытқу. Криометрия
Сұйықтардағы газ ерітінділері. Генри заңы. Сұйық-сұйық ерітінділердегі бу қысымы. Рауль заңынын ауытқу. Криометрия Судьба углеродного скелета аминокислот
Судьба углеродного скелета аминокислот Периодическая система химических элементов Д.И. Менделеева. История развития химии
Периодическая система химических элементов Д.И. Менделеева. История развития химии Теория электролитической диссоциации
Теория электролитической диссоциации Фараонова Змея
Фараонова Змея Электрохимиялық талдау әдістері. Дәріс № 13-14
Электрохимиялық талдау әдістері. Дәріс № 13-14 Презентация по химии Биополимеры и их компоненты
Презентация по химии Биополимеры и их компоненты  Свойства спирта и воды
Свойства спирта и воды Химическое образование в современной средней (полной) общеобразовательной школе
Химическое образование в современной средней (полной) общеобразовательной школе Решение задач на нахождение молекулярной формулы органических веществ
Решение задач на нахождение молекулярной формулы органических веществ Непредельные углеводороды. (Лекция 6)
Непредельные углеводороды. (Лекция 6) Алканы. Бутан - С4Н10
Алканы. Бутан - С4Н10 Описание оврага или обнажения (методика проведения практической работы на контрольном туристском маршруте, в походе)
Описание оврага или обнажения (методика проведения практической работы на контрольном туристском маршруте, в походе) Дәрілік зат ретінде қолданылатын сульфанил қышқылы және оның туындылары (сульфаниламидтер)
Дәрілік зат ретінде қолданылатын сульфанил қышқылы және оның туындылары (сульфаниламидтер) Медь. Содержание в природе
Медь. Содержание в природе