Содержание
- 2. Основные понятия и определения Грубодисперсные системы Суспензии Эмульсии Аэрозоли
- 3. Основные понятия и определения Коллоидные растворы Растворы– однофазные системы переменного состава, состоящие из 2 или более
- 4. Теории растворов Физическая теория (Вант-Гофф, Аррениус) – Химическая теория (Менделеев, Каблуков)
- 5. Современная теория объединяет обе теории. Растворы обладают переменностью состава К р-рам не применимы стехиом. законы Р-ры
- 6. Сольватная теория Процесс растворения состоит из 3 стадий Фазовый переход – разрушение кристал. решетки
- 7. Сольватная теория Сольватация ионов Диффузия сольватов
- 8. Растворимость Растворимость – способность в-ва раст-ся в опред. кол-ве раств-ля. Мерой раств-ти крист. в-ва явл-ся конц.
- 9. Растворимость На растворимость влияют: 1. Природа компонентов 1) «Подобное раствор-ся в подобном» 2) Н-связи (неограниченно раст-мы
- 10. Растворимость 2. Температура
- 11. 3. Влияние давления Ув-ние Р приводит к росту раст-сти газов. Закон Генри: раст-сть газа при постоянной
- 12. Свойства растворов неэлектролитов Идеальный раствор – Образ-ие идеального р-ра не сопровождается объемными и тепловыми эффектами.
- 13. Коллигативные свойства растворов Коллиг-ные св-ва – 1. Давление насыщенного пара р-ля над р-ром 2. Температура кипения
- 14. Давление насыщенного пара растворителя над раствором (Первый закон Рауля) жидкость ⮀ пар Растворение в-ва в жидкости
- 15. Первый закон Рауля Обозначим: Pо – давление насыщенного пара р-ля над чистым р-лем; P1о - давление
- 16. Первый закон Рауля P1о = Pо ⋅ Х1
- 17. Первый закон Рауля давление насыщенного пара р-ля над р-ром равно его давлению над чистым р-лем, умноженному
- 18. Первый закон Рауля относительное понижение Р насыщенного пара р-ля над р-ром = мольной доле раст-ного в-ва.
- 19. Температура кипения и замерзания раствора. Второй закон Рауля Tкип. – Tзам. ––
- 20. Температура кипения и замерзания раствора. Второй закон Рауля Повышение tкип р-ра и понижение его tзам прямо
- 21. Осмос Осмотическое давление – это такое Р, которое нужно приложить, чтобы подавить осмос. Вант-Гофф: Pосм. =
- 22. Растворы электролитов Электролиты – это в-ва, способные диссоциировать в р-рах или расплавах на ионы. Доказательство 1.
- 23. Теория электролитической диссоциации Аррениуса (ТЭД) Основные положения ТЭД 1. Электролиты в растворах диссоциируют на ионы. 2.
- 24. Колличественные характеристики процесса диссоциации Константа диссоциации. КД =
- 25. Колличественные характеристики процесса диссоциации Степень диссоциации – это отношение числа диссоциированных молекул к общему числу молекул:
- 26. Колличественные характеристики процесса диссоциации α α > 30% - сильный 3% ≤ α ≤ 30% -
- 27. Связь степени дис-ции с изотоническим коэф-том
- 28. Закон разбавления Оствальда Для слабых электролитов α → 0, а (1 - α) →1 Отсюда: α
- 29. Факторы, влияющие на степень диссоциации α зависит от конц-ции р-ра. α зависит от T. 3. α
- 31. Скачать презентацию




























 Олигосахариды и полисахариды
Олигосахариды и полисахариды Презентация по Химии "Волокнистые материалы вокруг нас" - скачать смотреть
Презентация по Химии "Волокнистые материалы вокруг нас" - скачать смотреть 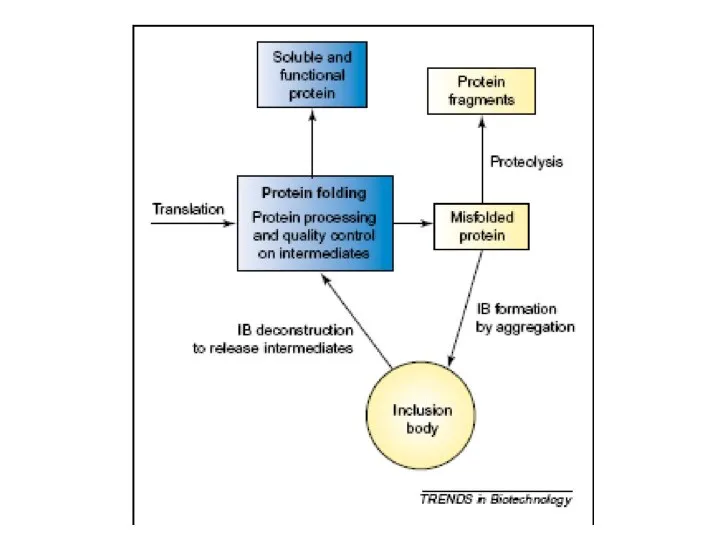 Рефолдинг миниантител
Рефолдинг миниантител Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева Составил: учитель хим
Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева Составил: учитель хим Методические рекомендации по изучению курса «Коррозия и защита металлов»
Методические рекомендации по изучению курса «Коррозия и защита металлов» Бромды метил буының концентрациясын анықтау тәсілдемесі
Бромды метил буының концентрациясын анықтау тәсілдемесі Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії, алотропні видозміни Оксигену і Соли в свете теории ЭД
Соли в свете теории ЭД Строение твердых и жидких металлов. Зональная ликвация
Строение твердых и жидких металлов. Зональная ликвация Презентация Подгруппа углерода и азота
Презентация Подгруппа углерода и азота Сульфаттар және эфирсульфаттар
Сульфаттар және эфирсульфаттар Устойчивое развитие
Устойчивое развитие Обмен белков, жиров и углеводов
Обмен белков, жиров и углеводов Основы общей химии
Основы общей химии Вдоль по радуге
Вдоль по радуге Машиностроительные материалы
Машиностроительные материалы The alkali metals
The alkali metals Устойчивость и коагуляция коллоидных систем
Устойчивость и коагуляция коллоидных систем Правила безпечного використання засобів побутової хімії.
Правила безпечного використання засобів побутової хімії.  Электролитическая диссоциация веществ
Электролитическая диссоциация веществ Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон
Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон Химический состав живых организмов. Метаболизм
Химический состав живых организмов. Метаболизм Аргентум, или серебро
Аргентум, или серебро Chemistry of life
Chemistry of life Алюминий
Алюминий  Гетерогенный катализ
Гетерогенный катализ Драгоценные камни
Драгоценные камни ОВР в гетерогенных системах
ОВР в гетерогенных системах