Содержание
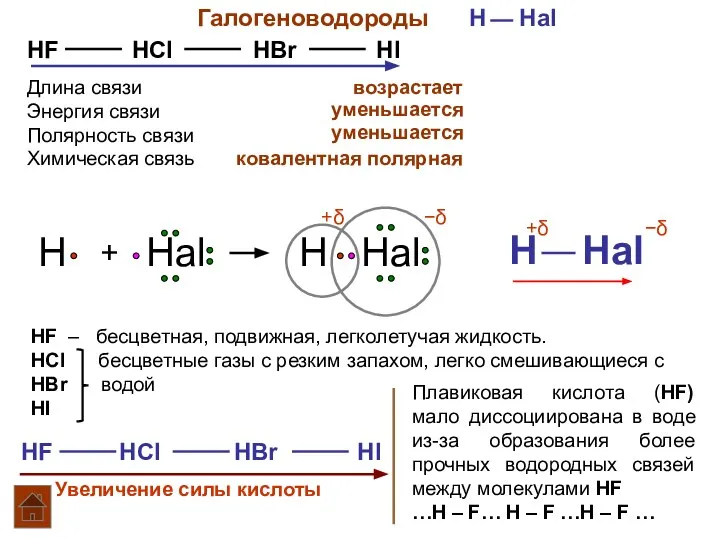
- 2. Галогеноводороды H Hal HF HCl HBr HI Длина связи Энергия связи Полярность связи возрастает уменьшается уменьшается
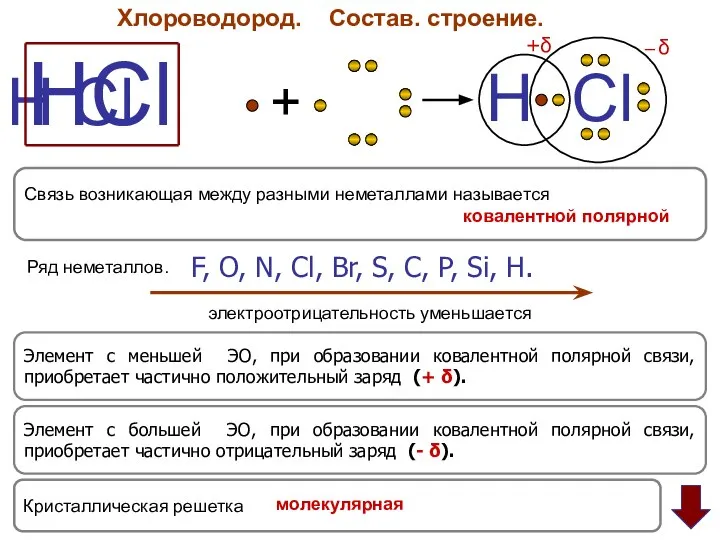
- 3. Хлороводород. Состав. строение. HCl H Cl + H Cl +δ ─ δ Элемент с большей ЭО,
- 5. Получение хлороводорода В лаборатории для получения HCl используют реакцию обмена между кристаллическим хлоридом натрия и концентрированной
- 6. Физические свойства хлороводорода Хлороводород – это газ с резким запахом, без цвета, очень хорошо растворим в
- 7. Соляная кислота (HCl) Классификация Соляная кислота по: наличию кислорода: основности: растворимости в воде: летучести: степени электролитической
- 8. Физические свойства соляной кислоты Соляная кислота – бесцветная дымящаяся на воздухе жидкость (в продажу поступает 36%-ный
- 9. Химические свойства соляной кислоты 1. Действие соляной кислоты на индикаторы 2. Взаимодействие с металлами 3. Взаимодействие
- 10. Соляная кислота необратимо диссоциирует в водном растворе. Составьте уравнение диссоциации соляной кислоты. HCl = H+ +
- 11. Взаимодействие соляной кислоты с металлами Составьте уравнение реакции соляной кислоты с цинком. Рассмотрите с т.зр. ТЭД
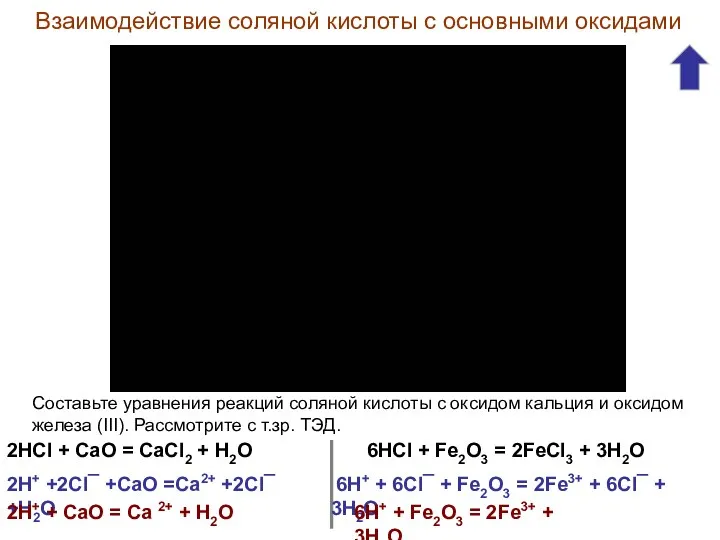
- 12. Взаимодействие соляной кислоты с основными оксидами Составьте уравнения реакций соляной кислоты с оксидом кальция и оксидом
- 13. Реакция нейтрализации Составьте уравнения реакций соляной кислоты c гидроксидом натрия. Рассмотрите с т.зр. ТЭД. HCl +
- 14. Взаимодействие соляной кислоты с солями Составьте уравнения реакций соляной кислоты c карбонатом натрия натрия. Рассмотрите с
- 15. Применение соляной кислоты 1. Получение солей 4. При паянии 3. Приготовление лекарств 2. Производство пластмасс и
- 16. HCl 1 3 2 4 5 6
- 17. Соли соляной кислоты (хлориды) Хлорид натрия 1. Состав NaCl 2. Строение Химическая связь между катионами и
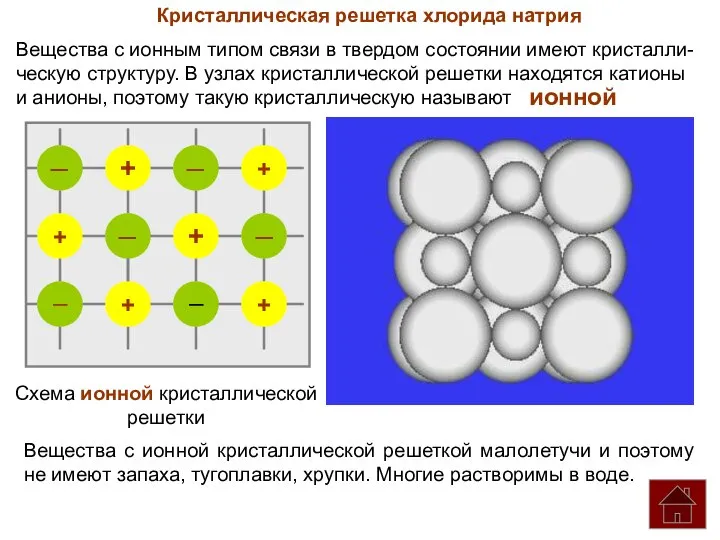
- 18. Кристаллическая решетка хлорида натрия Вещества с ионным типом связи в твердом состоянии имеют кристалли- ческую структуру.
- 19. Качественное определение галогенид-ионов На соляную кислоту и ее соли хлориды, равно как на HBr и бромиды,
- 21. Скачать презентацию














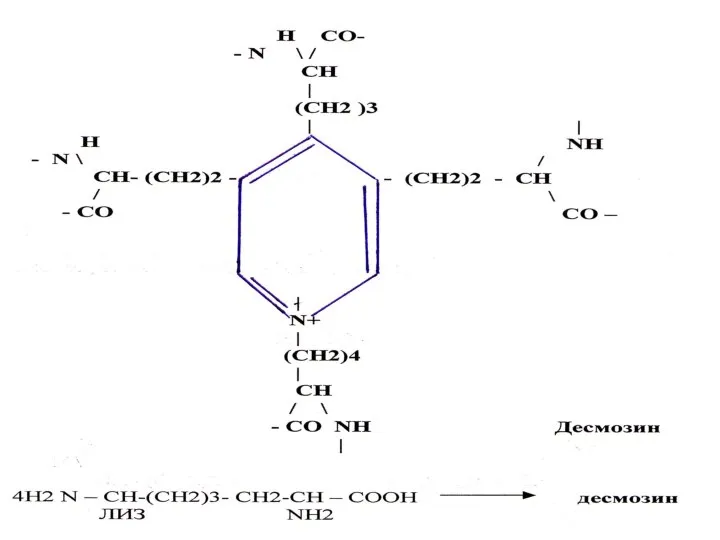 Гиалурон қышқылы
Гиалурон қышқылы Минералы
Минералы Водорастворимые витамины. 7 свойств водорастворимых витаминов
Водорастворимые витамины. 7 свойств водорастворимых витаминов Азот в природе
Азот в природе Сапфиры. Месторождения сапфира
Сапфиры. Месторождения сапфира Основные понятия и законы химии
Основные понятия и законы химии - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Презентация по Химии "Алкены." - скачать смотреть бесплатно_
Презентация по Химии "Алкены." - скачать смотреть бесплатно_ Прогнозування хімічної обстановки під час застосування хімічної зброї
Прогнозування хімічної обстановки під час застосування хімічної зброї Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3
Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3 Викторина Своя игра по химии
Викторина Своя игра по химии Химическая реакция
Химическая реакция Чистящие и моющие средства для мытья посуды
Чистящие и моющие средства для мытья посуды Коллоидная химия
Коллоидная химия Аміак
Аміак  Қазіргі кезде қолданылатын дезинсектицидтер
Қазіргі кезде қолданылатын дезинсектицидтер Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский Хімія та обмін ліпідів
Хімія та обмін ліпідів Исследование свойств моющих средств
Исследование свойств моющих средств Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5
Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5 Силикатная промышленность
Силикатная промышленность Генетическая связь между классами веществ
Генетическая связь между классами веществ Химическая викторина Пятый элемент
Химическая викторина Пятый элемент Хлор. Отравления хлором
Хлор. Отравления хлором Презентация по Химии "Основания, их классификация и свойства в свете теории электролитической диссоциации" - скачать смотрет
Презентация по Химии "Основания, их классификация и свойства в свете теории электролитической диссоциации" - скачать смотрет Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Серосодержащие макрогетероциклы (тиакраун-соединения)
Серосодержащие макрогетероциклы (тиакраун-соединения)