Содержание
- 2. ВВЕДЕНИЕ (2) * ЦЕЛИ КУРСА создать основу для дальнейшего изучения химических дисциплин, сформировать элементарные навыки работы
- 3. ПРЕДМЕТ ХИМИИ (1) Химия – естественная наука, изучающая вещества, их строение, свойства и превращения. Вещество –
- 4. ПРЕДМЕТ ХИМИИ (2) Материя находится в непрерывном движении (филос.: материя не существует без движения). Формы движения
- 5. * Основы химии. ПРЕДМЕТ ХИМИИ (3) Мерой движения и взаимодействия различных видов материи служит энергия Мерой
- 6. ПРЕДМЕТ ХИМИИ (4) * Основы химии. 20 млн. органических веществ 0,5 млн. неорганических веществ Каждое из
- 7. ПРЕДМЕТ ХИМИИ (5) * Основы химии. Превращения веществ, сопровождающиеся изменением состава, называются химическими реакциями. Химические реакции
- 8. СКОЛЬКО ХИМИЙ НА СВЕТЕ? Журнал «Химия и жизнь - XXI век». №№ 5 и 6, 2009
- 9. РАЗДЕЛЫ ХИМИИ (1) * Основы химии. Общая химия - изучает общетеоретические вопросы химии: основные понятия и
- 10. РАЗДЕЛЫ ХИМИИ (2) * Основы химии. Неорганическая химия - занимается изучением химической природы элементов и их
- 11. РАЗДЕЛЫ ХИМИИ (3) * Основы химии. Физическая химия использует физические методы для изучения химических систем. Важное
- 12. РАЗДЕЛЫ ХИМИИ (4) * Основы химии. Биохимия изучает сложнейшие химические процессы, протекающие в живых организмах Геохимия
- 13. ОБЪЕКТЫ ИЗУЧЕНИЯ (1) * Основы химии. Объектом изучения в химии являются химические элементы и их соединения
- 14. ОБЪЕКТЫ ИЗУЧЕНИЯ (2) * Основы химии. Химический элемент (лат. elementum - часть чего-то) – совокупность (вид)
- 15. ОБЪЕКТЫ ИЗУЧЕНИЯ (3) * Основы химии. Каждый элемент обозначается символом из одной или двух латинских букв
- 16. ОБЪЕКТЫ ИЗУЧЕНИЯ (4) * Основы химии. Химические элементы существуют в виде простых веществ, состоящих из атомов
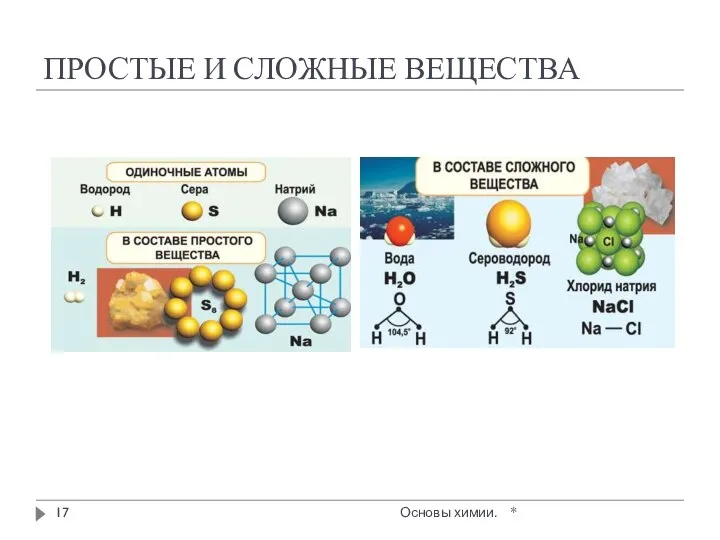
- 17. ПРОСТЫЕ И СЛОЖНЫЕ ВЕЩЕСТВА * Основы химии.
- 18. АЛЛОТРОПИЯ (1) * Основы химии. Аллотропия – способность химического элемента образовывать несколько простых веществ, называемых аллотропными
- 19. АЛЛОТРОПИЯ(2) Аллотропные модификации олова: α-Sn (серое олово, полупроводник со структурой алмаза) и β-Sn (обычное белое олово,
- 20. АЛЛОТРОПИЯ (3) Аллотропные модификации фосфора Р: белый (желтый), красный и черный * Основы химии.
- 21. АЛЛОТРОПИЯ (4) Аллотропные модификации серы (S): ромбическая, моноклинная и пластическая (аморфная) Аллотропные модификации кислорода: молекулярный кислород
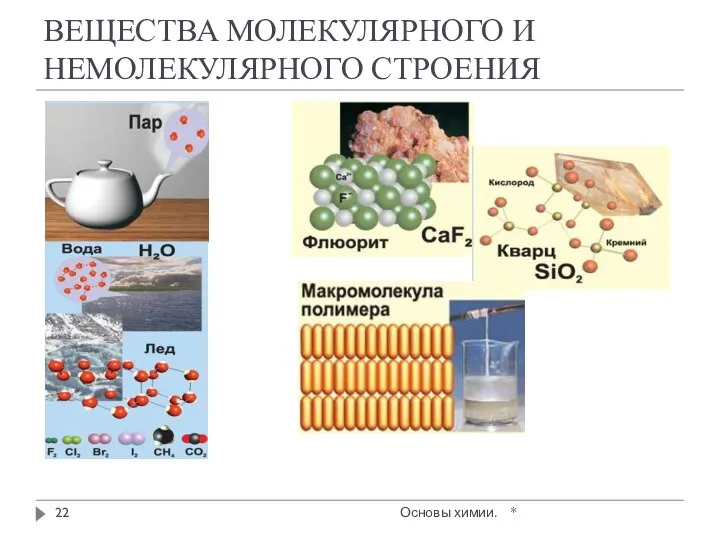
- 22. ВЕЩЕСТВА МОЛЕКУЛЯРНОГО И НЕМОЛЕКУЛЯРНОГО СТРОЕНИЯ * Основы химии.
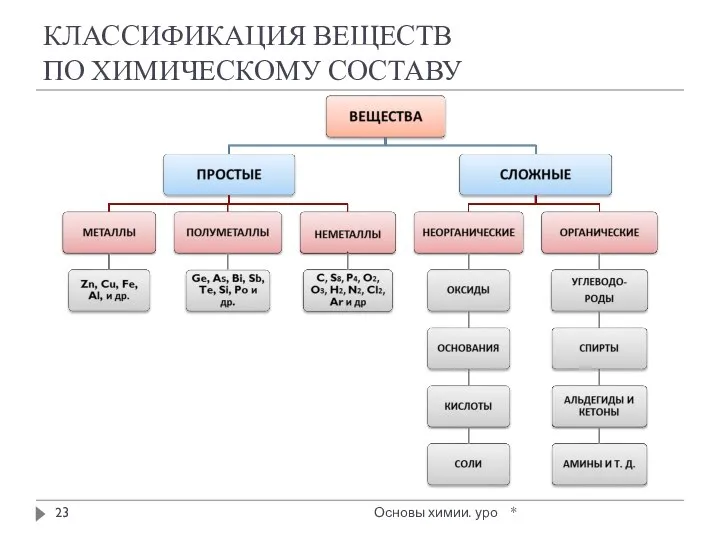
- 23. КЛАССИФИКАЦИЯ ВЕЩЕСТВ ПО ХИМИЧЕСКОМУ СОСТАВУ * Основы химии. уро
- 24. ОСНОВНЫЕ ЗАКОНЫ ХИМИИ (1) * Основы химии. Закон сохранения материи и энергии Если в одном месте
- 25. ОСНОВНЫЕ ЗАКОНЫ ХИМИИ (2) * Основы химии. Закон постоянства состава вещества Всякое чистое вещество независимо от
- 26. ОСНОВНЫЕ ЗАКОНЫ ХИМИИ (3) Закон кратных отношений Если два химических элемента дают несколько соединений, то массовые
- 27. ОСНОВНЫЕ ЗАКОНЫ ХИМИИ (4) Закон объемных отношений Объемы газов, вступающих в химическую реакцию, и объемы газов,
- 28. ОСНОВНЫЕ ПОНЯТИЯ (1) Атом – электронейтральная частица, состоящая из положительно заряженного ядра и вращающихся вокруг него
- 29. ОСНОВНЫЕ ПОНЯТИЯ (2) Масса атомов и молекул очень мала, 10-24 – 10-23 г Например, масса атома
- 30. ОСНОВНЫЕ ПОНЯТИЯ (3) Относительная атомная масса элемента Ar (или просто атомная масса) – масса атома, выраженная
- 31. ОСНОВНЫЕ ПОНЯТИЯ (4) МОЛЬ - это количество вещества, содержащее столько частиц (атомов, молекул, ионов, электронов или
- 32. ОСНОВНЫЕ ПОНЯТИЯ (5) Молярная масса (М) – масса 1 моля вещества в граммах [М] = [г/моль]
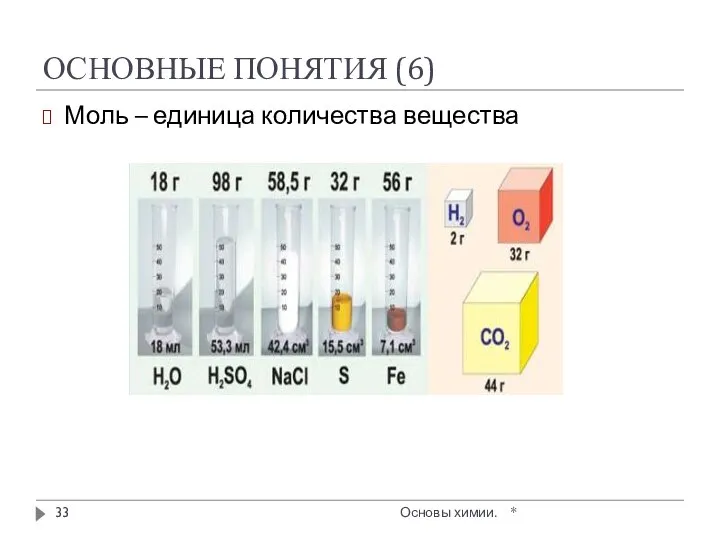
- 33. ОСНОВНЫЕ ПОНЯТИЯ (6) Моль – единица количества вещества * Основы химии.
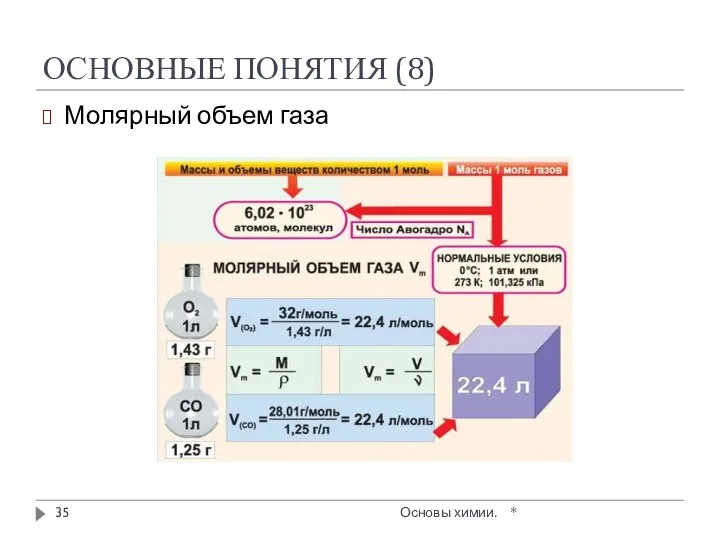
- 34. ОСНОВНЫЕ ПОНЯТИЯ (7) * Основы химии. Молярный объем газа VM – объем одного моля газа при
- 35. ОСНОВНЫЕ ПОНЯТИЯ (8) Молярный объем газа * Основы химии.
- 36. ОСНОВНЫЕ ПОНЯТИЯ (7) Моль это: 6,02•1023 частиц масса вещества в граммах, численно равная молярной массе вещества
- 38. Скачать презентацию






























 Алканы
Алканы Урок химии в 9-ом классе Тема урока "Сера"
Урок химии в 9-ом классе Тема урока "Сера" Метод кислотноосновного титрования (Метод нейтрализации)
Метод кислотноосновного титрования (Метод нейтрализации) Химия-технологиялық процестеріндегі негізгі заңдылықтары. Технологиялық процестерідегі тепетеңдік
Химия-технологиялық процестеріндегі негізгі заңдылықтары. Технологиялық процестерідегі тепетеңдік Примерная рабочая программа основного общего образования предмета Химия
Примерная рабочая программа основного общего образования предмета Химия Метод инверсионной вольтамперометрии
Метод инверсионной вольтамперометрии Цепная сополимеризация
Цепная сополимеризация Специфическое поведение гетерофункциональных соединений как результат взаимного влияния атомов
Специфическое поведение гетерофункциональных соединений как результат взаимного влияния атомов Колебания кристаллической решетки и ее тепловые свойства. Тепловые свойства
Колебания кристаллической решетки и ее тепловые свойства. Тепловые свойства Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов
Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов Равновесие в растворах электролитов
Равновесие в растворах электролитов Химия S - элементов
Химия S - элементов ИЗ ОПЫТА ИСПОЛЬЗОВАНИЯ ИНТЕРАКТИВНОЙ ДОСКИ НА УРОКАХ ХИМИИ.
ИЗ ОПЫТА ИСПОЛЬЗОВАНИЯ ИНТЕРАКТИВНОЙ ДОСКИ НА УРОКАХ ХИМИИ. Основания (оснόвные гидроксиды)
Основания (оснόвные гидроксиды)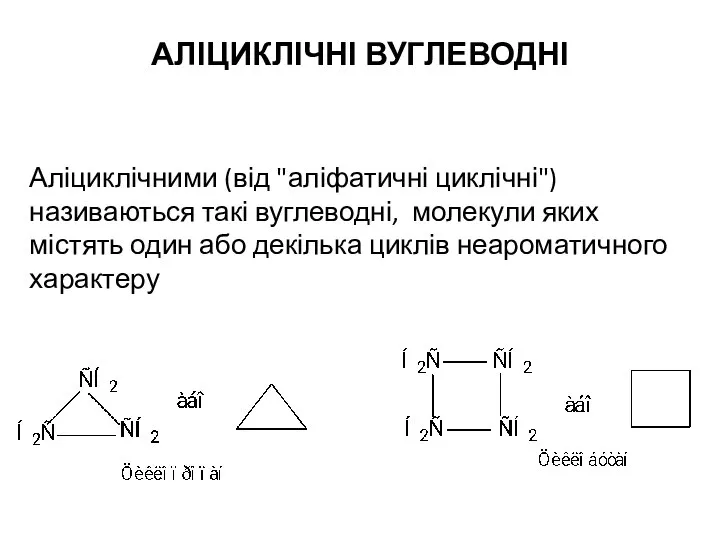 Аліциклічні вуглеводні
Аліциклічні вуглеводні Термодинамические расчеты и формальная кинетика
Термодинамические расчеты и формальная кинетика Презентация по теме Круговорот углерода в природе 9 класс
Презентация по теме Круговорот углерода в природе 9 класс Кислотные дожди
Кислотные дожди  Презентація на тему: Твердість води Способи усунення твердості води
Презентація на тему: Твердість води Способи усунення твердості води  Цікаві факти про хімію
Цікаві факти про хімію Оцтова кислота, молекулярна і структурна формули, фізичні властивості . Хімічні властивості. Застосування
Оцтова кислота, молекулярна і структурна формули, фізичні властивості . Хімічні властивості. Застосування  Гидролиз. Сущность процесса гидролиза
Гидролиз. Сущность процесса гидролиза Химия. Вещества. Занятие 1
Химия. Вещества. Занятие 1 Строение атома
Строение атома Электромагнитное облучение. Радиоактивное загрязнение
Электромагнитное облучение. Радиоактивное загрязнение Электролитическая диссоциация
Электролитическая диссоциация Маңызды химиялық өндірістер
Маңызды химиялық өндірістер Элементердің құрамына қарай бөлінуі
Элементердің құрамына қарай бөлінуі