Содержание
- 2. СТЕПЕНЬ ОКИСЛЕНИЯ – ЭТО МЕРА «ДЕФОРМАЦИИ» ЭЛЕКТРОННОЙ ОБОЛОЧКИ ПРИ ОБРАЗОВАНИИ ХИМИЧЕСКОЙ СВЯЗИ. Она показывает как и
- 3. Строгое определение степени окисления: СТЕПЕНЬ ОКИСЛЕНИЯ – ЭТО УСЛОВНЫЙ ЗАРЯД АТОМА ХИМИЧЕСКОГО ЭЛЕМЕНТА В СЛОЖНОМ ВЕЩЕСТВЕ,
- 4. ПРАВИЛА И ИСКЛЮЧЕНИЯ: Степень окисления у свободных атомов и атомов, образующих простые вещества, равна нулю!!! У
- 5. Постоянные степени окисления: Металлы IA группы (Li, Na, K, Rb, Cs, Fr) +1 Металлы IIA группы
- 6. Бинарные соединения Бинарными называются соединения, молекулы которых состоят из атомов двух химических элементов.
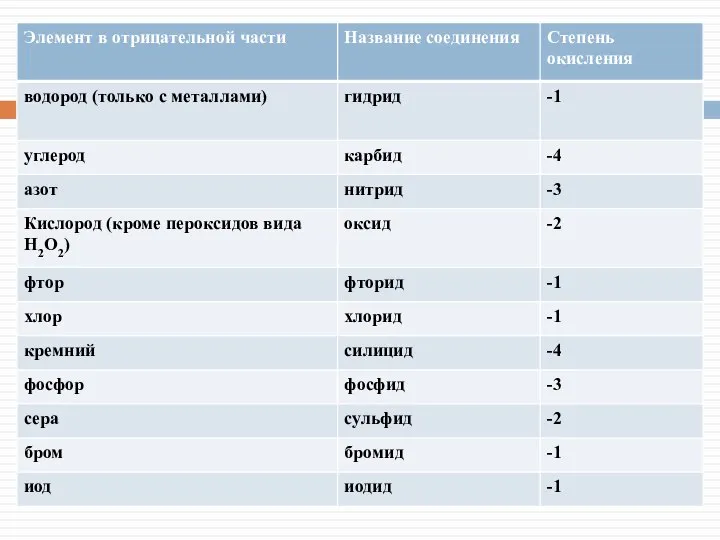
- 7. Номенклатура бинарных соединений: Называется «отрицательная часть» молекулы (таблица на следующем слайде) Называется «положительная часть» молекулы (элемент
- 10. Скачать презентацию






 Гиалурон қышқылы
Гиалурон қышқылы Минералы
Минералы Водорастворимые витамины. 7 свойств водорастворимых витаминов
Водорастворимые витамины. 7 свойств водорастворимых витаминов Азот в природе
Азот в природе Сапфиры. Месторождения сапфира
Сапфиры. Месторождения сапфира Основные понятия и законы химии
Основные понятия и законы химии - Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового
- Это оружие массового поражения, действие которого основано на токсических свойствах химических веществ. - Это оружие массового  Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки
Особенности химии, связанные с её физикализацией. Дифференциация и интеграция науки Презентация по Химии "Алкены." - скачать смотреть бесплатно_
Презентация по Химии "Алкены." - скачать смотреть бесплатно_ Прогнозування хімічної обстановки під час застосування хімічної зброї
Прогнозування хімічної обстановки під час застосування хімічної зброї Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3
Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3 Викторина Своя игра по химии
Викторина Своя игра по химии Химическая реакция
Химическая реакция Чистящие и моющие средства для мытья посуды
Чистящие и моющие средства для мытья посуды Коллоидная химия
Коллоидная химия Аміак
Аміак  Қазіргі кезде қолданылатын дезинсектицидтер
Қазіргі кезде қолданылатын дезинсектицидтер Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский
Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования Томский Хімія та обмін ліпідів
Хімія та обмін ліпідів Исследование свойств моющих средств
Исследование свойств моющих средств Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5
Личностно – ориентированный подход в обучении химии Талавир С.Е. Учитель химии МОУ СОШ№5 Силикатная промышленность
Силикатная промышленность Генетическая связь между классами веществ
Генетическая связь между классами веществ Химическая викторина Пятый элемент
Химическая викторина Пятый элемент Хлор. Отравления хлором
Хлор. Отравления хлором Презентация по Химии "Основания, их классификация и свойства в свете теории электролитической диссоциации" - скачать смотрет
Презентация по Химии "Основания, их классификация и свойства в свете теории электролитической диссоциации" - скачать смотрет Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Серосодержащие макрогетероциклы (тиакраун-соединения)
Серосодержащие макрогетероциклы (тиакраун-соединения)