Содержание
- 2. Антиоксиданты, и способы их изучения
- 3. Антиоксиданты - соединения, тормозящие процессы оксидативного стресса Оксидативный стресс - процесс, повреждения биологических структур, протекающий с
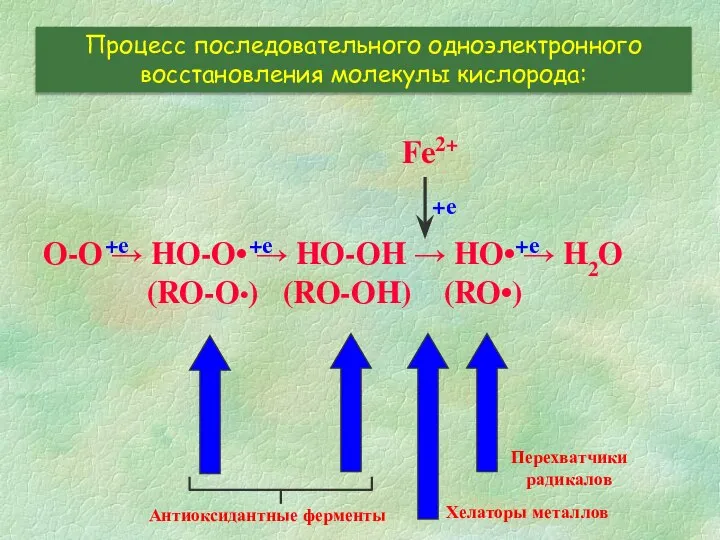
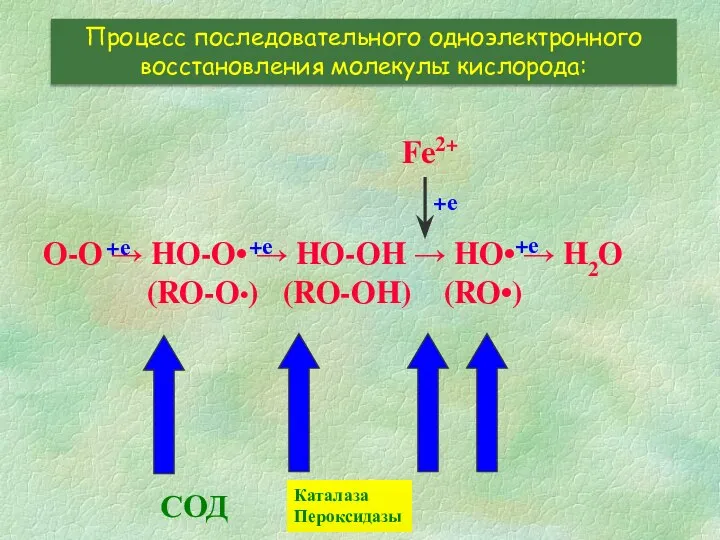
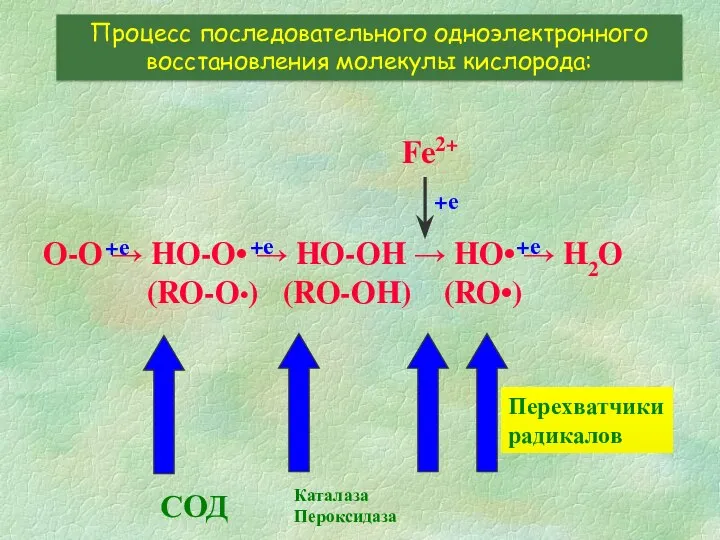
- 4. O-O → HO-O• → HO-OH → HO• → H2O (RO-O•) (RO-OH) (RO•) Процесс последовательного одноэлектронного восстановления
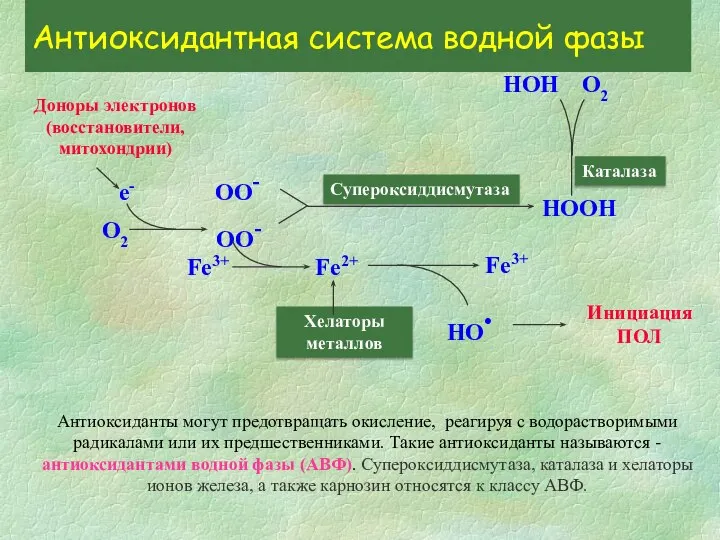
- 5. О2 Доноры электронов (восстановители, митохондрии) е- ОО- ОО- Супероксиддисмутаза НООН Каталаза Fe3+ Fe2+ Хелаторы металлов Инициация
- 6. Антиоксидантные ферменты Супероксид дисмутаза
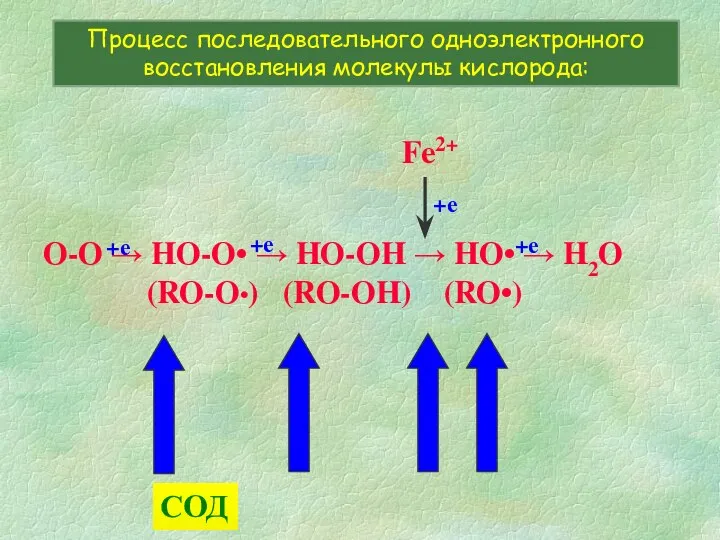
- 7. O-O → HO-O• → HO-OH → HO• → H2O (RO-O•) (RO-OH) (RO•) Процесс последовательного одноэлектронного восстановления
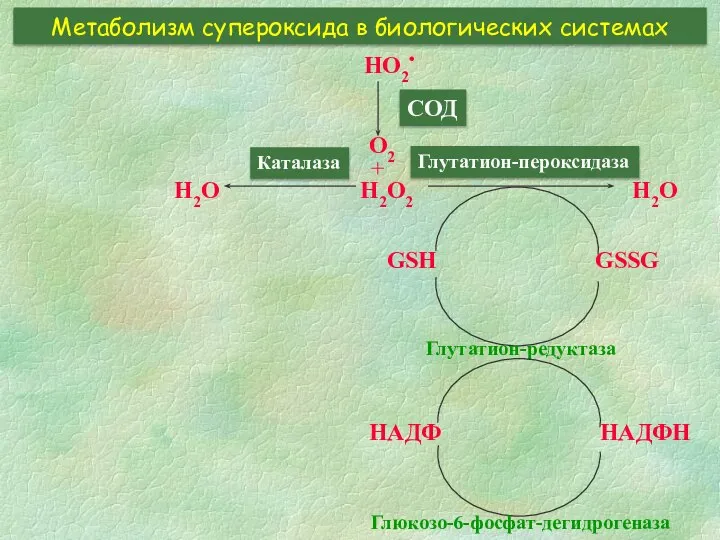
- 8. Метаболизм супероксида в биологических системах HO2• СОД O2 + H2O2 GSH GSSG Глутатион-редуктаза НАДФ НАДФН Глюкозо-6-фосфат-дегидрогеназа
- 9. Супероксиддисмутаза Супероксиддисмутаза (СОД) - единственный известный в настоящее время фермент, субстратом которого являются свободные радикалы. Супероксиддисмутаза
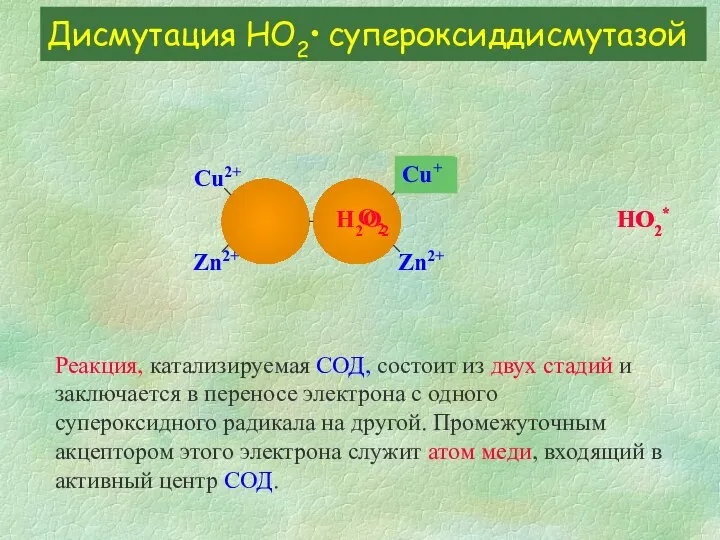
- 10. Дисмутация HО2• супероксиддисмутазой Реакция, катализируемая СОД, состоит из двух стадий и заключается в переносе электрона с
- 11. Дисмутация HО2• супероксиддисмутазой Сu2+ Zn2+ Zn2+ Сu2+ HO2* H2O2 Реакция, катализируемая СОД, состоит из двух стадий
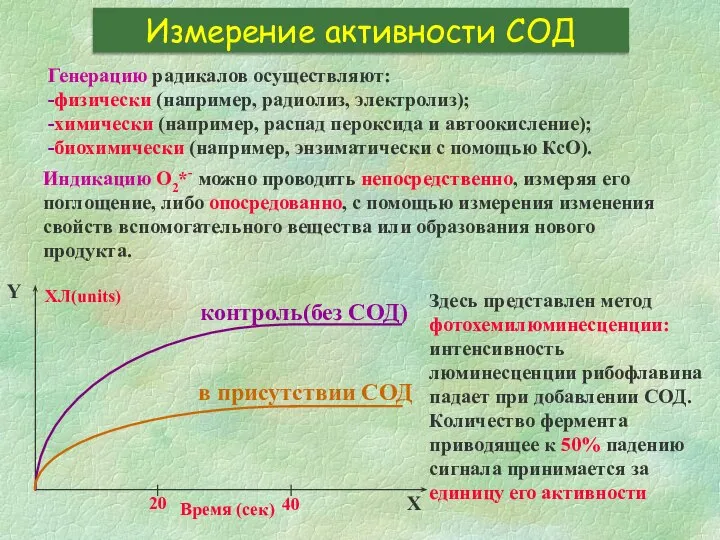
- 12. Измерение активности СОД Генерацию радикалов осуществляют: -физически (например, радиолиз, электролиз); -химически (например, распад пероксида и автоокисление);
- 13. Антиоксидантные ферменты Каталаза и Пероксидазы
- 14. O-O → HO-O• → HO-OH → HO• → H2O (RO-O•) (RO-OH) (RO•) Процесс последовательного одноэлектронного восстановления
- 15. Дезактивация перекиси водорода Перекись водорода (Н2О2) - основной источник самых токсичных радикалов в живых системах -
- 16. Как работают каталаза и пероксидаза? Стадии ферментативного цикла каталазы: Стадии ферментативного цикла пероксидазы: 1. Cat-Fe3+ +
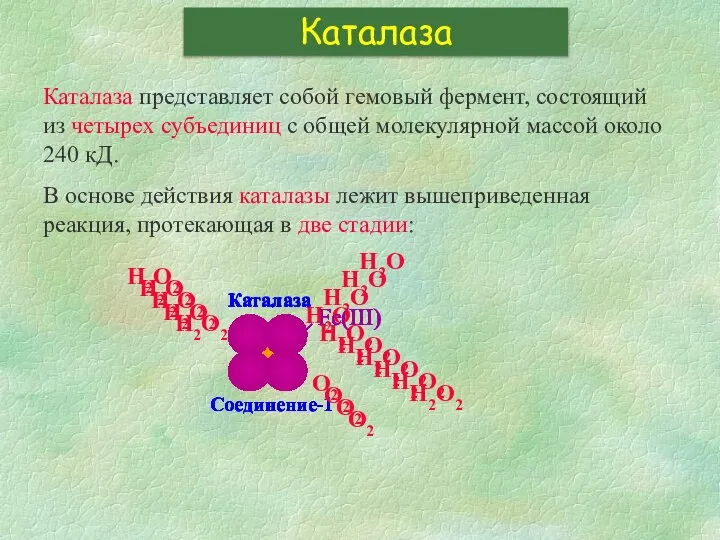
- 17. Каталаза представляет собой гемовый фермент, состоящий из четырех субъединиц с общей молекулярной массой около 240 кД.
- 18. Пероксидазы Пероксидазы также являются ферментами, разрушающими Н2О2 нерадикальным путем и образующими Н2О; при этом окислению подвергается
- 19. Перехватчики радикалов Антиоксиданты, и способы их изучения
- 20. O-O → HO-O• → HO-OH → HO• → H2O (RO-O•) (RO-OH) (RO•) Процесс последовательного одноэлектронного восстановления
- 21. Перехватчики радикалов В качестве системы защиты организма от повреждающего действия радикалов кислорода могут выступать низкомолекулярные вещества,
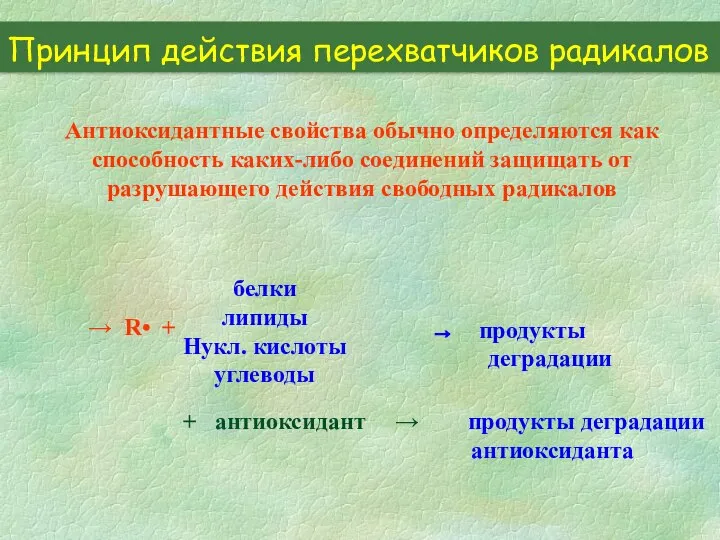
- 22. Принцип действия перехватчиков радикалов Антиоксидантные свойства обычно определяются как способность каких-либо соединений защищать от разрушающего действия
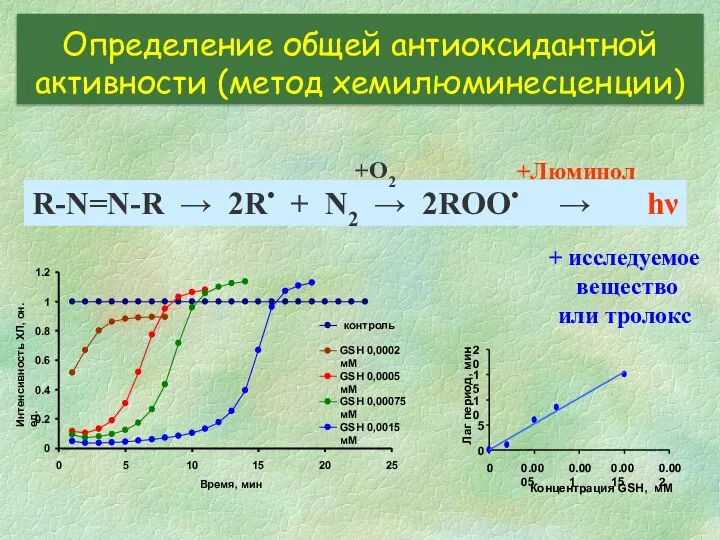
- 23. R-N=N-R → 2R• + N2 → 2ROO• → hν +O2 +Люминол 0 0.2 0.4 0.6 0.8
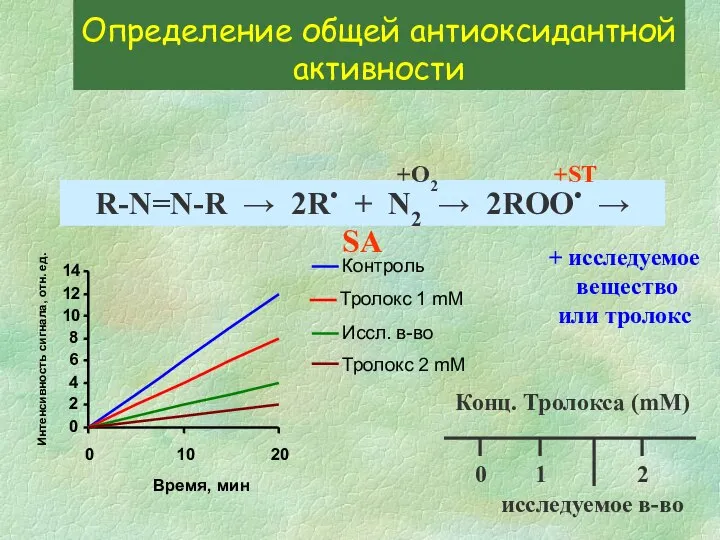
- 24. Определение общей антиоксидантной активности R-N=N-R → 2R• + N2 → 2ROO• → SA +O2 +ST 0
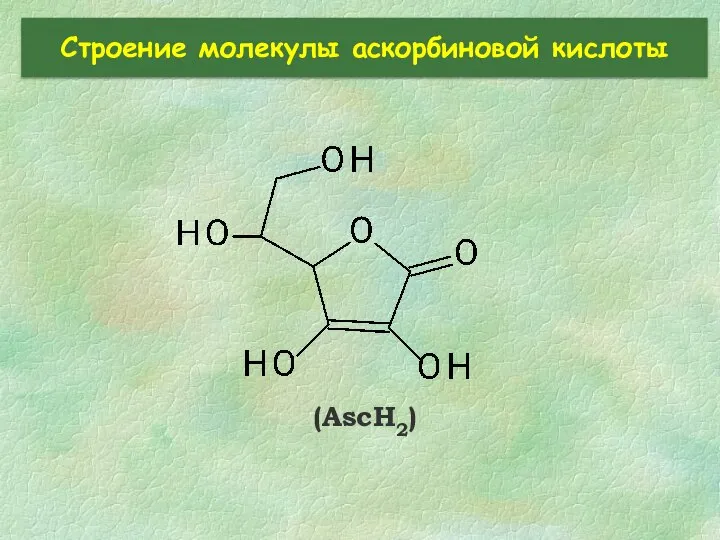
- 25. Строение молекулы аскорбиновой кислоты (AscH2)
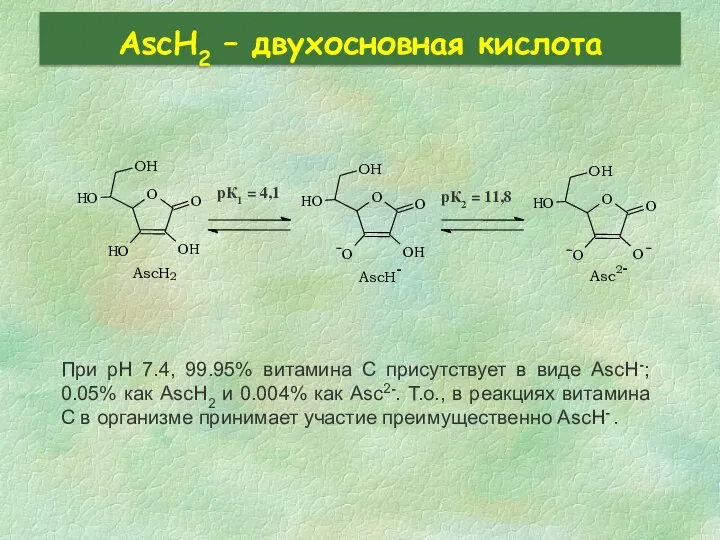
- 26. AscH2 – двухосновная кислота При pH 7.4, 99.95% витамина C присутствует в виде AscH-; 0.05% как
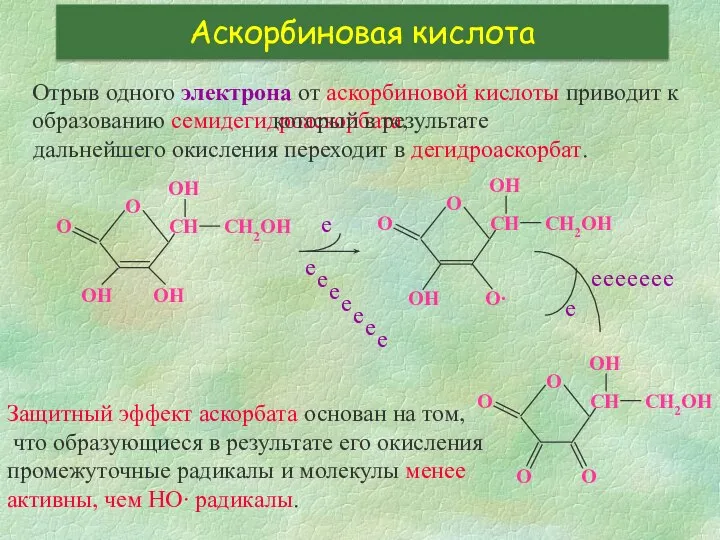
- 27. Аскорбиновая кислота Отрыв одного электрона от аскорбиновой кислоты приводит к образованию семидегидроаскорбата, е е е е
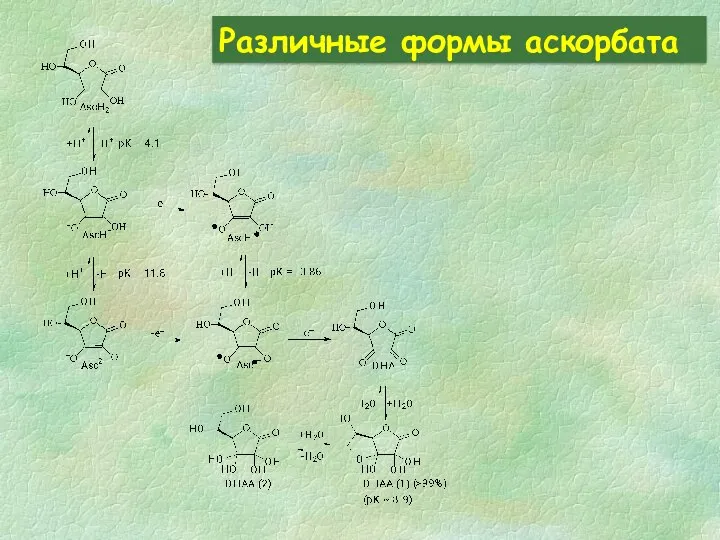
- 28. Различные формы аскорбата
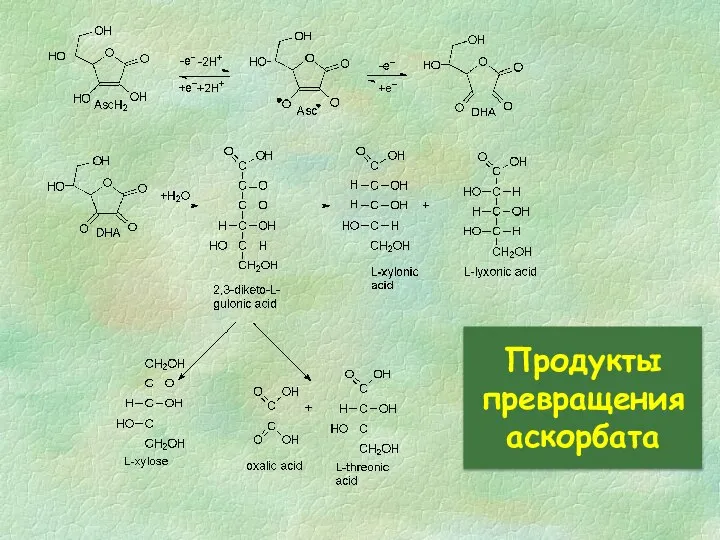
- 29. Продукты превращения аскорбата
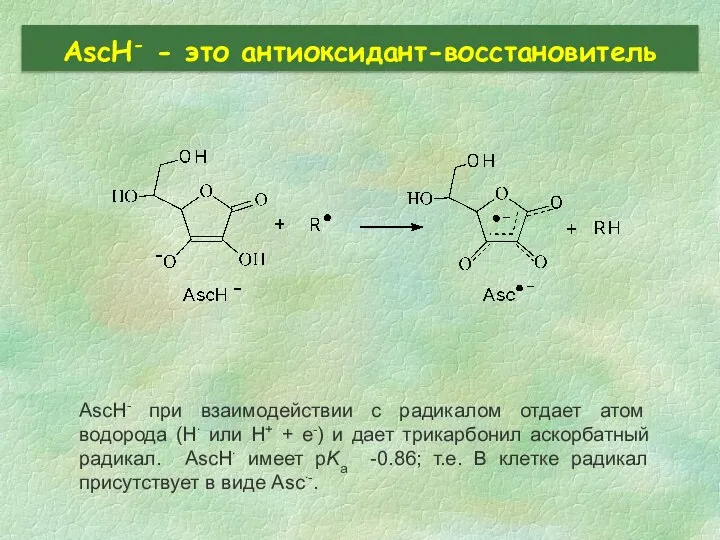
- 30. AscH- - это антиоксидант-восстановитель AscH- при взаимодействии с радикалом отдает атом водорода (H∙ или H+ +
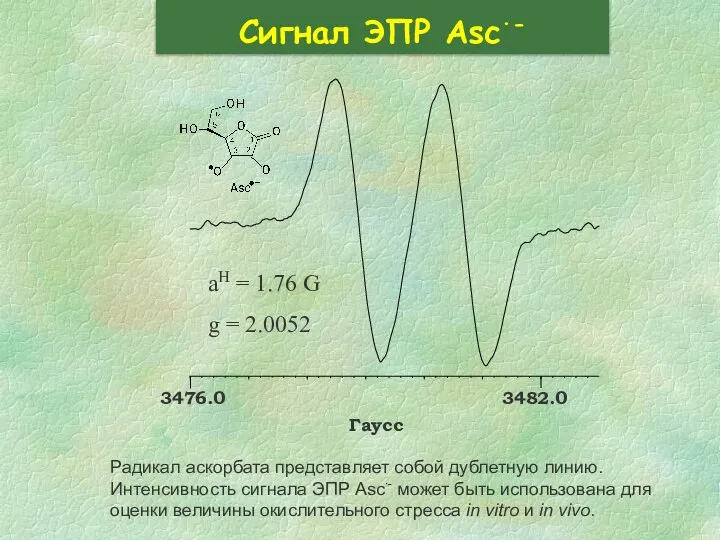
- 31. Сигнал ЭПР Asc∙- Радикал аскорбата представляет собой дублетную линию. Интенсивность сигнала ЭПР Asc∙- может быть использована
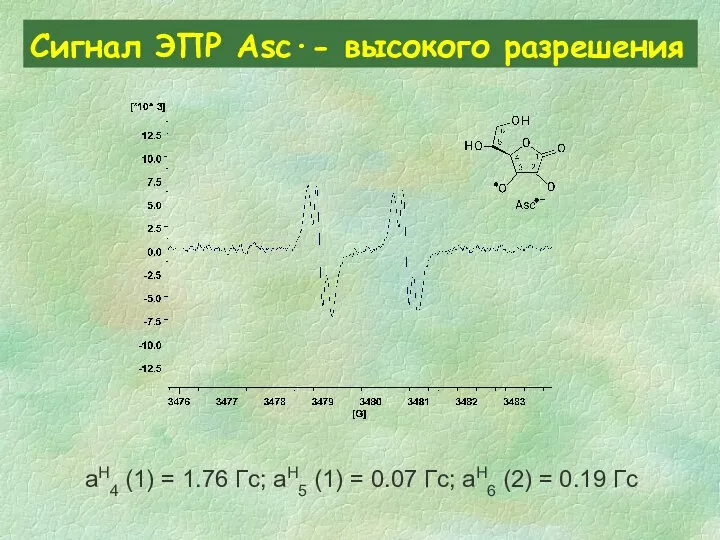
- 32. Сигнал ЭПР Asc∙- высокого разрешения aH4 (1) = 1.76 Гс; aH5 (1) = 0.07 Гс; aH6
- 33. Константы скорости взаимодействия аскорбата с некоторыми радикалами Приведенные константы скорости соответствуют реакции: AscH− + R∙ →
- 34. Asc∙- - маркер окислительного стресса [Asc∙-] – пропорциональна степени окисления аскорбата
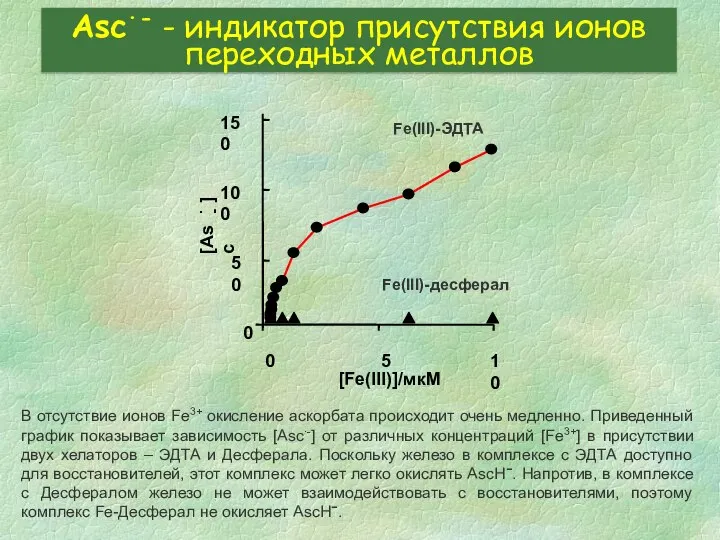
- 35. Asc∙- - индикатор присутствия ионов переходных металлов В отсутствие ионов Fe3+ окисление аскорбата происходит очень медленно.
- 37. Скачать презентацию












![Asc∙- - маркер окислительного стресса [Asc∙-] – пропорциональна степени окисления аскорбата](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393470/slide-33.jpg)
 Презентация по химии Введение в биоорганическую химию
Презентация по химии Введение в биоорганическую химию  Технологічні і біохімічні властивості м‘яса та м‘ясопродуктів. Будова тканин живих організмів
Технологічні і біохімічні властивості м‘яса та м‘ясопродуктів. Будова тканин живих організмів Современные проблемы химической технологии вяжущих материалов
Современные проблемы химической технологии вяжущих материалов Нефть: состав, основные физико-химические свойства. Классификация нефтей
Нефть: состав, основные физико-химические свойства. Классификация нефтей Кислоты
Кислоты Моделі будови атома
Моделі будови атома Контрольная работа
Контрольная работа Металлы. Атомы металлов
Металлы. Атомы металлов Презентация АТОМНАЯ ЭНЕРГЕТИКА
Презентация АТОМНАЯ ЭНЕРГЕТИКА Системы патогенредукции компонентов крови на основе субстанции рибофлавина
Системы патогенредукции компонентов крови на основе субстанции рибофлавина Электрофоретические и хроматографические методы
Электрофоретические и хроматографические методы Конкурс интерактивных презентаций «Интерактивная мозаика» автор: Кудрявцева Ирина Александровна МОУ «Средняя общеобразовател
Конкурс интерактивных презентаций «Интерактивная мозаика» автор: Кудрявцева Ирина Александровна МОУ «Средняя общеобразовател Сплавы металлов
Сплавы металлов  Химический состав клетки. Неорганические вещества клетки. Глава 1
Химический состав клетки. Неорганические вещества клетки. Глава 1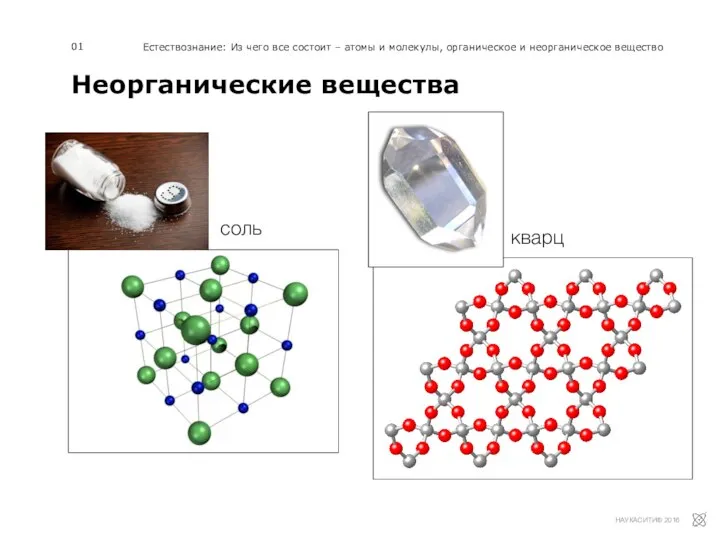 Неорганические вещества
Неорганические вещества Презентация по Химии "Исследование влияния токсикантов на активность ферментов на примере уреазы" - скачать смотреть бесплат
Презентация по Химии "Исследование влияния токсикантов на активность ферментов на примере уреазы" - скачать смотреть бесплат Соединения галогенов
Соединения галогенов Интегрированный урок по теме:
Интегрированный урок по теме: Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть
Презентация по Химии "Соединения серы (11 класс)" - скачать смотреть  Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций
Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций Алкины. Пропин
Алкины. Пропин Кристаллы. Монокристалл
Кристаллы. Монокристалл Полимеры, пластмассы и волокна
Полимеры, пластмассы и волокна Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Cвойства цементного камня с введением кольматирующей добавки системы Пенетрон-Адмикс
Cвойства цементного камня с введением кольматирующей добавки системы Пенетрон-Адмикс Математическое моделирование. Контурно-графический анализ
Математическое моделирование. Контурно-графический анализ Алкены. Химические свойства этилена
Алкены. Химические свойства этилена