Содержание
- 2. Актуальность: в настоящее время инфицирование при трансфузии крови и ее компонентов остается одной из серьезных проблем
- 3. Введение: Цель: Определить возможности систем на основе субстанции рибофлавина для разработки и промышленного производства отечественных систем
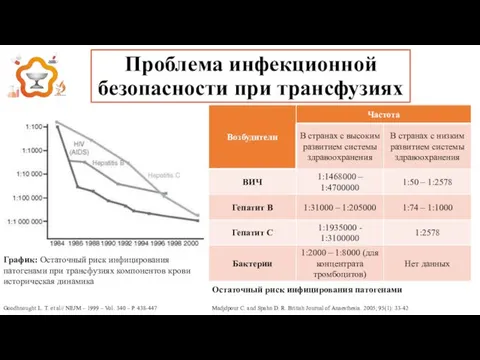
- 4. Проблема инфекционной безопасности при трансфузиях Goodhnought L. T. et al// NEJM – 1999 – Vol. 340
- 5. Методы преодоления инфекционных реакций при трансфузиях тщательный отбор доноров крови и ее компонентов пропаганда донорства с
- 6. Карантинизация Суть метода: компоненты крови выдаются в лечебные учреждения, только после повторного обследования доноров, через 4
- 7. Карантинизация Холодильная комната для карантинизации в ФГБУ «НМИЦ им. В. А. Алмазова» Свежезамороженная плазма
- 8. Патогенредукция Инактивация (редукция) патогенных биологических агентов» - технология обработки компонентов крови, направленная на прекращение репродукции патогенных
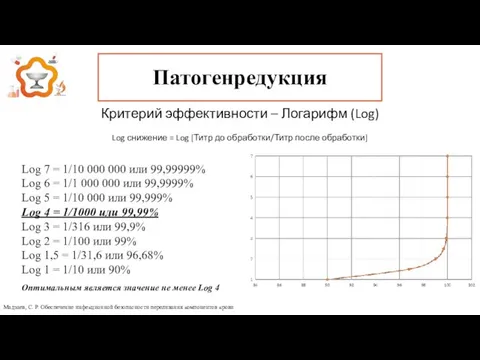
- 9. Патогенредукция Критерий эффективности – Логарифм (Log) Log снижение = Log [Титр до обработки/Титр после обработки] Log
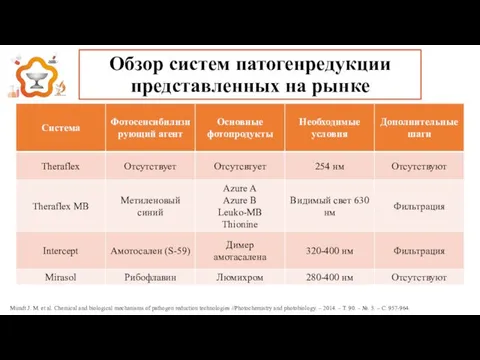
- 10. Обзор систем патогенредукции представленных на рынке Mundt J. M. et al. Chemical and biological mechanisms of
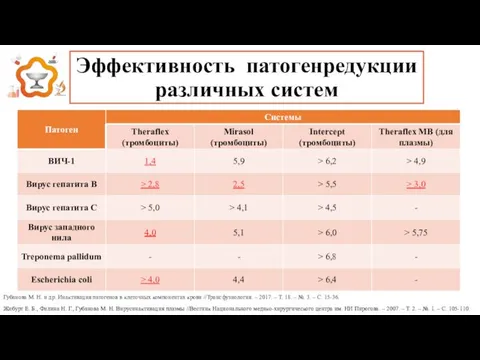
- 11. Эффективность патогенредукции различных систем Губанова М. Н. и др. Инактивация патогенов в клеточных компонентах крови //Трансфузиология.
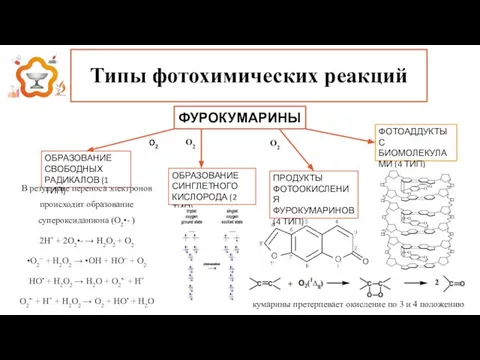
- 12. Типы фотохимических реакций ФУРОКУМАРИНЫ O2 O2 O2 ОБРАЗОВАНИЕ СВОБОДНЫХ РАДИКАЛОВ (1 ТИП) ОБРАЗОВАНИЕ СИНГЛЕТНОГО КИСЛОРОДА (2
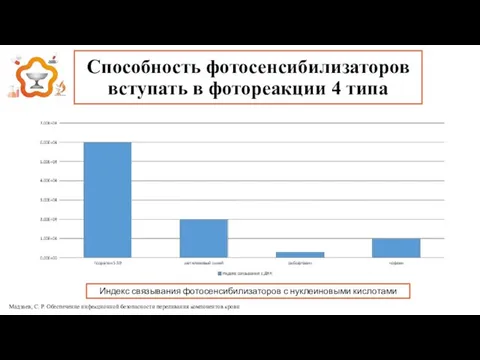
- 13. Способность фотосенсибилизаторов вступать в фотореакции 4 типа Мадзаев, С. Р. Обеспечение инфекционной безопасности переливания компонентов крови
- 14. Intercept, Cerus (US) Фотосенсибилизатор: амотосален Диапазон длин волн: 320-400 нм Реализует эффект благодаря фото реакциям 4
- 15. Mirasol, TerumoBCT (US) Фотосенсибилизатор: рибофлавин Эффект опосредован химическими реакциями 1 и 2 типа (происходит окисление остатков
- 16. Методы синтеза рибофлавина Существуют два метода синтеза: микробиологический и химический. Микробиологический является наиболее востребованным, так как
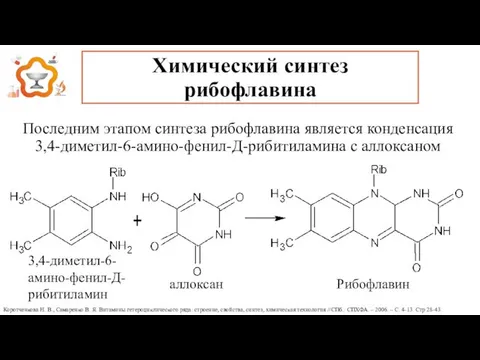
- 17. Химический синтез рибофлавина Последним этапом синтеза рибофлавина является конденсация 3,4-диметил-6-амино-фенил-Д-рибитиламина с аллоксаном аллоксан Рибофлавин 3,4-диметил-6-амино-фенил-Д-рибитиламин Коротченкова
- 18. Получение 4-о-ксилидина (один из методов, выход на о-ксилол 40%): Метод ацетилирования о-ксилола дейтсвием ацетилхлорида в присутствии
- 19. Химический синтез рибофлавина Получение 3,4-ксилил-Д-рибитиламина: Конденсация Д-рибозы с 4-о-ксилидином.
- 20. Химический синтез рибофлавина Получение 3,4-ксилил-Д-рибитиламина: Восстановление водородом образовавшегося в процессе конденсации «рибопиранозида» в присутствии скелетного никелевого
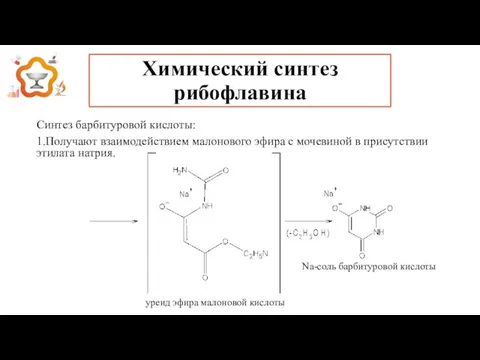
- 21. Химический синтез рибофлавина Синтез барбитуровой кислоты: 1.Получают взаимодействием малонового эфира с мочевиной в присутствии этилата натрия.
- 22. Химический синтез рибофлавина Синтез барбитуровой кислоты: 1.Получают взаимодействием малонового эфира с мочевиной в присутствии этилата натрия.
- 23. Рибофлавин в России В России синтезом рибофлавина по данным ГРЛС занимается завод «Полисан» в Белгороде. Завод
- 24. Theraflex, Macopharma (France) Фотосенсибилизатор: метиленовый голубой Вступает в фотохимические реакции 1, 2 и 4 типа Используется
- 25. Системы патогенредукции Mundt J. M. et al. Chemical and biological mechanisms of pathogen reduction technologies //Photochemistry
- 26. Исследование Анкета 1.Какие компоненты крови вы заготавливаете (множественный выбор) ? □ Плазма (B05AX03) □ Тромбоциты (B05AX02)
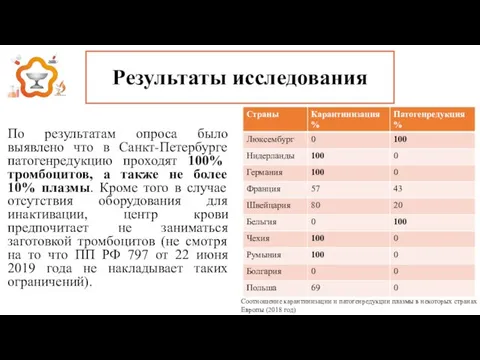
- 27. Результаты исследования По результатам опроса было выявлено что в Санкт-Петербурге патогенредукцию проходят 100% тромбоцитов, а также
- 28. Результаты исследования По результатам опроса выявлено: 2 центра не владеют ни одной системой патогенредукции 2 центра
- 29. Заключение Проведен обзор систем патогенредукции компонентов крови в отделениях трансфузиологии и станций переливаний крови Санкт-Петербурга. Установлен
- 30. Литература Goodhnought L. T. et al// NEJM – 1999 – Vol. 340 – P. 438-447 Madjdpour
- 31. Благодарность Выражаю благодарность: Кириллу Свечникову за красочные фотографии. Георгию Степанову и Юрию Литвинко за помощь в
- 33. Скачать презентацию





















 Ферменти. Історія вчення про ферменти
Ферменти. Історія вчення про ферменти Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии
Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии Диоксины, глобальные экотоксиканты
Диоксины, глобальные экотоксиканты Электроматериаловедение
Электроматериаловедение Мило. Синтетичні миючі засоби.
Мило. Синтетичні миючі засоби.  Аминокислоты
Аминокислоты Изменение в составе ядер атомов. Изотопы
Изменение в составе ядер атомов. Изотопы Презентация по Химии "Отчет по месячнику химии" - скачать смотреть
Презентация по Химии "Отчет по месячнику химии" - скачать смотреть  Дисперсные системы: общая характеристика и классификация
Дисперсные системы: общая характеристика и классификация Кристаллы
Кристаллы История развития контролируемой радикальной полимеризации. Управление ростом полимерной цепи нитроксильными радикалами
История развития контролируемой радикальной полимеризации. Управление ростом полимерной цепи нитроксильными радикалами Нитраты в продуктах
Нитраты в продуктах Антибиотики-аминогликозиды: получение, свойства, исследование и применение. Связь между химическим строением и действием
Антибиотики-аминогликозиды: получение, свойства, исследование и применение. Связь между химическим строением и действием Элементы химической термодинамики и биоэнергетики
Элементы химической термодинамики и биоэнергетики Алюминий – металл будущего
Алюминий – металл будущего Тема : Спирты Презентация по химии Ученицы 11 «Б» класса ЗОШ №41 Зануды Татьяны
Тема : Спирты Презентация по химии Ученицы 11 «Б» класса ЗОШ №41 Зануды Татьяны  Предельные углеводороды и их галогенопроизводные. Спирты, эфиры, альдегиды и их производные
Предельные углеводороды и их галогенопроизводные. Спирты, эфиры, альдегиды и их производные Полиазометины (полишиффовы основания)
Полиазометины (полишиффовы основания) Химия и производство. Химическая промышленность и химические технологии
Химия и производство. Химическая промышленность и химические технологии Химическое равновесие
Химическое равновесие Алкалоиды. Классификация алкалоидов:
Алкалоиды. Классификация алкалоидов: Растворы
Растворы Хімія та обмін ліпідів
Хімія та обмін ліпідів Водорастворимые витамины
Водорастворимые витамины Теория сплавов
Теория сплавов Серебро - химический элемент в периодической таблице с атомным номером 47. 8 класс
Серебро - химический элемент в периодической таблице с атомным номером 47. 8 класс Моя профессия химик-аналитик
Моя профессия химик-аналитик