Содержание
- 2. Пойдет ли процесс самопроизвольно — без воздействия извне — или он принципиально невозможен. Чтобы подойти к
- 3. Во многих случаях изменение энтропии процесса можно оценить качественно: • Энтропия всегда увеличивается при переходе из
- 4. Именно поэтому испарение жидкости, растворение соли в воде или смешение газов происходит самопроизвольно, а вместе с
- 5. Общее правило (калькуляция) – самопроизвольно протекают процессы в которых любая система стремится к минимуму энтальпии и
- 6. В термодинамике величину ΔG определяют как ΔG=ΔG0 + RT lnКравн Изменение энергии Гиббса (G) при наступлении
- 7. ФОРМАЛЬНАЯ КИНЕТИКА Итак, термодинамика позволяет с большой точностью предсказать принципиальную возможность протекания процесса и конечное состояние
- 8. Общие условия осуществления и свойства равновесных процессов : Бесконечно малая разность действующих и противодействующих сил. Совершение
- 9. В термодинамике учитывается только начальное и конечное состояния системы, но не рассматривается механизм перехода и не
- 10. ПОВТОРИМ ЕЩЕ РАЗ- термодинамическая возможность процесса (ΔG Однако термодинамический запрет на самопроизвольное протекание процесса (ΔG >
- 11. Можно выделить две главные задачи химической кинетики, определяющие ее практическое и теоретическое значение: экспериментальное исследование скорости
- 13. Скорость химической реакции зависит от множества факторов: природы реагирующих веществ, их концентрации, температуры, природы растворителя и
- 15. В связи с этим для элементарных реакций вводится понятие молекулярность – число молекул, принимающих участие в
- 18. Зависимость скорости химической реакции от температуры выражается правилом Вант-Гоффа. При повышении температуры на каждые 10° скорость
- 19. ФОРМАЛЬНАЯ КИНЕТИКА
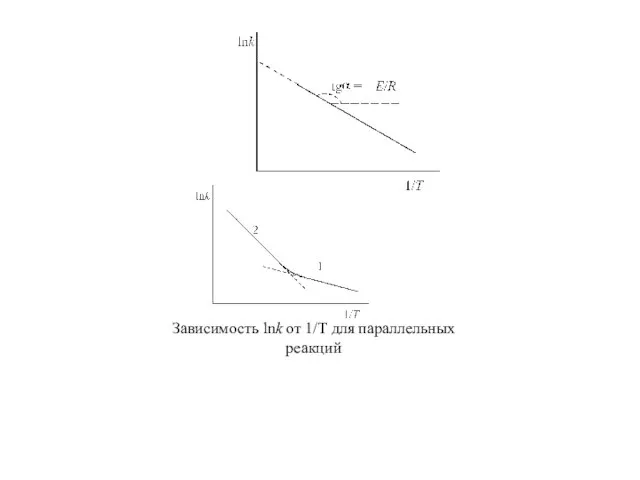
- 20. Зависимость lnk от 1/T для параллельных реакций
- 23. Подвод реагента осуществляется за счет диффузии . Так как энергия активации диффузии невелика, то при изменении
- 24. Рис. Температурная зависимость константы скорости гетерогенной химической реакции
- 25. Каталитические процесс Катализ – явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых
- 26. Причиной увеличения скорости реакции при положительном катализе является уменьшение энергии активации при протекании реакции через активированный
- 27. Гомогенный катализ – каталитические реакции, в которых реагенты и катализатор находятся в одной фазе. В случае
- 29. Скачать презентацию

























 Требования, особенности, оценка знаний по химии. ОГЭ - 2016
Требования, особенности, оценка знаний по химии. ОГЭ - 2016 Смазывающие вещества
Смазывающие вещества Водородная связь
Водородная связь Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены
Неметаллы. Положение неметаллов в ПСХЭ Д.И. Менделеева. Галогены Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований
Растворы и процессы, проходящие в растворах. Протолитическая теория кислот и оснований Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі
Металдар мен бейметалдар, олардың қосылыстарының қасиеттерінің период және топ бойынша өзгеруі Практическая работа по химии. Строение пламени
Практическая работа по химии. Строение пламени Эндогенная серия. Вулканогенно-осадочная группа
Эндогенная серия. Вулканогенно-осадочная группа Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД) Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп
Класифікація органічних сполук за будовою вуглецевого скелету та природою функціональних груп “Проценты”, “Массовая доля” при решении задач. Интегрированный урок химии и математики
“Проценты”, “Массовая доля” при решении задач. Интегрированный урок химии и математики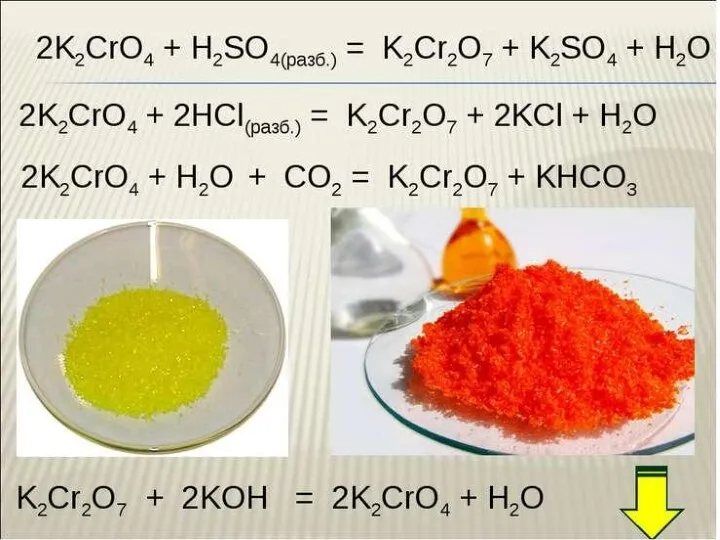 Хром. Соединения хрома
Хром. Соединения хрома История изучения структуры белка Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру
История изучения структуры белка Лайнус Полинг считается первым учёным, который смог успешно предсказать вторичную структуру Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен
Алкены. Строение. Изомерия. Химические свойства. Получение. Учитель химии ГОУ СОШ №277 Кировского района г. Санкт-Петербурга Елен Алкалоиды, как лекарственные вещества. Источники получения. Методы установления строения. Классификация. (Тема 9)
Алкалоиды, как лекарственные вещества. Источники получения. Методы установления строения. Классификация. (Тема 9) Типы изомерии
Типы изомерии Синтетические моющие средства
Синтетические моющие средства Кадмий (Cadmium)
Кадмий (Cadmium) Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян
Тема: «Бишофит – новый старый антигололедный реагент» Авторы: Гончаревич Анастасия Клокова Татьян Химия и физика полимеров. Курс лекций
Химия и физика полимеров. Курс лекций Строение вещества. Химические элементы
Строение вещества. Химические элементы Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны
Графен. Классические и квантовые низкоразмерные системы. Ковалентная химическая связь: σ- и π-электроны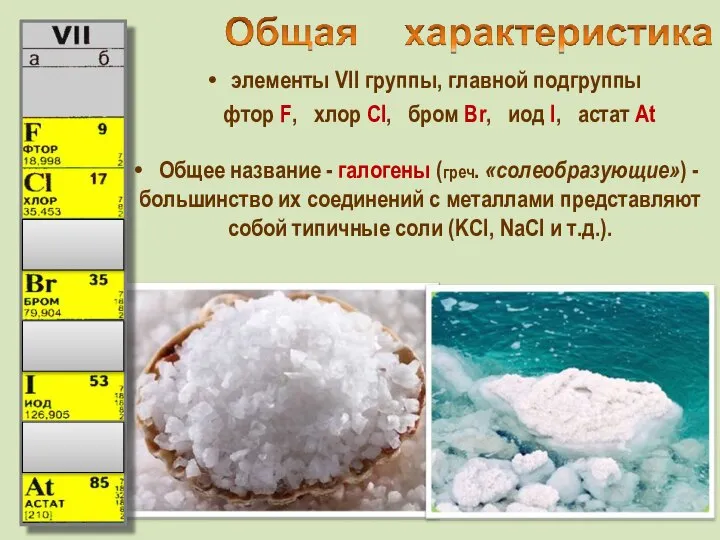 Элементы VII группы
Элементы VII группы Уроки зельеварения. Задача 6
Уроки зельеварения. Задача 6 Основные положения МКТ МКТ- молекулярно-кинетическая теория
Основные положения МКТ МКТ- молекулярно-кинетическая теория  Промышленное получение аминокислот и их применение в медицине и диетологии
Промышленное получение аминокислот и их применение в медицине и диетологии Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия
Положение кислорода и серы в Периодической системе химических элементов, строение атомов. Строение простых веществ. Аллотропия Физическая и коллоидная химия
Физическая и коллоидная химия