Содержание
- 2. Задачи: познакомиться с типами химических связей ; научиться определять по молекулярной формуле соединения тип связей в
- 3. Что такое химическая связь? Химическая связь - это взаимодействие атомов, которое связывает их в молекулы, ионы,
- 4. Различают четыре типа химических связей: Ионная связь. Ковалентная связь. Металлическая связь. Водородная связь.
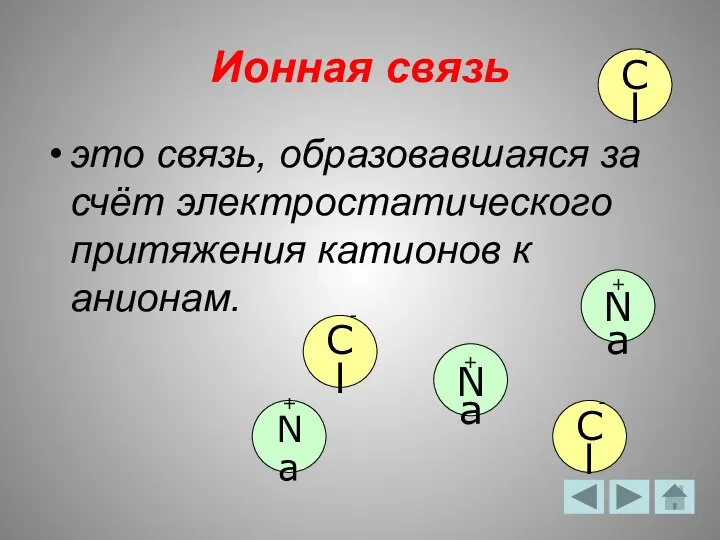
- 5. Ионная связь это связь, образовавшаяся за счёт электростатического притяжения катионов к анионам. + Na - Cl
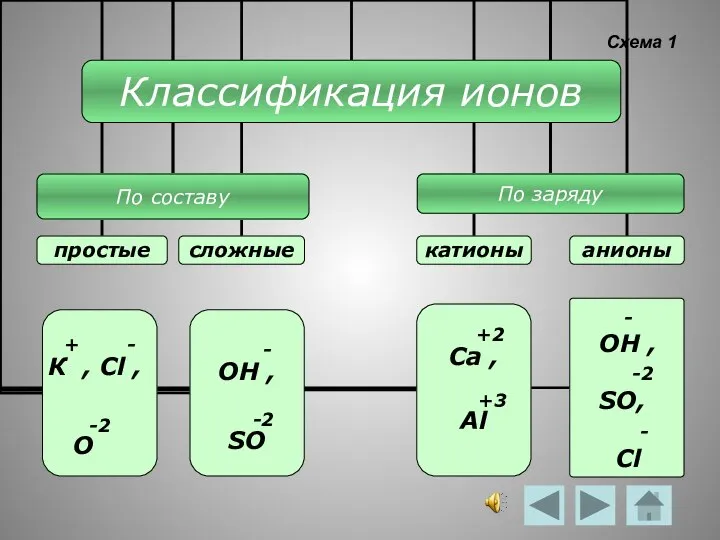
- 6. Схема 1 - ОН , -2 SO, - Cl
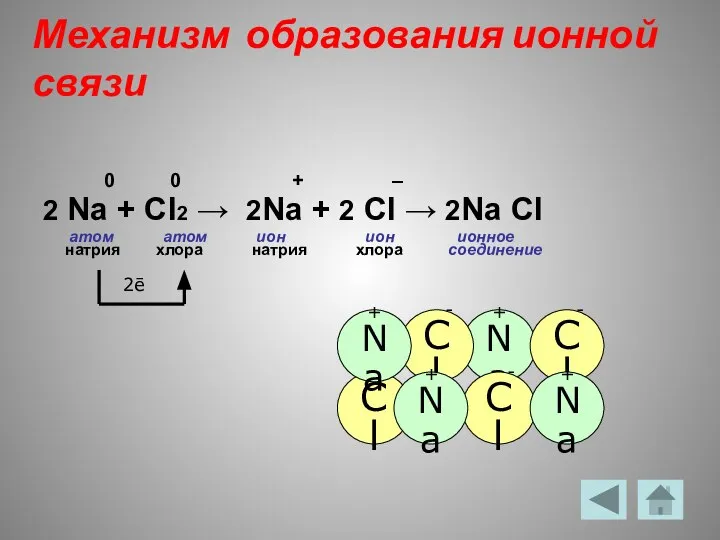
- 7. Механизм образования ионной связи 0 0 + – 2 Na + Cl2 → 2Na + 2
- 8. Ковалентная связь это связь, возникает между атомами за счёт образования общих электронных пар. ē ē ē
- 9. Схема 2 обменный донорно- акцепторный полярная неполярная σσ (сигма) – связь ππ (π (пиπ (пи)π (пи)
- 10. Обменный механизм образования ковалентной связи ☼ Действует, когда атомы образуют общие электронные пары за счёт объединения
- 11. Донорно-акцепторный механизм образования ковалентной связи ☼ Действует между веществами донором и акцептором. Донор – вещество, у
- 12. Степень смещения электронных пар ☼Зависит от ЭЛЕКТРООТРИЦАТЕЛЬНОСТИ элементов. Ряд электроотрицательности: F, O, N, C l, Br,
- 13. Кратность ковалентной связи ☼Зависит от числа общих электронных пар, связывающих атомы. Бывает: ПРОСТАЯ « - »
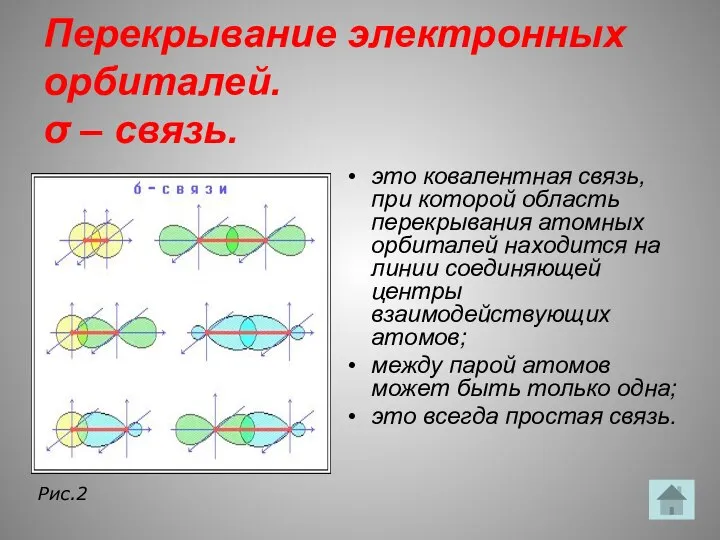
- 14. Перекрывание электронных орбиталей. σ – связь. это ковалентная связь, при которой область перекрывания атомных орбиталей находится
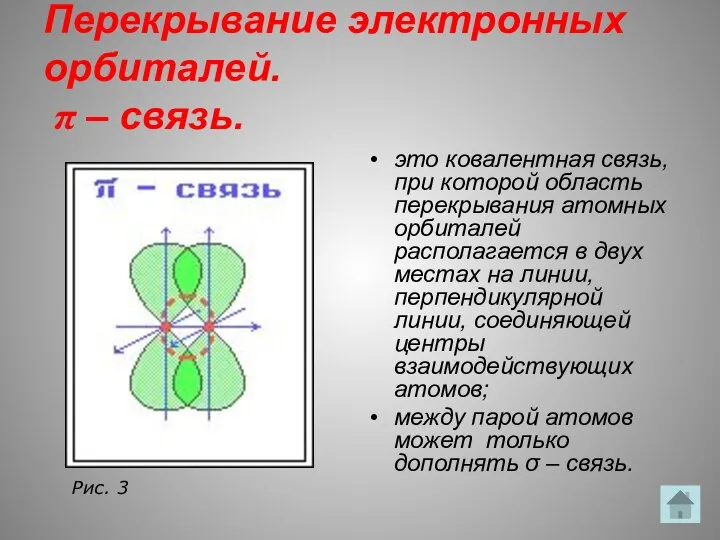
- 15. Перекрывание электронных орбиталей. π – связь. это ковалентная связь, при которой область перекрывания атомных орбиталей располагается
- 16. Металлическая связь это связь, которую осуществляют относительно свободные электроны между ионами металлов в металлической решётке. n+
- 17. Механизм образования металлической связи: 0 n+ М - nē = М Например: для элементов (металлов) Ι
- 18. Водородная связь Межмолекулярная водородная связь – это связь между атомами водорода одной молекулы и сильноотрицательными элементами(O,
- 20. Скачать презентацию












 Уравнение Г-Х-К для мембранного потенциала
Уравнение Г-Х-К для мембранного потенциала Связующие для полимерных композиционных материалов. (Тема 2)
Связующие для полимерных композиционных материалов. (Тема 2) Закон действующих масс и его применение к различным типам равновесий
Закон действующих масс и его применение к различным типам равновесий Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3)
Основные положения теории растворов электролитов, используемых в аналитической химии. (Лекция 3) Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна
Тема урока: «Химический элемент - водород» Подготовила: Михно Валерия 9 «В» класс Учитель: Назаренко Любовь Дмитриевна  Бензол: строение и свойства
Бензол: строение и свойства Чистящие и моющие средства для мытья посуды
Чистящие и моющие средства для мытья посуды Гетероциклические соединения
Гетероциклические соединения Термодинамика химических процессов
Термодинамика химических процессов Литосфера. Физико-химические процессы в литосфере
Литосфера. Физико-химические процессы в литосфере Бронза. Свойства
Бронза. Свойства Учитель химии МОУ СОШ №18 Лаврик Виктория Александровна
Учитель химии МОУ СОШ №18 Лаврик Виктория Александровна  Кремний и его соединения
Кремний и его соединения Нуклеиновые кислоты
Нуклеиновые кислоты Энергетический обмен в клетке - катаболизм
Энергетический обмен в клетке - катаболизм Необратимые электродные процессы. Часть 1
Необратимые электродные процессы. Часть 1 Презентация по химии Теоретические основы аналитической химии Химическое равновесие в гомогенной системе
Презентация по химии Теоретические основы аналитической химии Химическое равновесие в гомогенной системе  Влияние межмолекулярных F…F контактов на энергию кристаллической решетки металлоорганических комплексов Ge
Влияние межмолекулярных F…F контактов на энергию кристаллической решетки металлоорганических комплексов Ge Строение электронной оболочки атома
Строение электронной оболочки атома Формы парфюмерно-косметической продукции
Формы парфюмерно-косметической продукции Щелочные и щелочно-земельные металлы Na K Li Cs Ba Rb Fr
Щелочные и щелочно-земельные металлы Na K Li Cs Ba Rb Fr  Одноатомні спирти Підготували Учениці 9-Б класу
Одноатомні спирти Підготували Учениці 9-Б класу  Оценка химической обстановки при авариях на химически опасных объектах
Оценка химической обстановки при авариях на химически опасных объектах Температура и тепловое равновесие
Температура и тепловое равновесие Повторительное обобщение по неорганической химии, подготовка к ГИА
Повторительное обобщение по неорганической химии, подготовка к ГИА Химическое равновесие
Химическое равновесие Абсолютное первенство по химии
Абсолютное первенство по химии Рідкі кристали та їх властивості Класифікація та застосування
Рідкі кристали та їх властивості Класифікація та застосування