Содержание
- 2. Порядковый номер: 6 Строение атома: р – 6, n – 6, е – 6 Энергетических уровней:
- 3. +6С )2)4 +14Si )2)8)4 +32Ge )2)8)18)4 +50Sn )2)8)18)18)4 +82Pb )2)8)18)32)18)4 Общая электронная формула внешнего слоя S2
- 4. С Si Ge Sn Pb Металлические свойства увеличиваются Подгруппа углерода
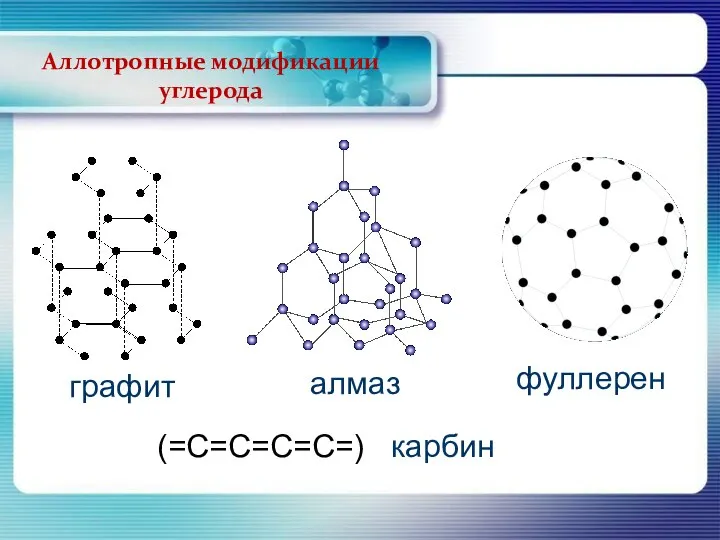
- 5. Аллотропные модификации углерода графит алмаз фуллерен (=С=С=С=С=) карбин
- 6. А л м а з
- 7. Звезда ордена Св. Андрея Первозванного Алмаз «Шах» Скипетр императорский А л м а з
- 8. Большая императорская корона Малая императорская корона А л м а з
- 9. Г р а ф и т Применение графита: Электроды для электролиза Облицовка сопел ракетных двигателей Стержни
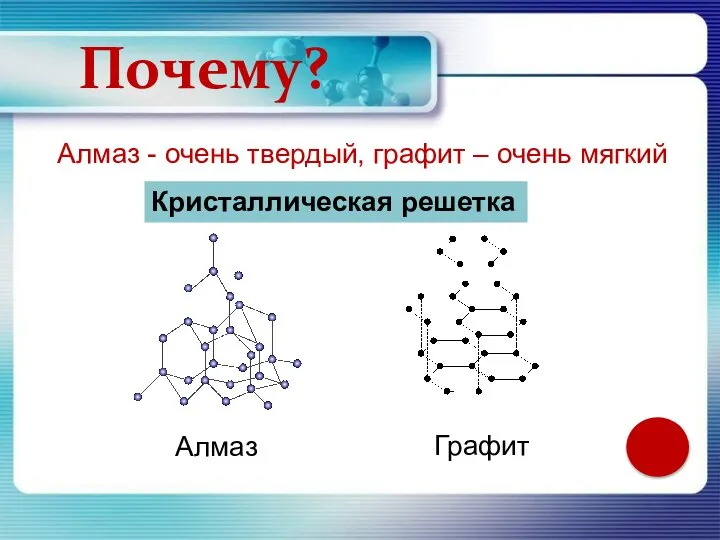
- 10. Алмаз - очень твердый, графит – очень мягкий Кристаллическая решетка Почему? Алмаз Графит
- 11. Алмаз имеет атомную кристаллическую решетку, в которой каждый атом углерода связан с четырьмя атомами. В пространстве
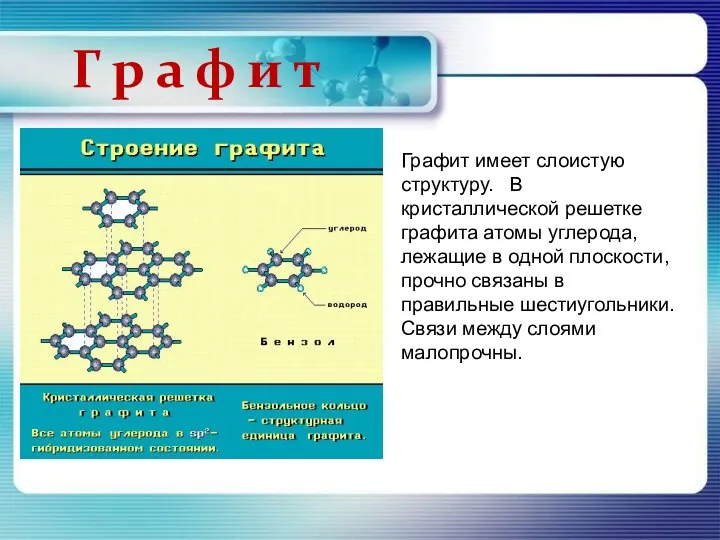
- 12. Графит имеет слоистую структуру. В кристаллической решетке графита атомы углерода, лежащие в одной плоскости, прочно связаны
- 13. Сходное с графитом строение имеют: Сажа Древесный уголь Кокс типографская краска, картриджи, резина, косметическая тушь восстановитель
- 14. Н.Д. Зелинский Уголь - адсорбент Адсорбция – способность поглощать вещества
- 15. Угольные фильтры В бытовых фильтрах, в промышленном производстве, на очистных сооружениях – уголь поглощает вредные вещества
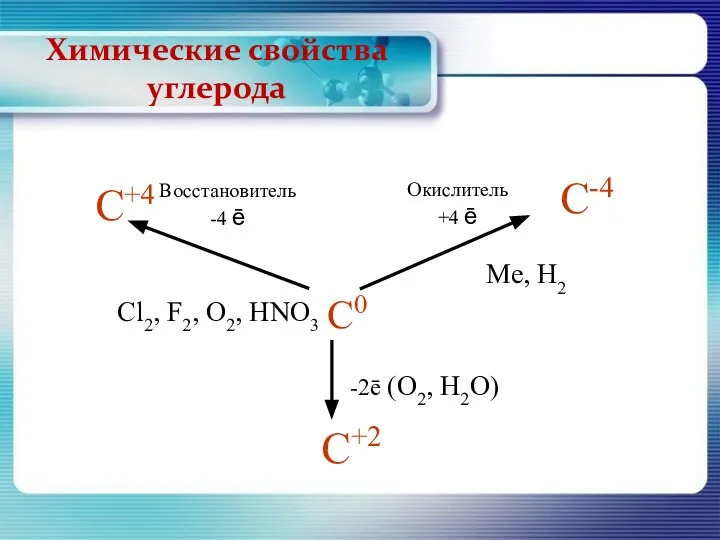
- 16. Химические свойства углерода
- 17. Химические свойства углерода В реакциях с активными неметаллами углерод легко окисляется: C+O2→CO2 2C+O2→2CO C+2S→CS2 C+2F2→CF4
- 18. Химические свойства углерода Углерод может проявлять восстановительные свойства и при взаимодействии со сложными веществами: C+2CuO→2Cu+CО2 C+2H2SO4(конц.)
- 19. Химические свойства углерода В реакциях с металлами и менее активными неметаллами углерод - окислитель: 2C+H2→C2H2 C+Si→SiC
- 20. Решите тест: 1. Конфигурация внешнего электронного уровня элементов подгруппы углерода: а) ns2np2 б) ns2np3 в) ns2np4
- 21. 4. Углерод является: а) восстановителем б) восстановителем и окислителем в) окислителем г) не проявляет окислительно-восстановительных свойств
- 22. Ответы:
- 24. Скачать презентацию

















 Химия және медицина
Химия және медицина Colloid chemistry
Colloid chemistry Показатель активности водородных ионов. Лабораторная работа №4
Показатель активности водородных ионов. Лабораторная работа №4 Растворы. Теория электролитической диссоциации
Растворы. Теория электролитической диссоциации Пищевые жиры
Пищевые жиры  Биохимия витаминов. Водорастворимые витамины. (Лекция 21)
Биохимия витаминов. Водорастворимые витамины. (Лекция 21) Презентация к уроку химии в 8 классе « Вещество» Учитель химии МКОУ СОШ с.Айлино Савельева Н.А.
Презентация к уроку химии в 8 классе « Вещество» Учитель химии МКОУ СОШ с.Айлино Савельева Н.А. Нанотехнологии в химии
Нанотехнологии в химии  Шкала рН. Лекция 03-1
Шкала рН. Лекция 03-1 Исследовательская работа на тему: Лед и соль
Исследовательская работа на тему: Лед и соль Магний. Магний алудың электролиттік жолы. Магний алудың термиялық жолдары
Магний. Магний алудың электролиттік жолы. Магний алудың термиялық жолдары Физические свойства
Физические свойства Аминокислоты
Аминокислоты Счастливы вместе с химией
Счастливы вместе с химией Строение электронных оболочек атомов
Строение электронных оболочек атомов Производные изохинолина
Производные изохинолина Математический аппарат квантовой механики
Математический аппарат квантовой механики Реологические методы исследования пищевых продуктов
Реологические методы исследования пищевых продуктов Основные свойства материалов
Основные свойства материалов Карбоновые кислоты
Карбоновые кислоты Алкины. Физические и химические свойства
Алкины. Физические и химические свойства Функціональні матеріали для високоенергетичної електроніки. (Лекція 1)
Функціональні матеріали для високоенергетичної електроніки. (Лекція 1) Презентация по Химии "Жиры животных" - скачать смотреть
Презентация по Химии "Жиры животных" - скачать смотреть  Состав и свойства нефти
Состав и свойства нефти Олигонуклеотидный синтез
Олигонуклеотидный синтез Полусинтетическое масло
Полусинтетическое масло Крахмал (C6H10O5)n
Крахмал (C6H10O5)n  Аминокислоты
Аминокислоты