Содержание
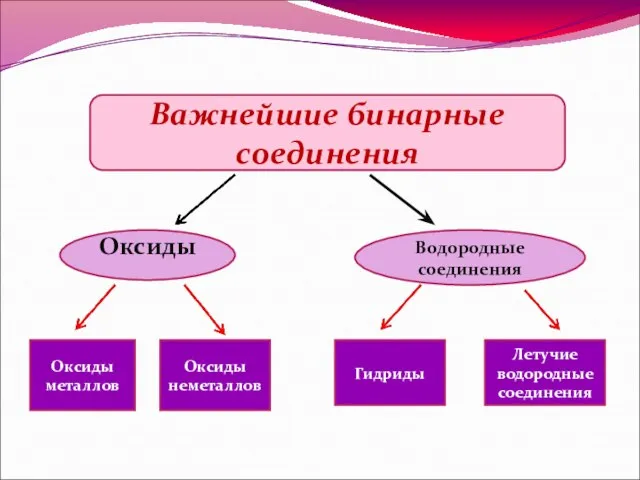
- 2. Важнейшие бинарные соединения Оксиды Водородные соединения Оксиды металлов Оксиды неметаллов Гидриды Летучие водородные соединения
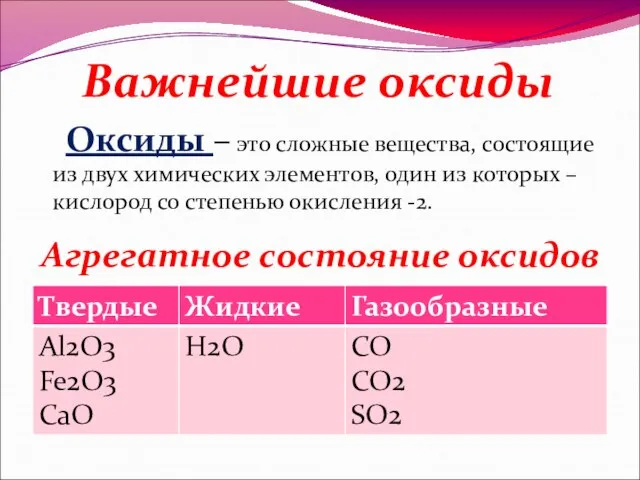
- 3. Оксиды – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород со
- 4. Красный железняк Fe2O3 Оксид железа (III) Синонимы: красный железняк, кровавик, черный.. Fe2O3, или красный железняк
- 5. МАГНИТНЫЙ ЖЕЛЕЗНЯК Fe2O4 Магнитный камень (магнитный железняк) Магнетит, он же магнитный железняк
- 6. КРЕМНЕЗЁМ (КВАРЦЕВЫЙ ПЕСОК) SiO2 oксид кремния (IV) Кварцевый песок - желтый Кварцевый песок - белый
- 7. Негашенная известь СаО оксид кальция (II)
- 8. Применение СаО
- 9. Вода H2O оксид водорода Особенности воды: Имеет три агрегатных состояния – жидкость, лед, пар; Обладает большой
- 10. Вода в природе:
- 11. Вода в промышленности:
- 12. Углекислый газ СО2 оксид углерода (IV) Образуется при: При дыхании; При гниении и тлении органических веществ;
- 13. СО2 оксид углерода (IV)
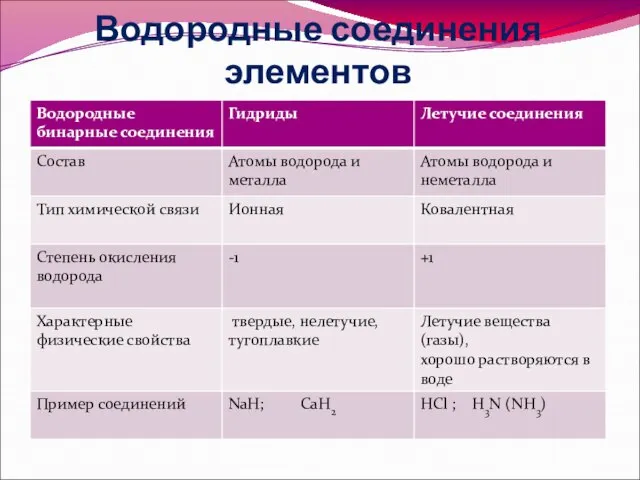
- 14. Водородные соединения элементов
- 15. Хлороводород HCl Свойства хлороводорода: Бесцветный газ; Тяжелее воздуха; На воздухе дымит; Хорошо растворим в воде –
- 16. Аммиак NH3 Свойства аммиака: 1. Бесцветный газ; 2. В два раза легче воздуха; 3. Хорошо растворяется
- 17. Выполните задания: Задание 1. Назовите вещества, имеющие формулы: CaO, Fe2O3, CO, SO2. Расставьте степени окисления. Задание
- 18. Задание 3. Какие названия соответствуют формуле СО2: а) оксид углерода (II) б) карбид кислорода (II) в)
- 19. Задание 5. Используя текст учебника найдите названия и формулы веществ, о которых идет речь: 1. вещество
- 21. Скачать презентацию















 Соли. Состав и номенклатура
Соли. Состав и номенклатура Аттестационная работа. Проектно - исследовательская технология, как способ формирования УУД по химии
Аттестационная работа. Проектно - исследовательская технология, как способ формирования УУД по химии студентка группы ГЭ-1-07 факультета ЭиУ Малышева Е.И. «Биомасса – альтернативный источник энергии» студентка группы ГЭ-1-07 фак
студентка группы ГЭ-1-07 факультета ЭиУ Малышева Е.И. «Биомасса – альтернативный источник энергии» студентка группы ГЭ-1-07 фак Углеводы
Углеводы Простые вещества металлы
Простые вещества металлы Уроки зельеварения. Задача 6
Уроки зельеварения. Задача 6 Матчворк Підготувала учениця 11-А класу Шведюк Людмила
Матчворк Підготувала учениця 11-А класу Шведюк Людмила  Уран. Получение урана
Уран. Получение урана Азот
Азот Сера
Сера В чем секрет любви к мороженому ?
В чем секрет любви к мороженому ? Литье под давлением реактопластов
Литье под давлением реактопластов Олигомеризация олефинов
Олигомеризация олефинов Кристаллография. Точечные группы симметрии, принцип их вывода с помощью понятия о группах. Формы кристаллов низшей категории
Кристаллография. Точечные группы симметрии, принцип их вывода с помощью понятия о группах. Формы кристаллов низшей категории Теоретические основы технологии неорганических веществ. (Тема 2)
Теоретические основы технологии неорганических веществ. (Тема 2) Химия биогенных элементов p -блока
Химия биогенных элементов p -блока Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды Азотная кислота – HNO3 – «взрывоопасная царская особа» МБОУ «Рождественская средняя общеобразовательная школа» Собинско
Азотная кислота – HNO3 – «взрывоопасная царская особа» МБОУ «Рождественская средняя общеобразовательная школа» Собинско Высокомолекулярные вещества
Высокомолекулярные вещества Фосфор и его соединения
Фосфор и его соединения Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Амфотерні гідроксиди
Амфотерні гідроксиди Презентация по Химии "Природні І синтетичні Органічні речовини" - скачать смотреть бесплатно
Презентация по Химии "Природні І синтетичні Органічні речовини" - скачать смотреть бесплатно Эндогенная серия. Карбонатитовая группа
Эндогенная серия. Карбонатитовая группа Поверхностные явления
Поверхностные явления Коррозия металлов
Коррозия металлов Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері
Химиялық, принципиалдық және технологиялық сызбанұсқалар. Технологиялқ процестерді ұйымдастыру принциптері Реактор получения элементарной серы
Реактор получения элементарной серы