Содержание
- 2. Степень окисления — это тот заряд атома, который возникает при условии, что электронные пары его связей
- 3. МЕТОДЫ ВОССТАНОВЛЕНИЯ И ОКИСЛЕНИЯ Многочисленные методы восстановления и окисления можно разделить на четыре группы: химические, каталитические,
- 4. ХИМИЧЕСКИЕ МЕТОДЫ ВОССТАНОВЛЕНИЯ 1.Востановление металлами и их солями Щелочными металлами (натрием). Оловом и хлоридом олова(II) в
- 5. Восстановление натрием в спирте, в жидком аммиаке и в виде амальгамы Восстанавливающая способность увеличивается от метода
- 6. Механизм восстановления натрием во всех случаях одинаков: атомы натрия отдают электроны, источником протонов является спирт, аммиак
- 7. Технология восстановления щелочными металлами Методики восстановления простые, но опасные (например, к кипящему раствору сложного эфира в
- 8. Технология восстановления амальгамой натрия Амальгаму натрия получают растворением натрия в ртути, что вызывает дополнительные трудности (отвод
- 9. Восстановление оловом, хлоридом олова (II) и железом в кислой среде, цинком в кислой и щелочной средах
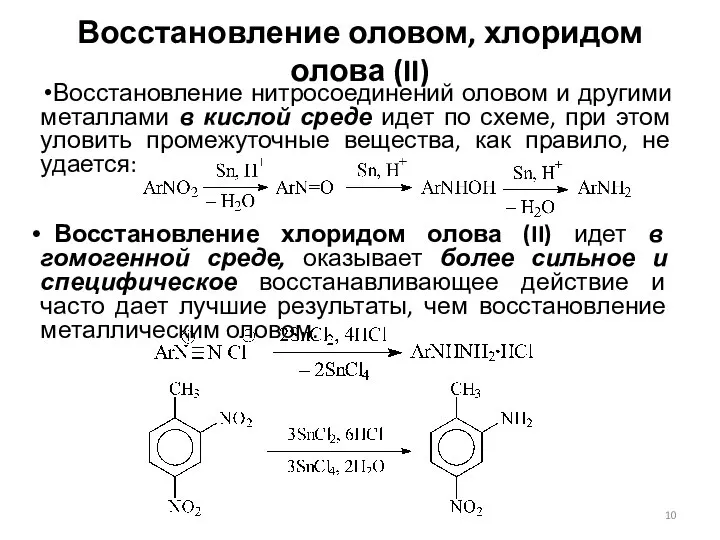
- 10. Восстановление оловом, хлоридом олова (II) Восстановление нитросоединений оловом и другими металлами в кислой среде идет по
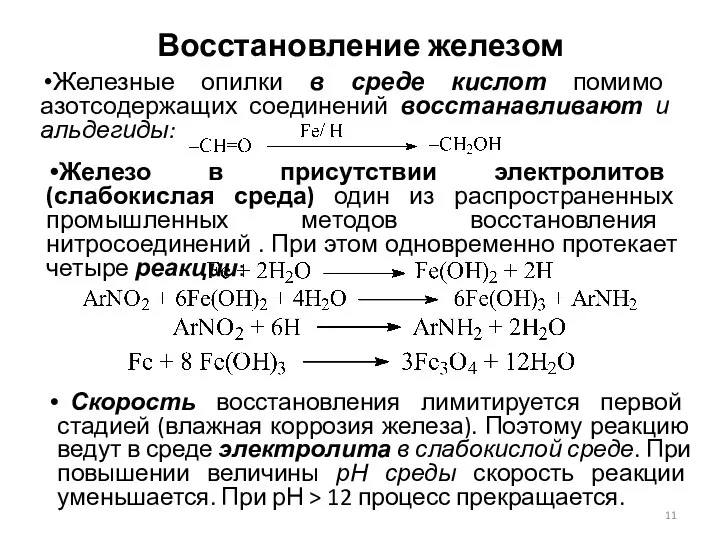
- 11. Восстановление железом Железные опилки в среде кислот помимо азотсодержащих соединений восстанавливают и альдегиды: Железо в присутствии
- 12. Технология восстановления железом в электролитах Электролиты (хлорид аммония, железа (II), и др.) можно получать в самом
- 13. Достоинства и недостатки восстановления железом в электролитах Метод - простотой, технологичный, дешевый, высокий выход. Недостаток метода
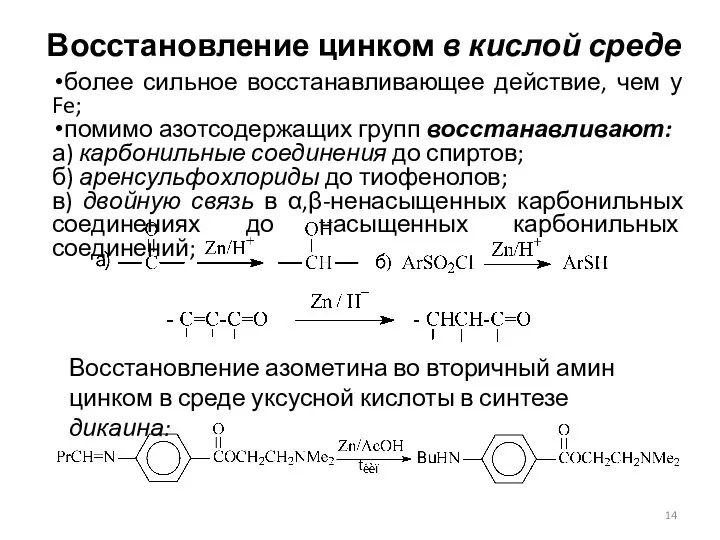
- 14. Восстановление цинком в кислой среде более сильное восстанавливающее действие, чем у Fe; помимо азотсодержащих групп восстанавливают:
- 15. Восстановление цинком в щелочной среде Нитроарены и другие производные, содержащие атом азота в щелочной среде восстанавливаются
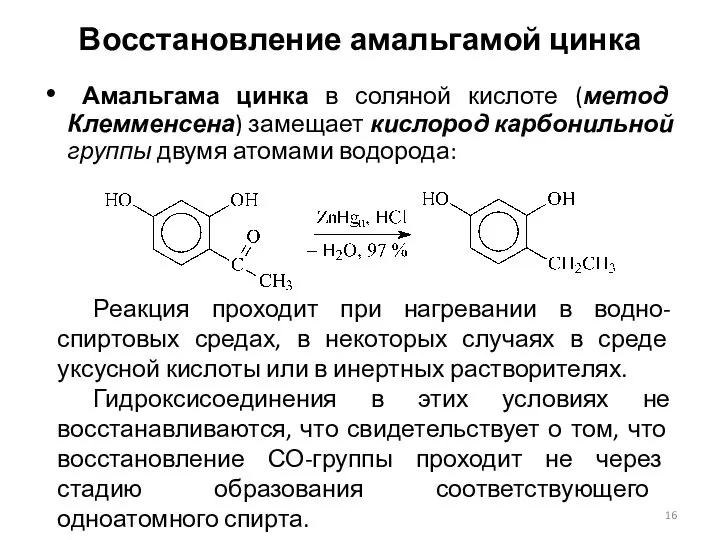
- 16. Восстановление амальгамой цинка Амальгама цинка в соляной кислоте (метод Клемменсена) замещает кислород карбонильной группы двумя атомами
- 17. Восстановление гидридами металлов сильные восстановители (LiAlH4 и NaBH4), используются для восстановления полярных двойных связей углерод–гетероатом, в
- 18. Алюмогидрид лития восстанавливает : не восстанавливает двойные связи углерод–углерод. Восстановление алюмогидридом лития - протекает в безводной
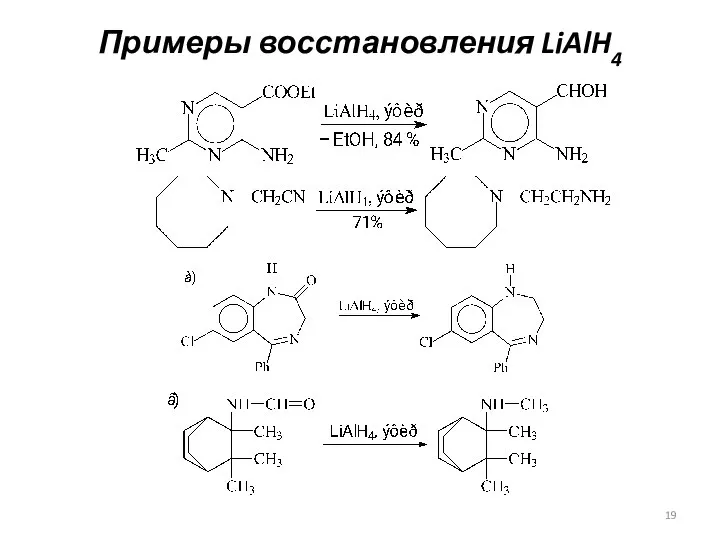
- 19. Примеры восстановления LiAlH4
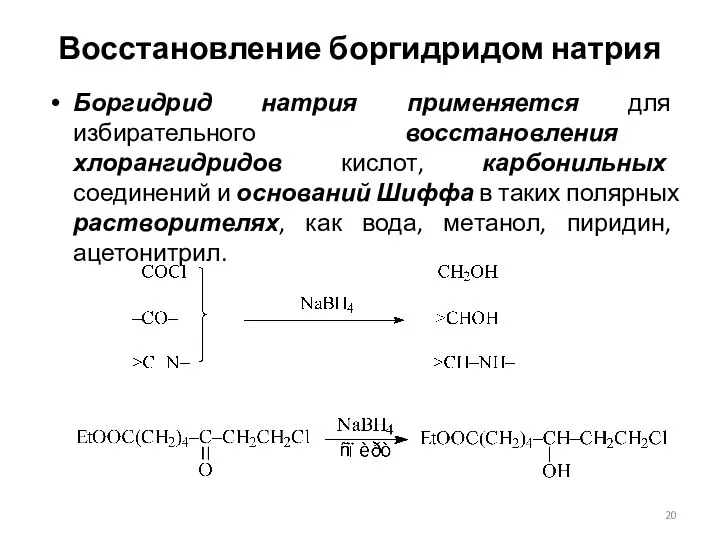
- 20. Восстановление боргидридом натрия Боргидрид натрия применяется для избирательного восстановления хлорангидридов кислот, карбонильных соединений и оснований Шиффа
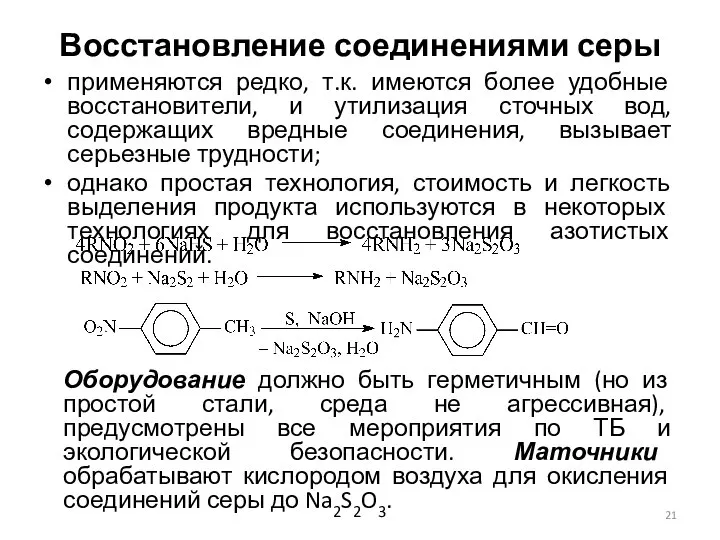
- 21. Восстановление соединениями серы применяются редко, т.к. имеются более удобные восстановители, и утилизация сточных вод, содержащих вредные
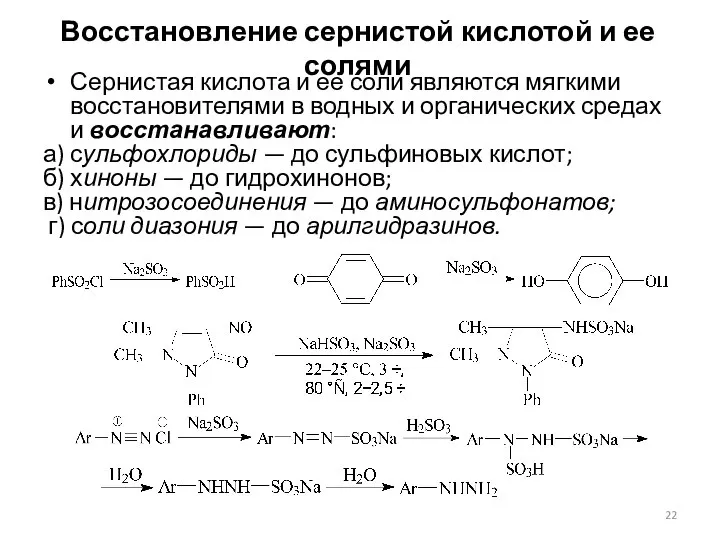
- 22. Восстановление сернистой кислотой и ее солями Сернистая кислота и ее соли являются мягкими восстановителями в водных
- 23. Восстановление алкоголятами алюминия Методом Меервейна-Понндорфа-Верлея) восстанавливают карбонильные соединения в спирты, не затрагивая другие функциональные группы. Алюминий
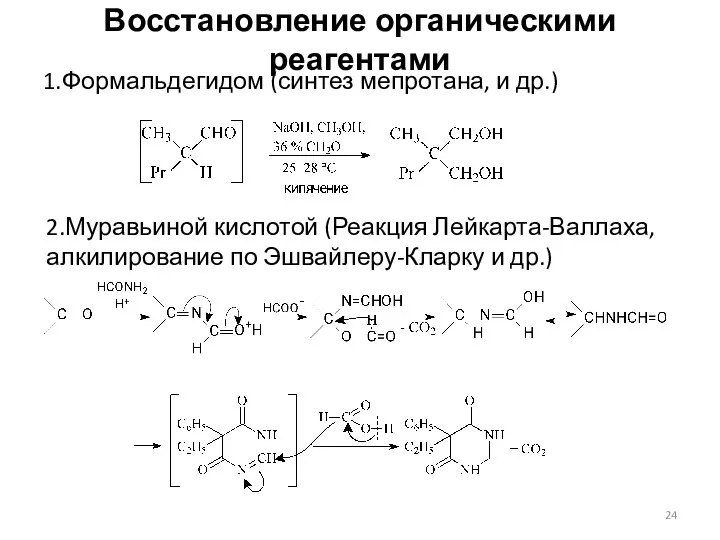
- 24. Восстановление органическими реагентами 1.Формальдегидом (синтез мепротана, и др.) 2.Муравьиной кислотой (Реакция Лейкарта-Валлаха, алкилирование по Эшвайлеру-Кларку и
- 25. Каталитическое восстановление водородом Достоинства: универсальность, высокая скорость процесса, высокий выход продукта, чистота получаемых продуктов и простота
- 26. Катализаторы В химико-фармацевтической промышленности широко применяют скелетный катализатор никель Ренея при нагревании в автоклавах, реже платиновые
- 28. Скачать презентацию
















 Каталіз: каталітичне гідрування
Каталіз: каталітичне гідрування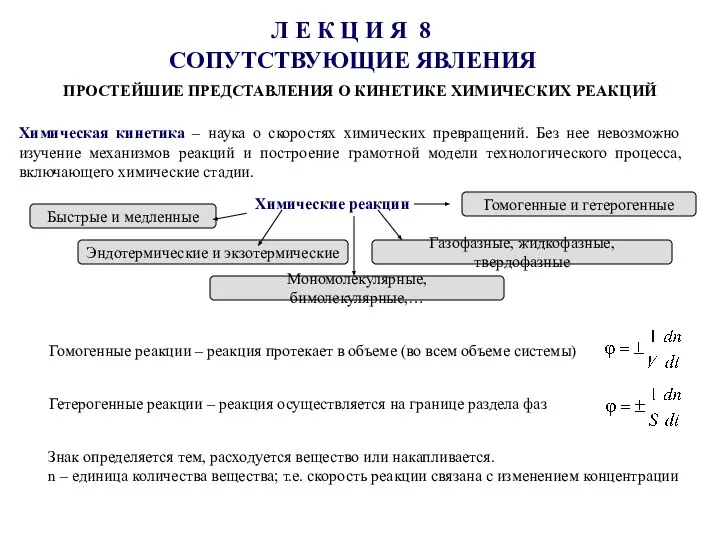 Простейшие представления о кинетике химических реакций
Простейшие представления о кинетике химических реакций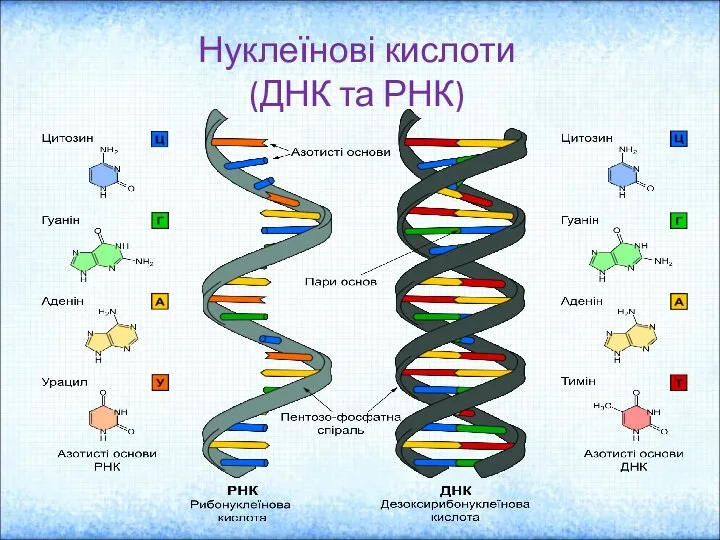 Нуклеїнові кислоти (ДНК та РНК)
Нуклеїнові кислоти (ДНК та РНК)  Фазовые и агрегатные состояния полимеров
Фазовые и агрегатные состояния полимеров Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Синергизм и синергические системы
Синергизм и синергические системы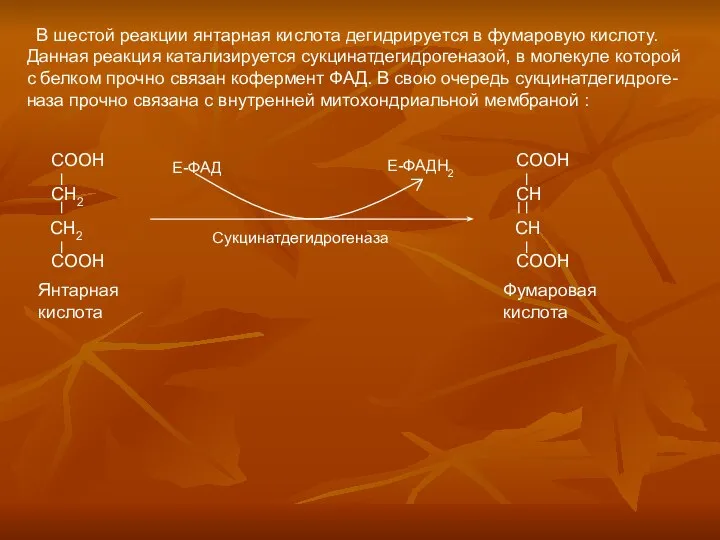 Аэробное окисление углеводов. (Часть 2)
Аэробное окисление углеводов. (Часть 2) Бейорганикалық заттар технологиясындағы жүйелерді термодинамикалық талдау
Бейорганикалық заттар технологиясындағы жүйелерді термодинамикалық талдау Соли. Классификация сложных веществ
Соли. Классификация сложных веществ Сахароза
Сахароза Соли «Na2SO4»
Соли «Na2SO4» Электролитическая диссоциация химических элементов Урок - лекция
Электролитическая диссоциация химических элементов Урок - лекция Аттестационная работа. Методическая разработка по выполнению проекта Анализ содержания ионов железа (III) в пищевых продуктах
Аттестационная работа. Методическая разработка по выполнению проекта Анализ содержания ионов железа (III) в пищевых продуктах Хімічна небезпека: походження, джерела та дії при хімічних забрудненнях
Хімічна небезпека: походження, джерела та дії при хімічних забрудненнях  Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Курс хімії за 11 клас
Курс хімії за 11 клас Предмет физической и коллоидной химии. Термодинамика
Предмет физической и коллоидной химии. Термодинамика Термодинамика и теплопередача. Реальные газы
Термодинамика и теплопередача. Реальные газы Рідкі кристали та їх властивості Підготувала Кравченко Дарина
Рідкі кристали та їх властивості Підготувала Кравченко Дарина  Александр Михайлович БУТЛЕРОВ Презентация учителя химии школы №122 Центрального р-на Санкт-Петербурга Поспеловой Светланы Викто
Александр Михайлович БУТЛЕРОВ Презентация учителя химии школы №122 Центрального р-на Санкт-Петербурга Поспеловой Светланы Викто Кристаллические решетки
Кристаллические решетки Метаморфические породы
Метаморфические породы Соли, как производные кислот и оснований. Их состав и номенклатура
Соли, как производные кислот и оснований. Их состав и номенклатура Омега 3
Омега 3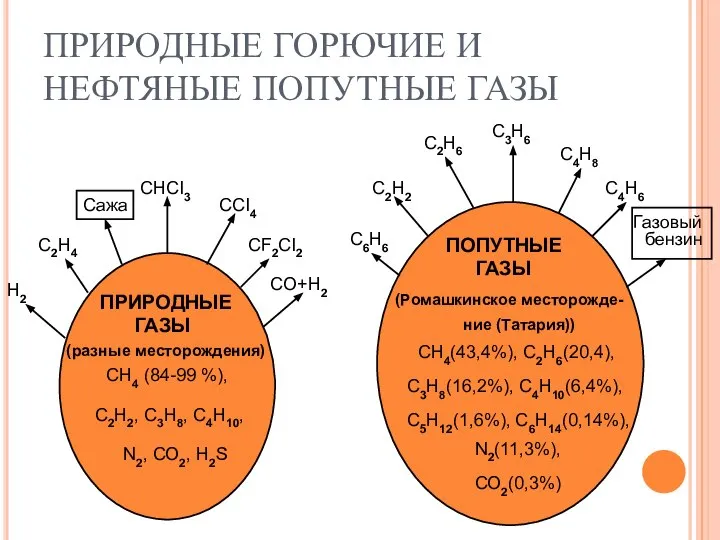 ПРИРОДНЫЕ ГОРЮЧИЕ И НЕФТЯНЫЕ ПОПУТНЫЕ ГАЗЫ
ПРИРОДНЫЕ ГОРЮЧИЕ И НЕФТЯНЫЕ ПОПУТНЫЕ ГАЗЫ  Химическая кинетика и катализ
Химическая кинетика и катализ Важнейшие нефтепродукты. Области их применения
Важнейшие нефтепродукты. Области их применения Кристаллические решетки
Кристаллические решетки