Содержание
- 2. Общая характеристика органических соединений Органические соединения являются производными углерода; Углерод в органических соединениях образует четыре ковалентные
- 3. Для органических соединений характерна изомерия: имея одинаковый химический состав, молекулы могут обладать различным пространственным строением и
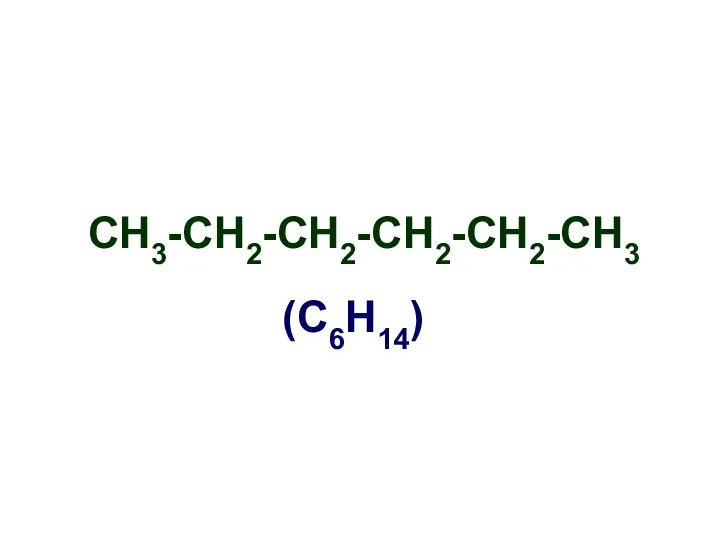
- 4. СН3-СН2-СН2-СН2-СН2-СН3 (С6Н14)
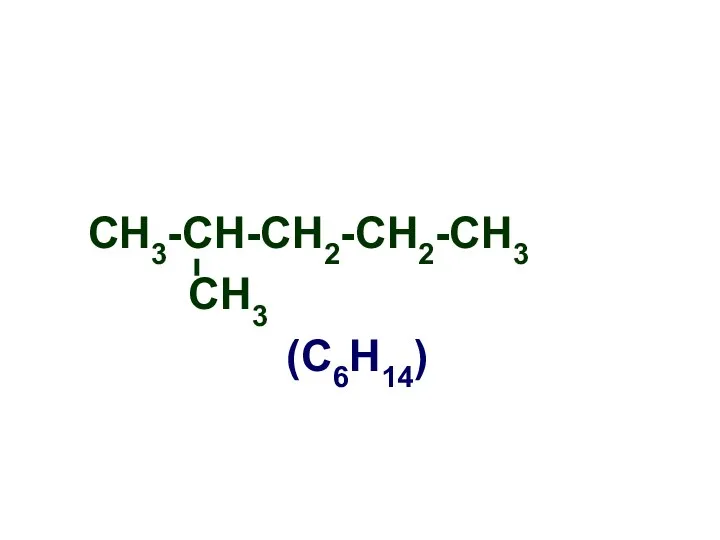
- 5. СН3-СН-СН2-СН2-СН3 СН3 (С6Н14)
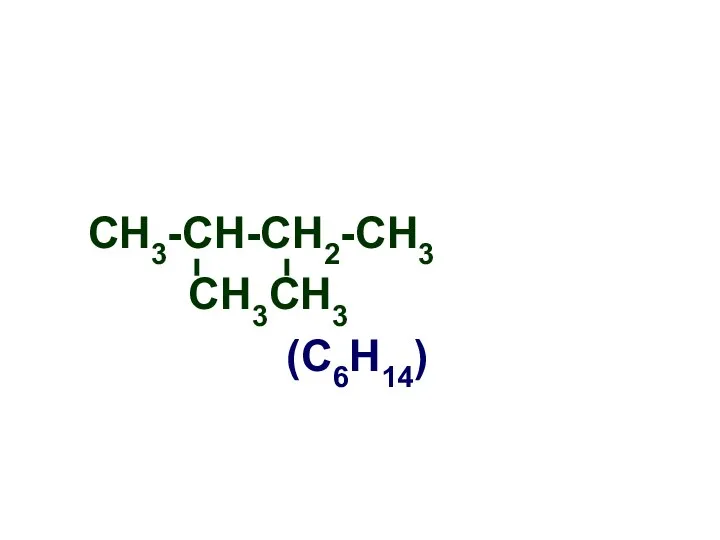
- 6. СН3-СН-СН2-СН3 СН3СН3 (С6Н14)
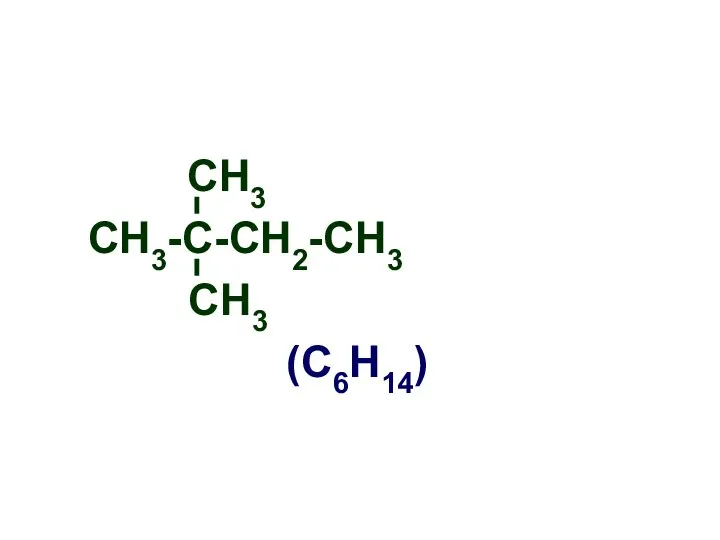
- 7. СН3-С-СН2-СН3 СН3 (С6Н14) СН3
- 8. Углеводороды В зависимости от наличия или отсутствия двойных и тройных связей углеводороды делятся на предельные или
- 9. Алканы Простейшим алканом является метан - СН4; Имея общую формулу - СnH2n+2, алканы образуют ряд соединений
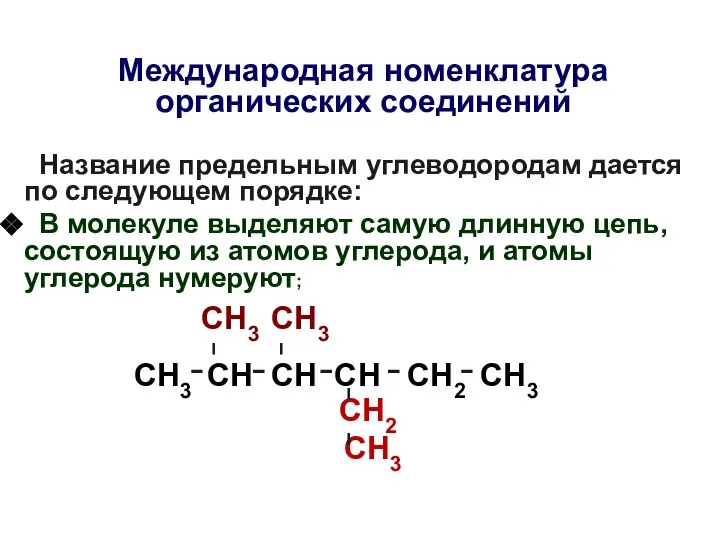
- 10. Международная номенклатура органических соединений Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную
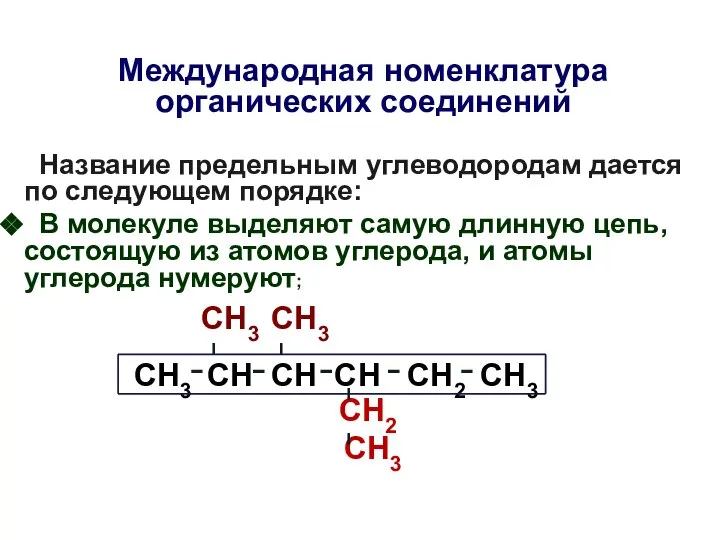
- 11. Международная номенклатура органических соединений Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную
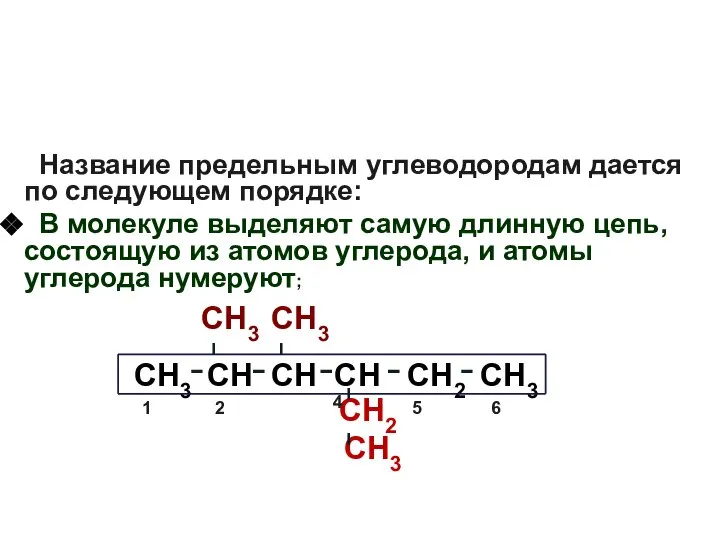
- 12. Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную цепь, состоящую из атомов
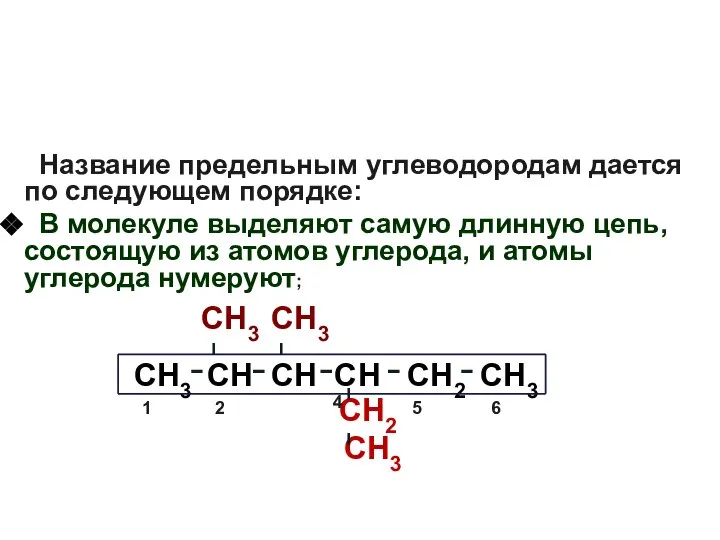
- 13. Название предельным углеводородам дается по следующем порядке: В молекуле выделяют самую длинную цепь, состоящую из атомов
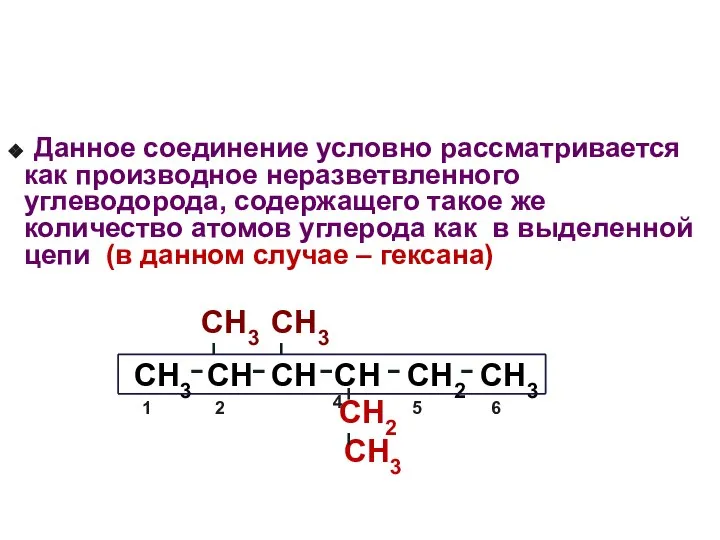
- 14. Данное соединение условно рассматривается как производное неразветвленного углеводорода, содержащего такое же количество атомов углерода как в
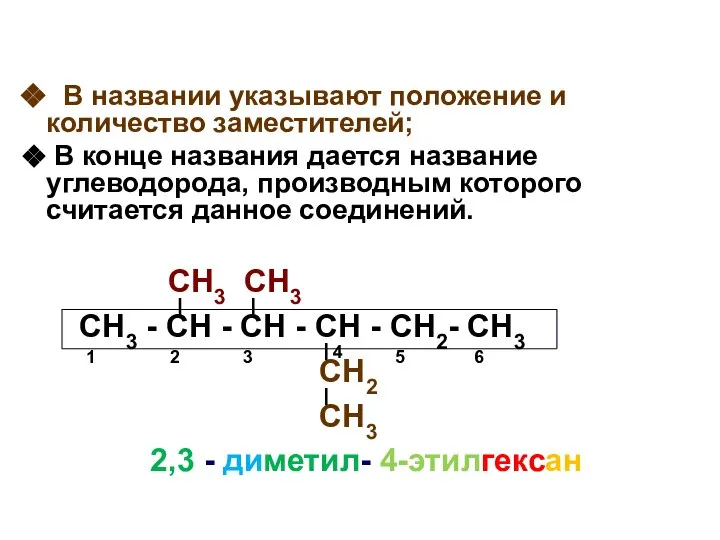
- 15. СН3 СН3 СН3 - СН - СН - СН - СН2- СН3 СН2 СН3 2,3 -
- 16. Физико-химические свойства алканов Все алканы не растворимы в воде; Алканы, содержащие не более 5 углеродных атомов,
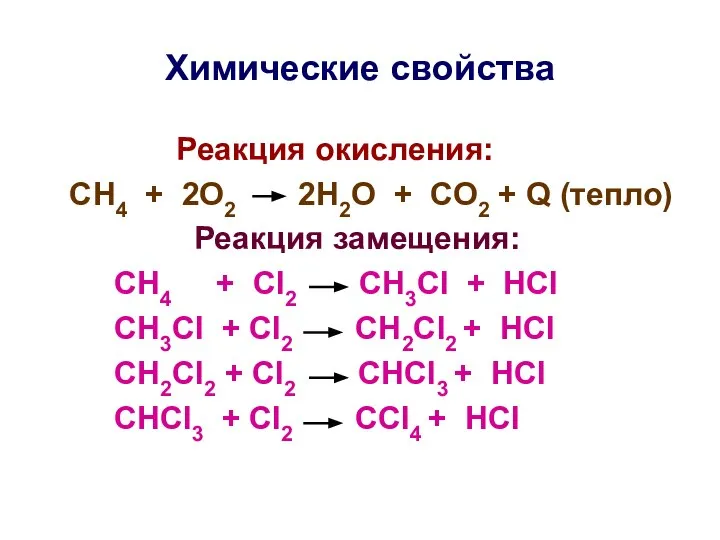
- 17. Химические свойства Реакция окисления: СН4 + 2О2 2Н2О + СО2 + Q (тепло) Реакция замещения: СН4
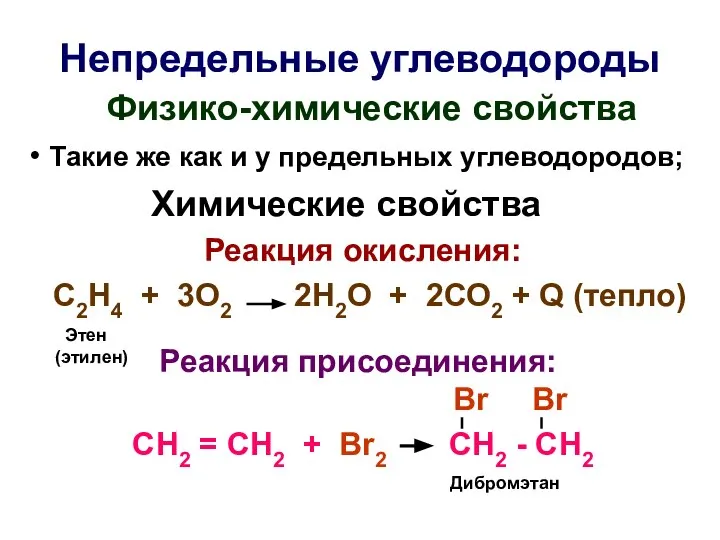
- 18. Непредельные углеводороды Физико-химические свойства Такие же как и у предельных углеводородов; Химические свойства Реакция окисления: С2Н4
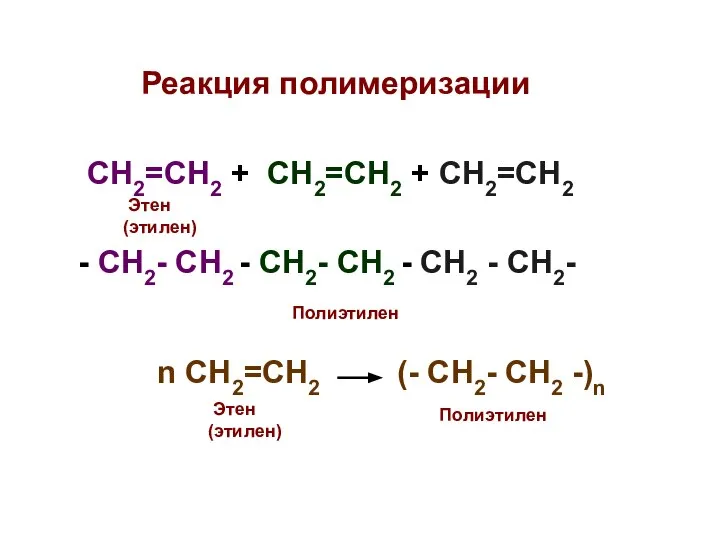
- 19. Реакция полимеризации СН2=СН2 + СН2=СН2 + СН2=СН2 - СН2- СН2 - СН2- СН2 - СН2 -
- 20. Номенклатура непредельных углеводов За основу названия берется название соответствующего предельного углеводорода, и в этом названии вместо
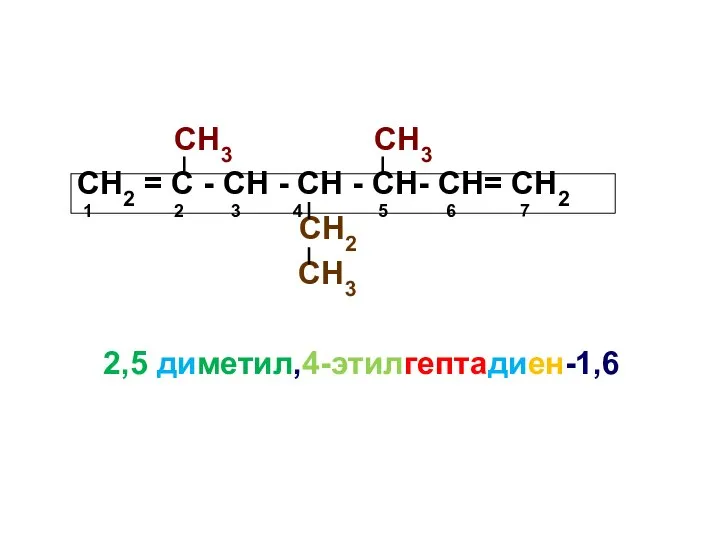
- 21. СН3 СН3 СН2 = С - СН - СН - СН- СН= СН2 СН2 СН3 2,5
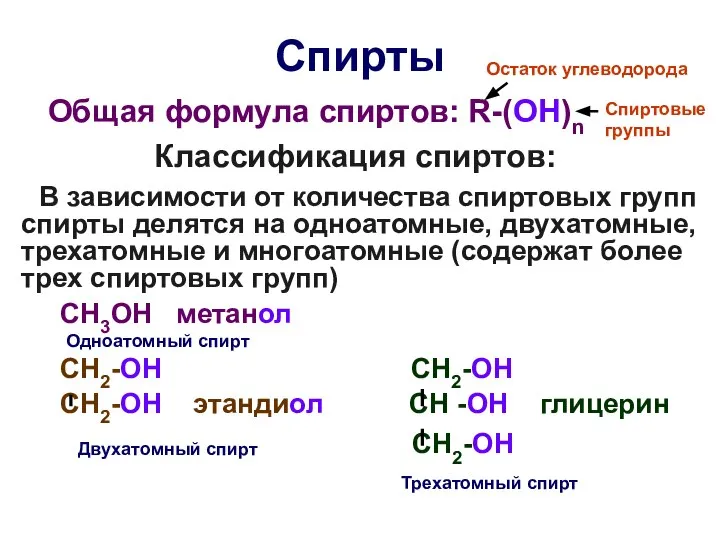
- 22. Спирты Общая формула спиртов: R-(OH)n Классификация спиртов: В зависимости от количества спиртовых групп спирты делятся на
- 23. Физико-химические свойства спиртов Низкомолекулярные спирты, содержащие не более 11-12 атомов углерода, являются жидкостями; Высокомолекулярные спирты, содержащие
- 24. Химические свойства спиртов Реакция окисления С2Н5ОН + 3О2 2СО2 + 3Н2О + Q С2Н5ОН CH3C Образование
- 25. Номенклатура спиртов За основу названия берется название углеводорода, входящего в молекулу спирта, и добавляется окончание «ол»
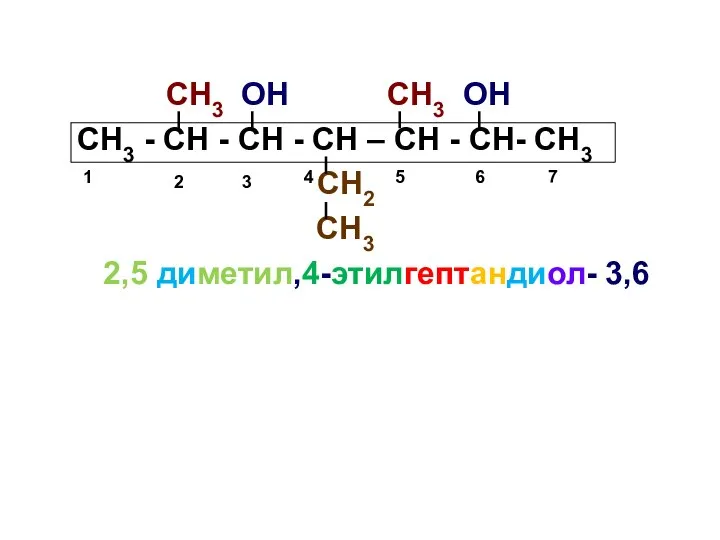
- 26. СН3 ОН СН3 ОН СН3 - СН - СН - СН – СН - СН- СН3
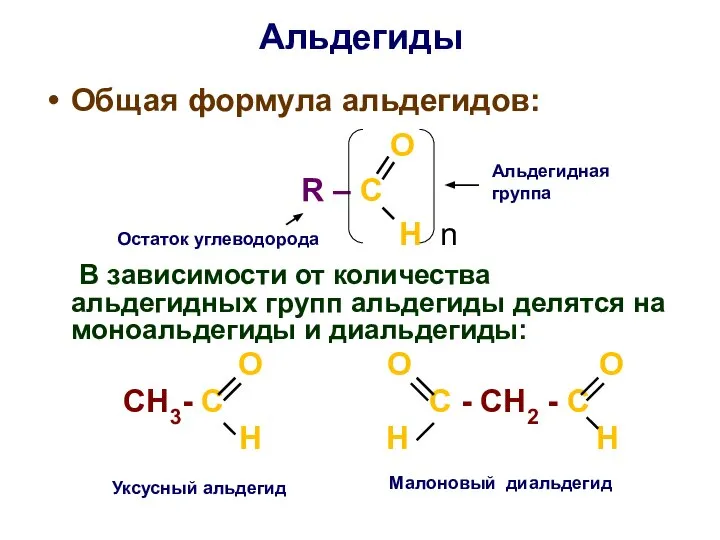
- 27. Альдегиды Общая формула альдегидов: O R – C H n В зависимости от количества альдегидных групп
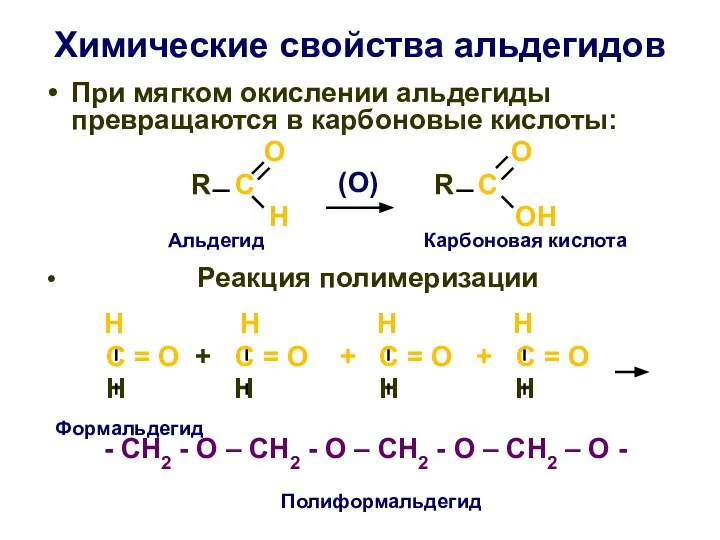
- 28. Химические свойства альдегидов При мягком окислении альдегиды превращаются в карбоновые кислоты: О О R C R
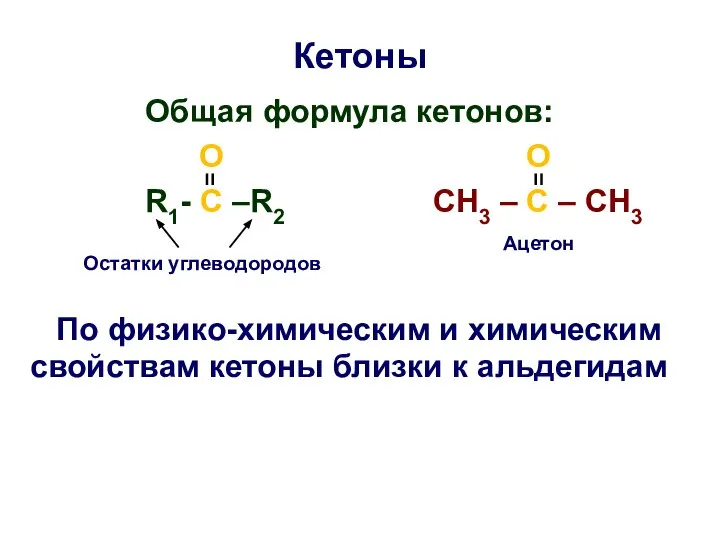
- 29. Кетоны Oбщая формула кетонов: O O R1- C –R2 CH3 – C – CH3 По физико-химическим
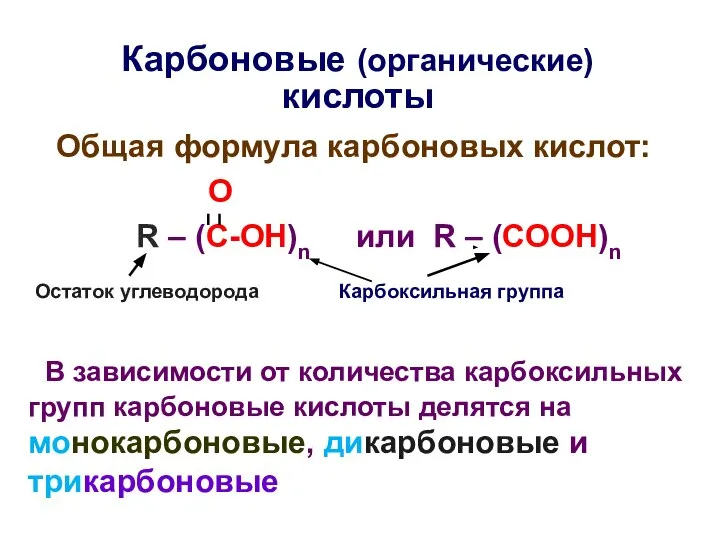
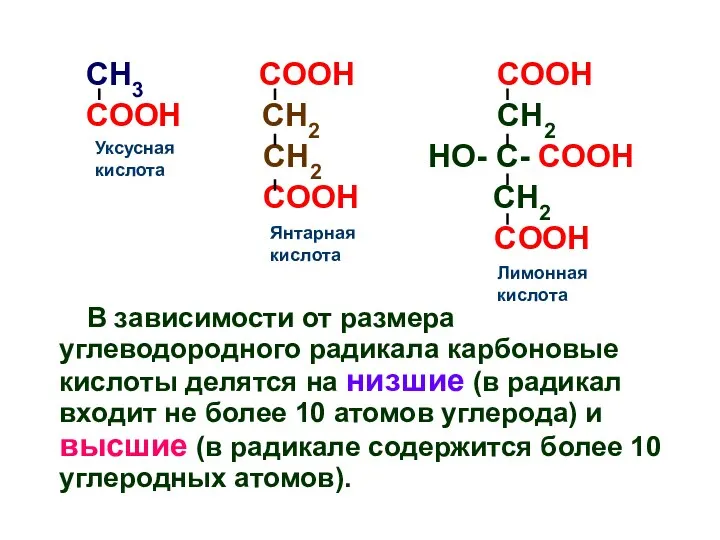
- 30. Карбоновые (органические) кислоты Общая формула карбоновых кислот: О R – (C-OH)n или R – (COOH)n В
- 31. CH3 COOH COOH COOH CH2 CH2 CH2 HO- C- COOH COOH CH2 COOH В зависимости от
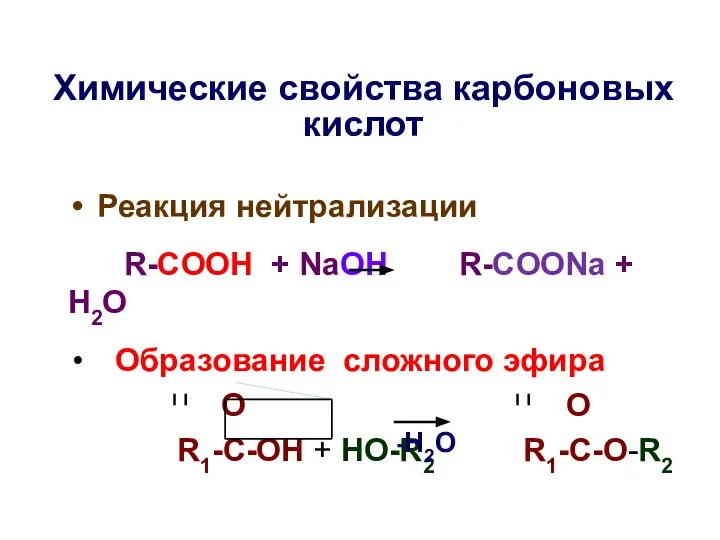
- 32. Химические свойства карбоновых киcлот Реакция нейтрализации R-COOH + NaOH R-COONa + H2O Образование сложного эфира O
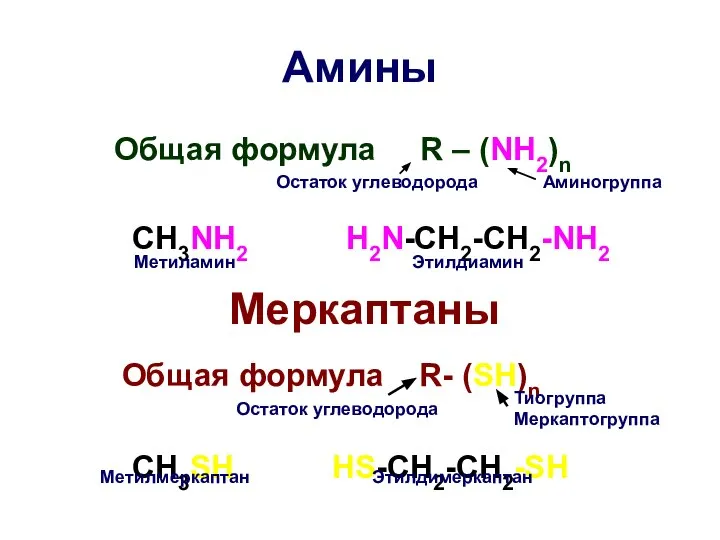
- 33. Амины Общая формула R – (NH2)n CH3NH2 H2N-CH2-CH2-NH2 Меркаптаны Общая формула R- (SH)n CH3SH HS-CH2-CH2-SH Остаток
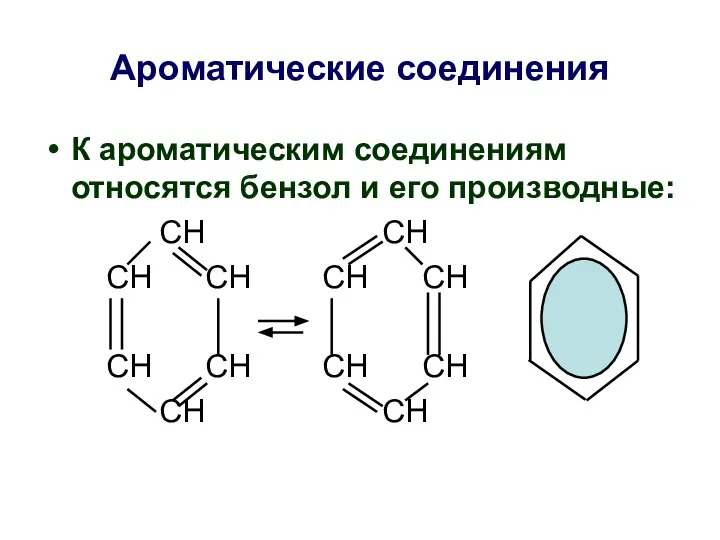
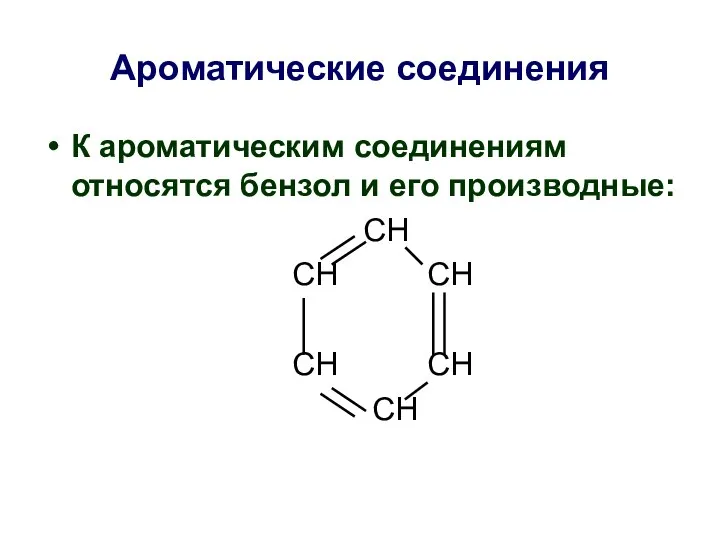
- 34. Ароматические соединения К ароматическим соединениям относятся бензол и его производные: СН СН СН СН СН СН
- 35. Ароматические соединения К ароматическим соединениям относятся бензол и его производные: СН СН СН СН СН СН
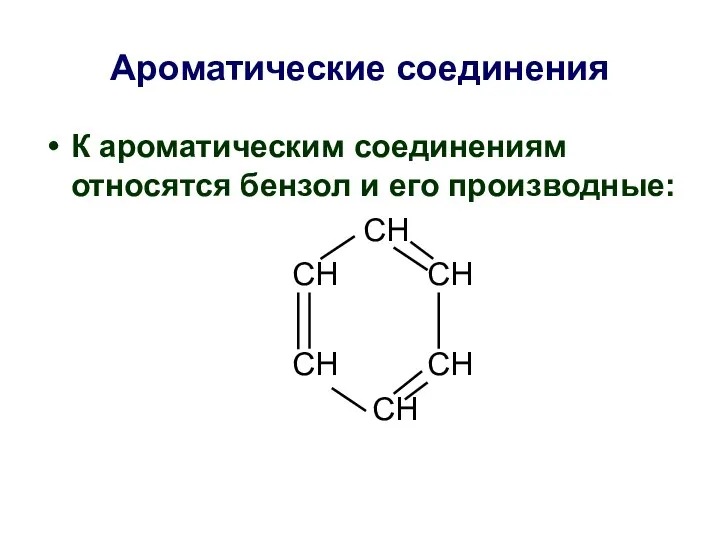
- 36. Ароматические соединения К ароматическим соединениям относятся бензол и его производные: СН СН СН СН СН СН
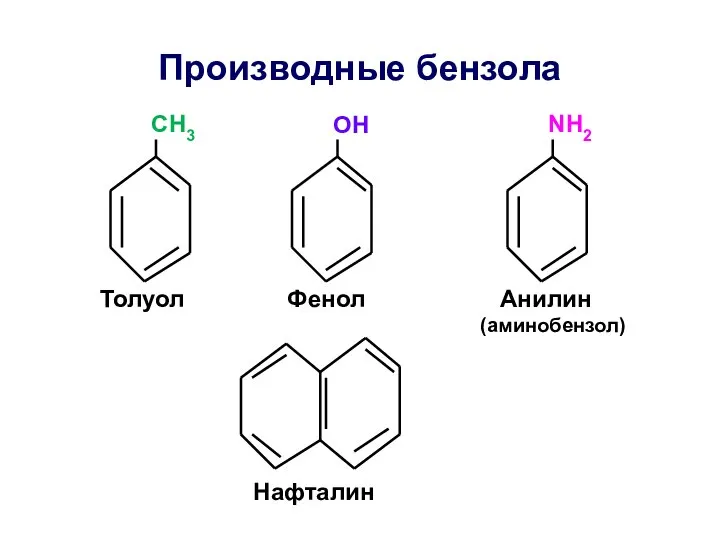
- 37. Производные бензола СН3 ОН NH2 Толуол Фенол Анилин (аминобензол) Нафталин
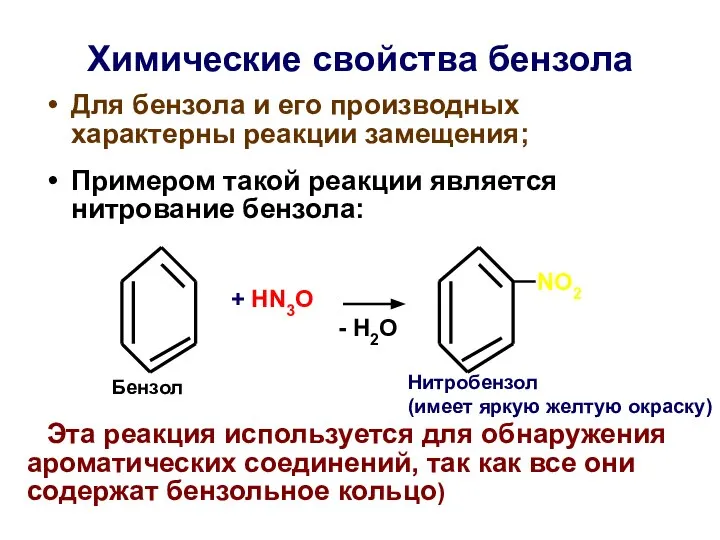
- 38. Химические свoйства бензола Для бензола и его производных характерны реакции замещения; Примером такой реакции является нитрование
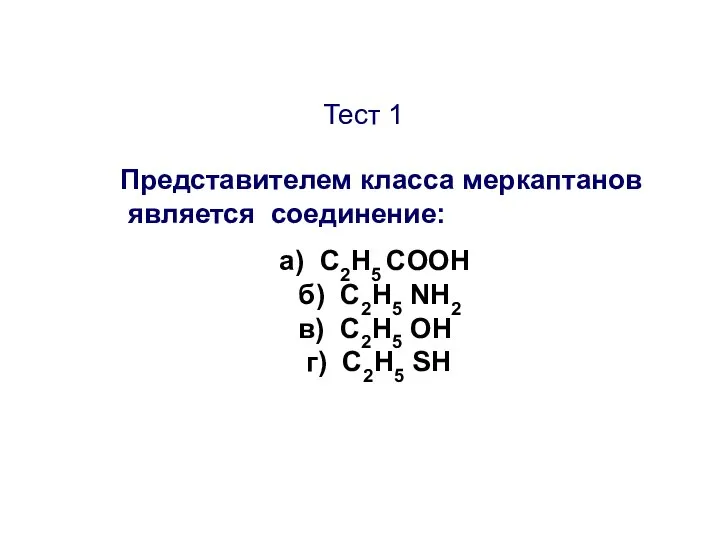
- 39. Тест 1 Представителем класса меркаптанов является соединение: а) C2H5 COOH б) C2H5 NH2 в) C2H5 ОН
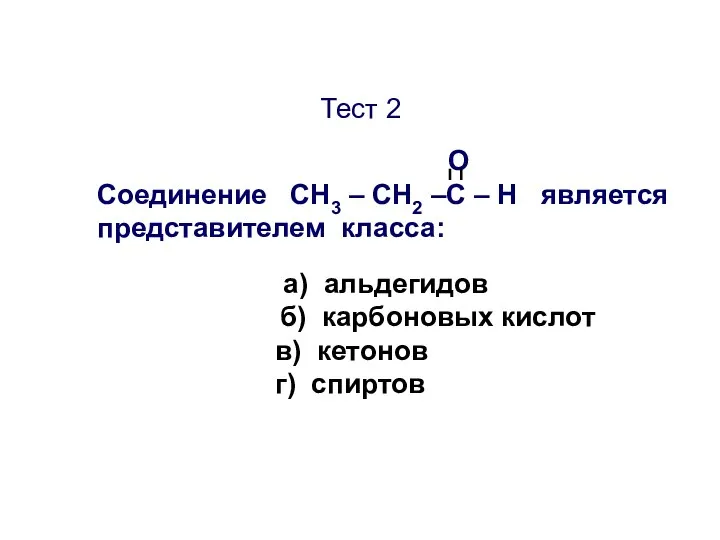
- 40. Тест 2 О Соединение CН3 – СН2 –С – Н является представителем класса: а) альдегидов б)
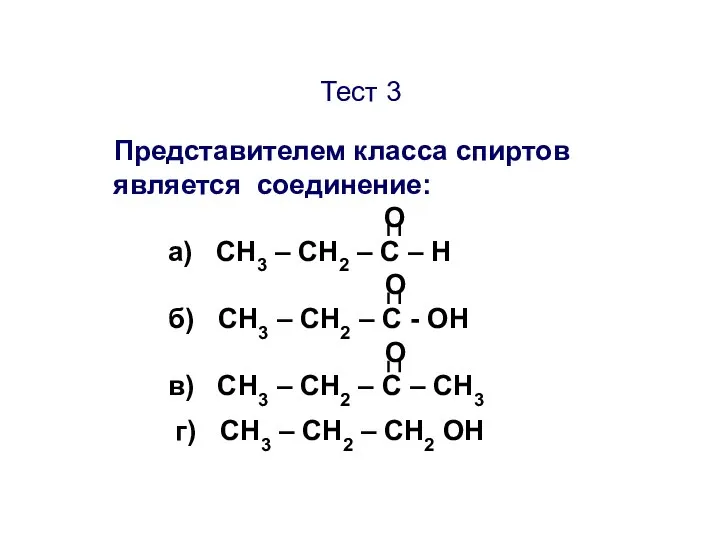
- 41. Тест 3 Представителем класса спиртов является соединение: О а) CН3 – СН2 – С – Н
- 42. Бензольное кольцо содержит: а) бутанол б) толуол в) циклопептан г) циклогексан Тест 4
- 43. Тест 5 В реакцию присоединения легко вступают: а) ароматические углеводороды б) непредельные углеводороды в) предельные углеводороды
- 44. Тест 5 Синтетическим полимером является: а) белок б) полипропилен в) крахмал г) целлюлоза
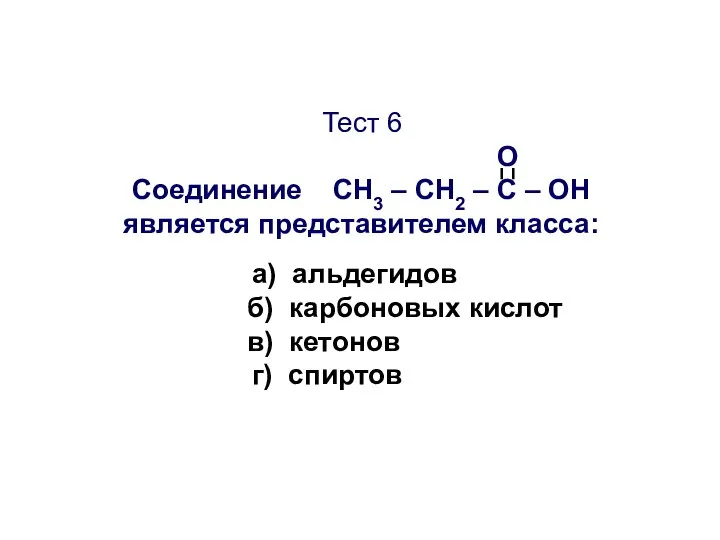
- 45. Тест 6 О Соединение CН3 – СН2 – С – ОН является представителем класса: а) альдегидов
- 46. Тест 7 Атомы углерода в органических соединениях образуют: а) одну ковалентную связь б) две ковалентные связи
- 47. Тест 8 Карбоновые кислоты легко вступают в реакцию: а) с альдегидами б) с бензолом б) с
- 48. Тест 9 Представителем класса карбоновых кислот является соединение: а) C2H6 б) C2H5NH2 в) C2H5ОН г) C2H5СООН
- 49. Тест 10 Для обнаружения ароматических соединений применяется реакция: а) гидролиза б) изомеризации в) нитрования г) фосфоролиза
- 50. Тест 11 Соединение НО- CН2 – СН2 – СН2 – ОН является представителем класса: а) одноатомных
- 51. Тест 12 Атомы углерода в органических соединениях соединяются: а) водородными связями б) ионными связями в) ковалентными
- 53. Скачать презентацию

















 Презентация по Химии "синтетичні миючі засоби" - скачать смотреть бесплатно
Презентация по Химии "синтетичні миючі засоби" - скачать смотреть бесплатно Строение атома (8 класс)
Строение атома (8 класс) Топливо и его характеристики
Топливо и его характеристики Химический элемент сера
Химический элемент сера Важнейшие минералы
Важнейшие минералы Прикладная химия. Теплоперенос в химических реакторах и теплообменники
Прикладная химия. Теплоперенос в химических реакторах и теплообменники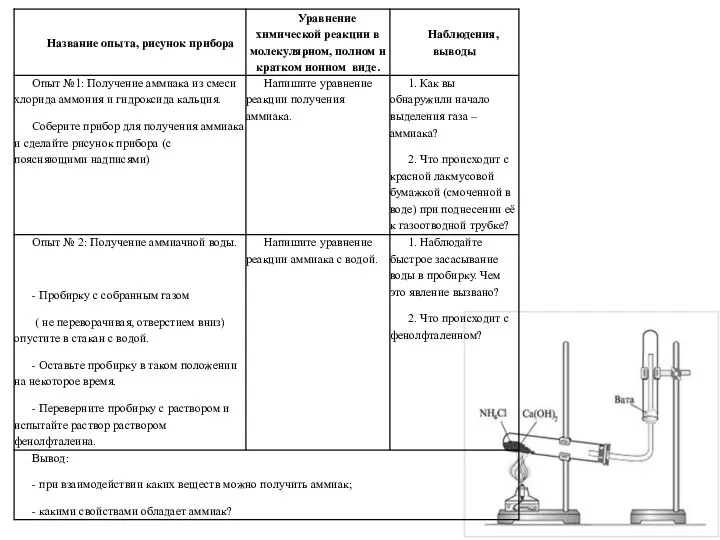 Получение аммиака и изучение его свойств
Получение аммиака и изучение его свойств Обобщение и систематизация знаний по теме: Общая характеристика химических элементов и химических реакций
Обобщение и систематизация знаний по теме: Общая характеристика химических элементов и химических реакций Виды присадок к моторному топливу. Керосин
Виды присадок к моторному топливу. Керосин Хром. Использование хрома
Хром. Использование хрома Азот
Азот Свойства солёной воды. Море у меня в стакане
Свойства солёной воды. Море у меня в стакане Изомеризация легких парафиновых углеводородов. Термогидрокаталитические процессы. Гидроочистка нефтяного сырья
Изомеризация легких парафиновых углеводородов. Термогидрокаталитические процессы. Гидроочистка нефтяного сырья Ячеечная модель реакторов
Ячеечная модель реакторов Предмет химии. Вещества и их физические свойства
Предмет химии. Вещества и их физические свойства Кислые породы повышенной щелочности и щелочные
Кислые породы повышенной щелочности и щелочные Сера. Аллотропные модификации
Сера. Аллотропные модификации Oxygen
Oxygen Что Вы ожидаете от занятия? Отметьте своё настроение.
Что Вы ожидаете от занятия? Отметьте своё настроение.  Получение и реакции пиразина
Получение и реакции пиразина Контроль в процессе обучения химии на старшей ступени школы
Контроль в процессе обучения химии на старшей ступени школы Химические явления. Уравнения химических реакций
Химические явления. Уравнения химических реакций Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Химико-технологические процессы современных производств. Лекция №3
Химико-технологические процессы современных производств. Лекция №3 Методы контроля и анализа веществ
Методы контроля и анализа веществ Химия элементов VA группы
Химия элементов VA группы Гормоны
Гормоны Тест по неметаллам
Тест по неметаллам