Содержание
- 5. ИНЕРТНЫЕ ГАЗЫ
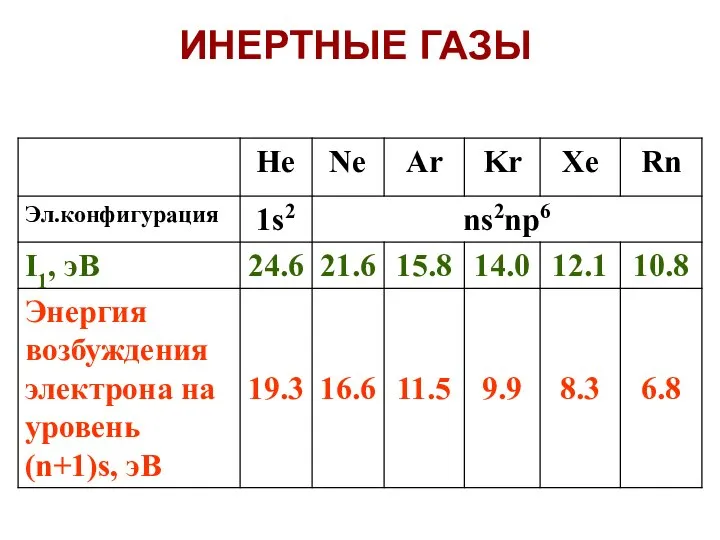
- 6. Значения I1 слишком велики, чтобы затраты энергии на образование катиона Э+ были компенсированы энергией, выделяющейся при
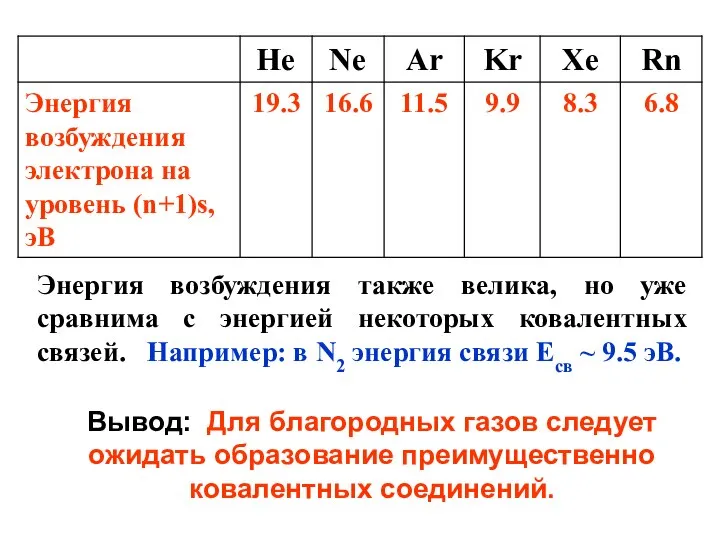
- 7. Энергия возбуждения также велика, но уже сравнима с энергией некоторых ковалентных связей. Например: в N2 энергия
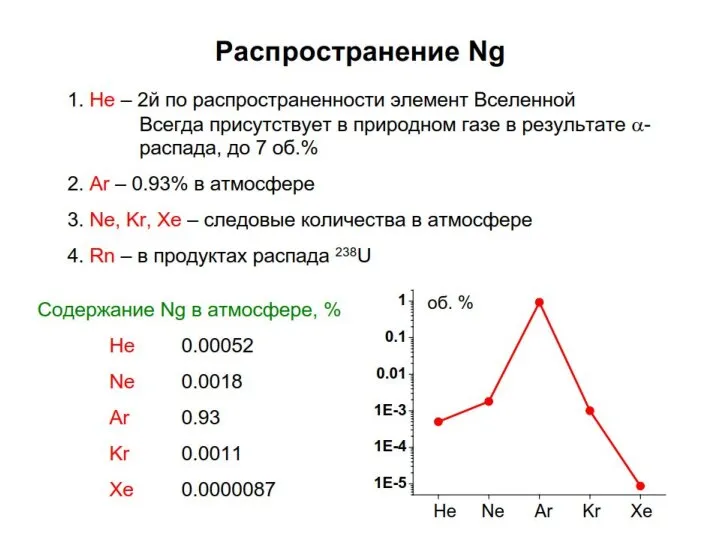
- 8. В природе инертные газы образуются в результате различных ядерных реакций. Часть инертных газов имеет космогенное происхождение.
- 9. Способность инертных газов к образованию химических соединений открыта сравнительно недавно. В настоящее время лучше изучена химия
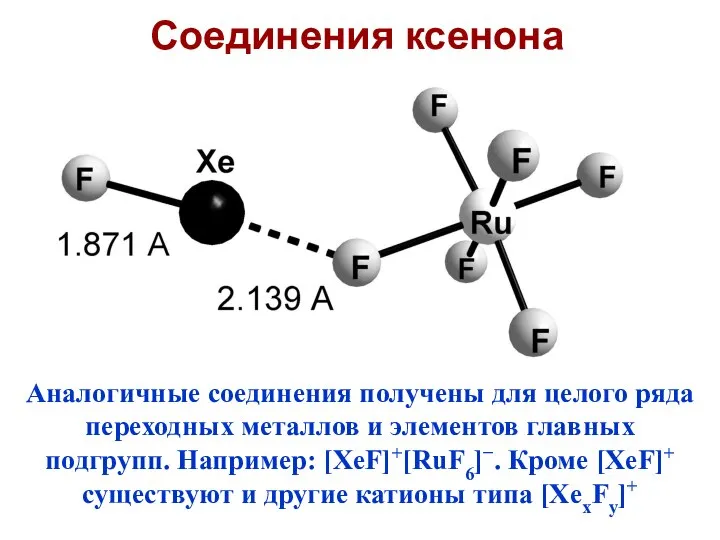
- 10. Соединения ксенона Ксенон – первый разрушил миф о химической инертности благородных газов. Первые соединения получены Нилом
- 11. Изучая реакцию O2 + PtF6 Бартлетт установил, что в ней образуется соль катиона диоксигенила O2+: O2
- 12. Далее он обратил внимание на то, что потенциал ионизации дикислорода и ксенона очень близки по значению:
- 13. Позднее были уточнены строение и состав этой соли. На самом деле (в соответствии с нашим начальным
- 14. Аналогичные соединения получены для целого ряда переходных металлов и элементов главных подгрупп. Например: [XeF]+[RuF6]−. Кроме [XeF]+
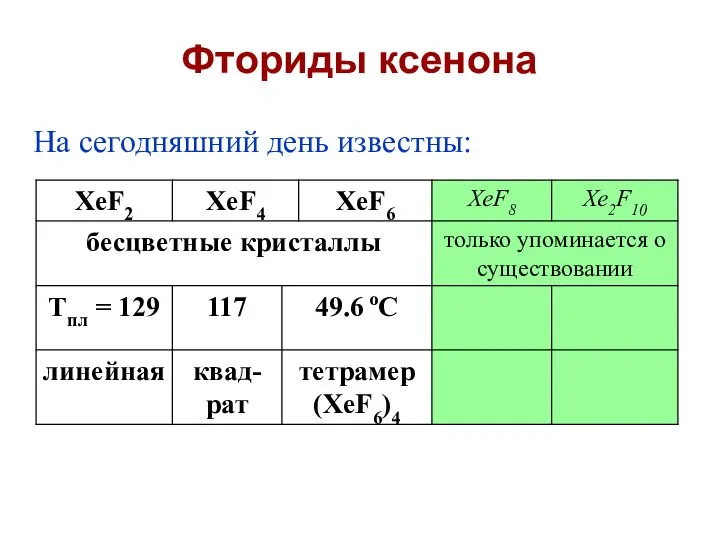
- 15. Фториды ксенона На сегодняшний день известны:
- 16. Xe + F2 = XeF2 (смесь Xe/F2 – 1:2, hν, 25 оС) Xe + 2F2 =
- 17. Химические свойства фторидов ксенона Окислительные свойства: сильные окислители XeF2(aq) + 2H+ + 2e = Xe +
- 18. Соединения других благородных газов
- 19. Соединения криптона Соединения криптона менее устойчивы, чем ксенона. Например: XeF2 – термод. стабилен ( ). KrF2
- 20. KrF2 медленно разлагается при комнатной температуре. Это требует особого, нетрадиционного, подхода к синтезу! Для получение KrF2
- 21. Применение инертных газов
- 22. 1) создание инертной атмосферы при проведении химических реакций и технических процессов, требующих отсутствия кислорода (литье из
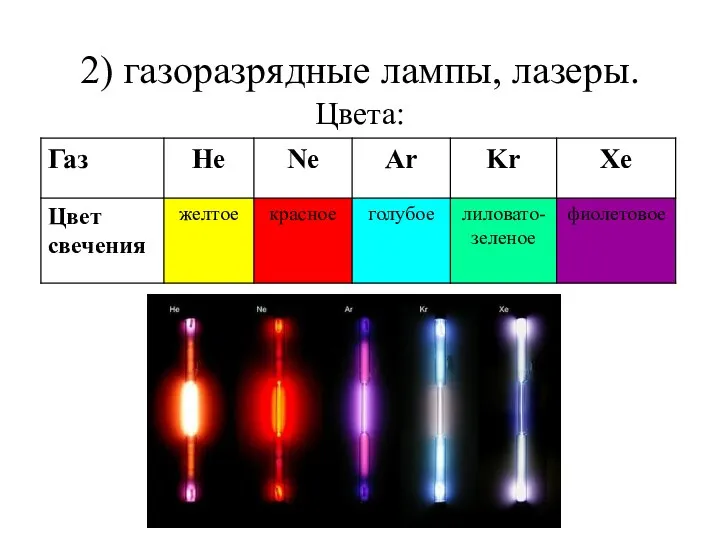
- 23. 2) газоразрядные лампы, лазеры. Цвета:
- 24. 3) гелий-кислородные дыхательные смеси для подводников (гелий в отличие от азота практически не растворяется в плазме
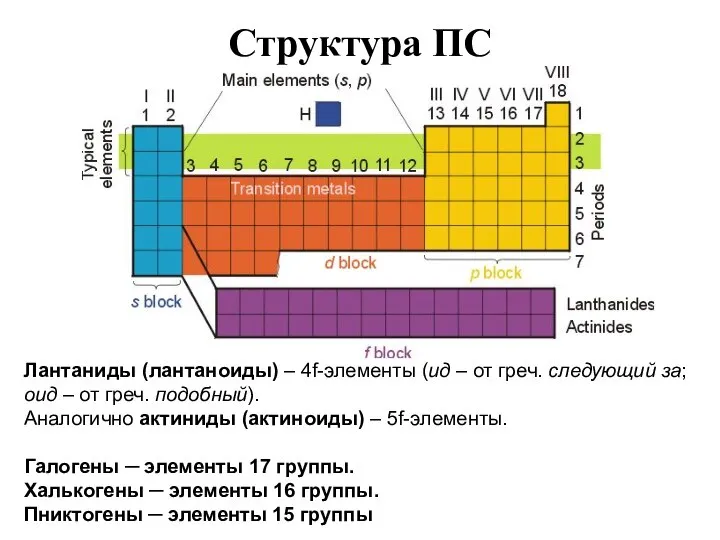
- 25. Структура ПС Лантаниды (лантаноиды) – 4f-элементы (ид – от греч. следующий за; оид – от греч.
- 26. Последовательность заполнения орбиталей Правило Клечковского: орбитальная энергия последовательно повышается по мере увеличения суммы главного квантового числа
- 27. Название Электроны в атоме Каждый электрон в атоме характеризуется четырьмя квантовыми числами Принцип Паули: в одном
- 28. Орбитальное число ℓ Электроны в атоме Главное квантовое число n: 1. Характеризует энергию взаимодействия электрона с
- 29. 1 определение переходных элементов Переходные элементы – элементы, расположенные в побочных подгруппах больших периодов периодической системы;
- 30. 2 определение переходных элементов 2) Переходные элементы – элементы, в атомах или ионах которых d- или
- 31. В то время как непереходные элементы в каждом периоде изменяются от металлов к неметаллам, все переходные
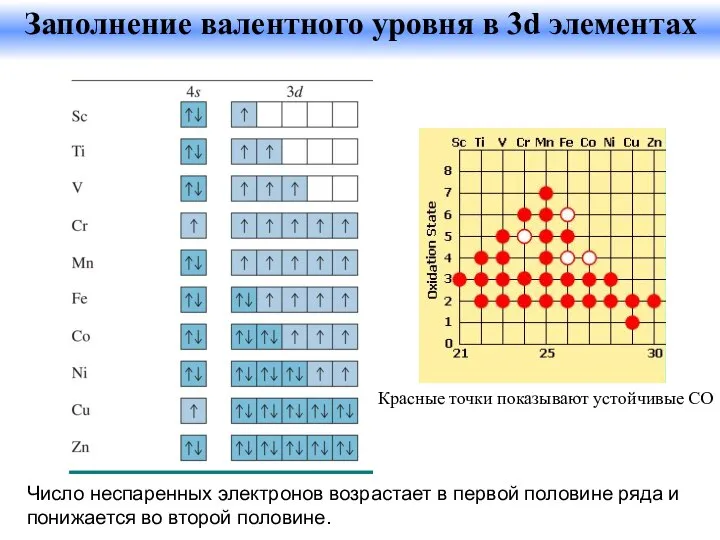
- 32. Число неспаренных электронов возрастает в первой половине ряда и понижается во второй половине. Заполнение валентного уровня
- 33. Разнообразие степеней окисления Количество возможных СО возрастает от Sc к Mn. Для Mn реализуются все возможные
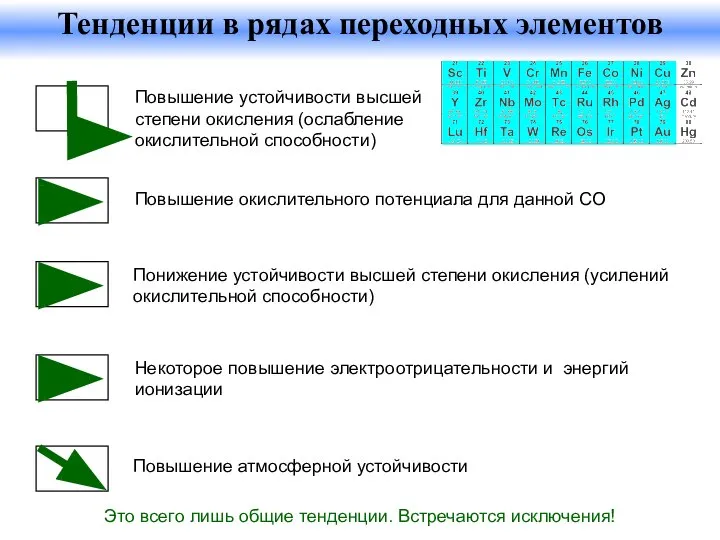
- 34. Повышение устойчивости высшей степени окисления (ослабление окислительной способности) Повышение окислительного потенциала для данной СО Понижение устойчивости
- 35. Координационные соединения переходных металлов
- 36. Соединения, состоящие из других, более простых соединений называются комплексными. Центральный атом – окружен молекулами или ионами
- 37. [Co(NH3)6]3+ – комплекс (катионный комплекс); [Co(NH3)6]Cl3 – комплексное соединение (соль). [Fe(CO)5] – комплекс и комплексное соединение.
- 38. Строение комплексного соединения K3 [Fe(CN)6] Ион-комплексообразователь (центральный атом) Лиганды от лат. ligare – связывать, соединять Координационное
- 39. Строение комплексного соединения Комплексное соединение состоит из: 1) внутренней сферы [комплекс] 2) внешней сферы (противоион) [Ni(NH3)6]Cl2
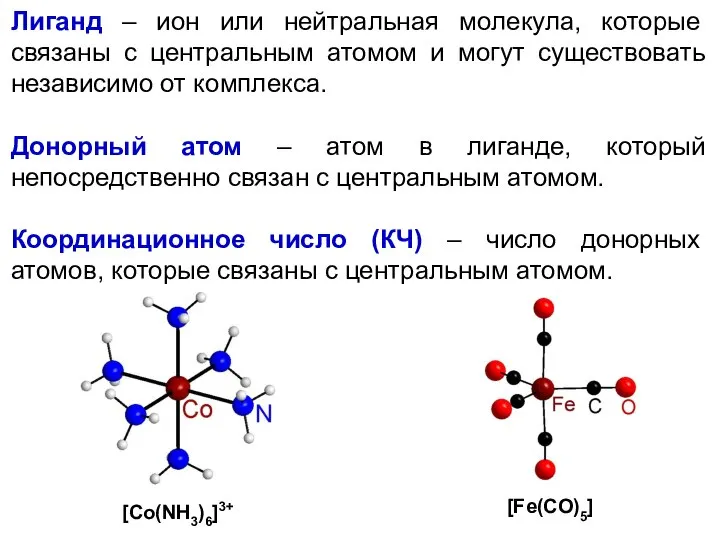
- 40. Лиганд – ион или нейтральная молекула, которые связаны с центральным атомом и могут существовать независимо от
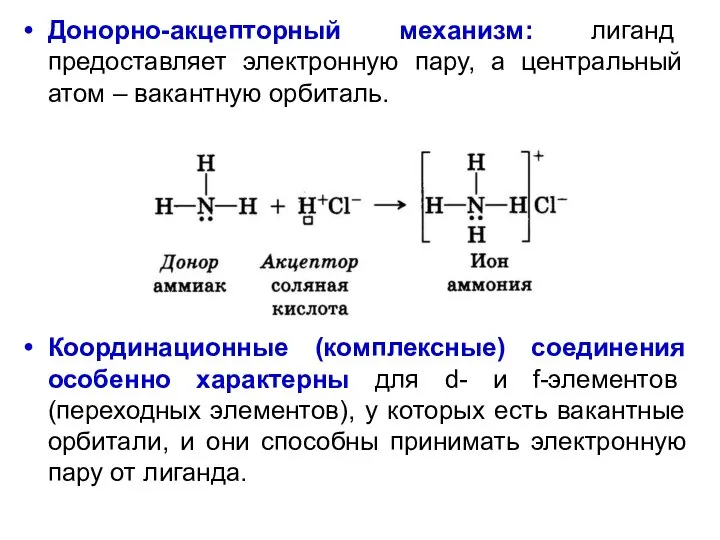
- 41. Донорно-акцепторный механизм: лиганд предоставляет электронную пару, а центральный атом – вакантную орбиталь. Координационные (комплексные) соединения особенно
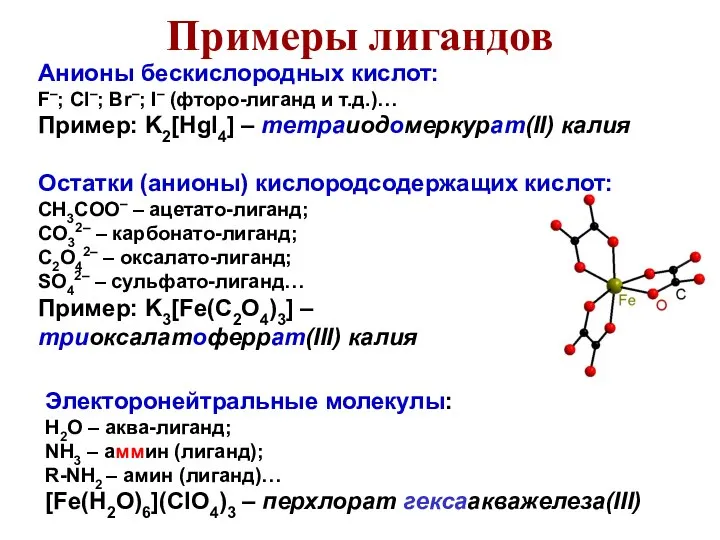
- 42. Анионы бескислородных кислот: F–; Cl–; Br–; I– (фторо-лиганд и т.д.)… Пример: K2[HgI4] – тетраиодомеркурат(II) калия Остатки
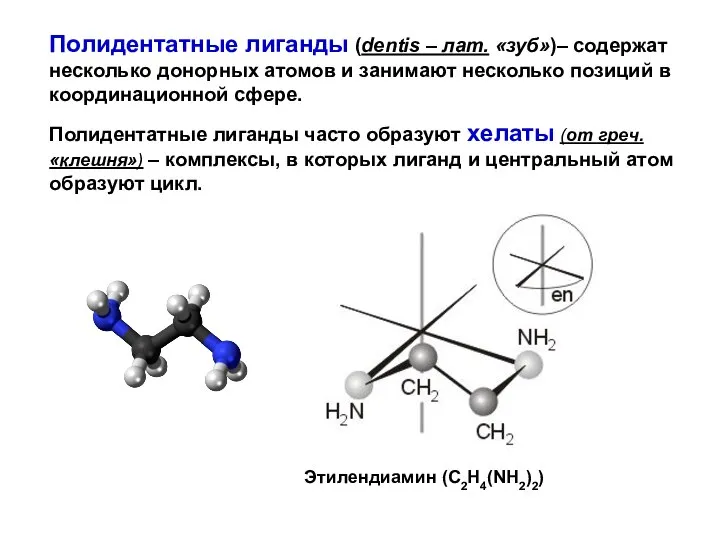
- 43. Полидентатные лиганды (dentis – лат. «зуб»)– содержат несколько донорных атомов и занимают несколько позиций в координационной
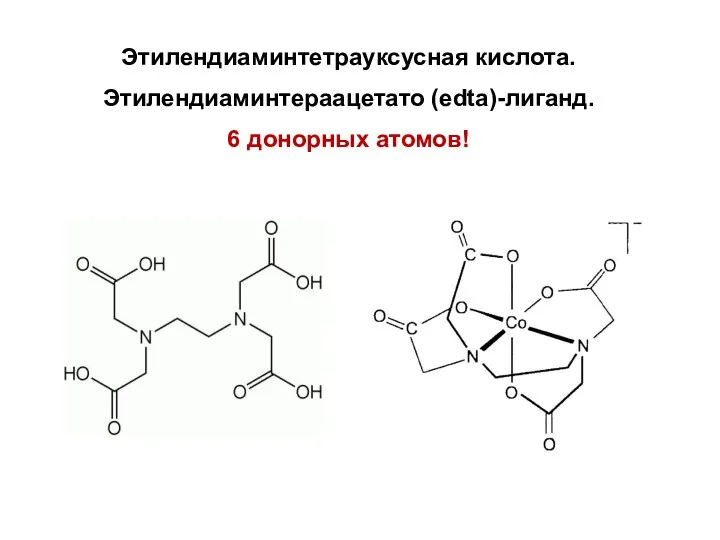
- 44. Этилендиаминтетрауксусная кислота. Этилендиаминтераацетато (edta)-лиганд. 6 донорных атомов!
- 45. ИЗОМЕРИЯ (от др.-греч. ἴσος – «равный», μέρος – «доля, часть») Явление, заключающееся в существовании химических соединений
- 46. Цис- и транс- изомеры, для квадратных частиц. [Pt(Gly)2] – диглицинатоплатина (II) Транс- менее растворим в воде,
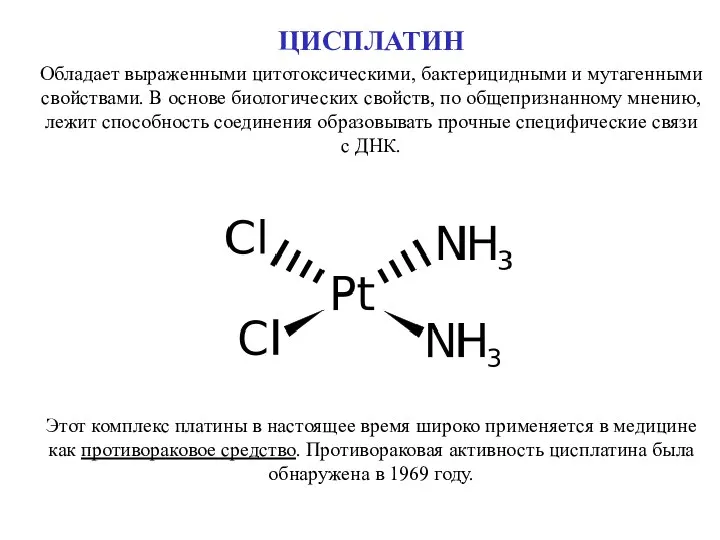
- 47. ЦИСПЛАТИН Обладает выраженными цитотоксическими, бактерицидными и мутагенными свойствами. В основе биологических свойств, по общепризнанному мнению, лежит
- 48. ос- (mer-) реберный гран- (fac-) граневой Для октаэдрических частиц [Pt(NH3)2Cl4] [Co(NH3)3Cl3] транс- (trans-) цис- (cis-) Геометрическая
- 49. Лиганды во внутренней и внешней координационной сфере меняются местами. [Co(NH3)5Cl]CN – пентаамминхлорокобальт (II) цианид [Co(NH3)5СN]Cl –
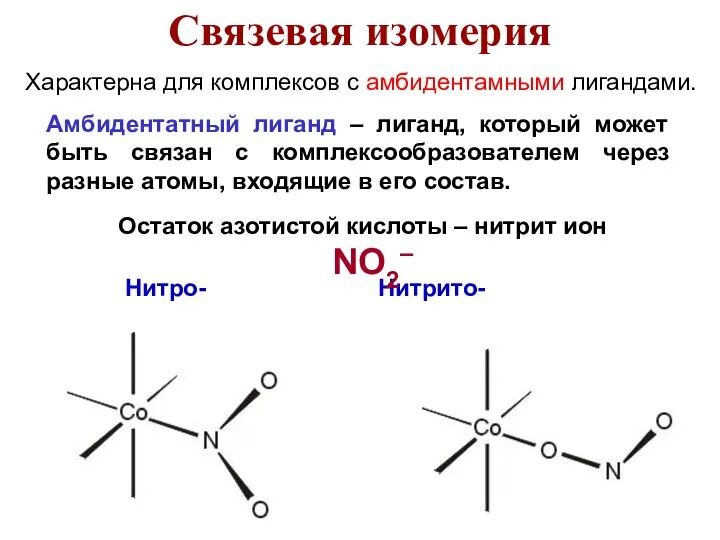
- 50. Характерна для комплексов с амбидентамными лигандами. Амбидентатный лиганд – лиганд, который может быть связан с комплексообразователем
- 51. для комплексных солей, в которых и катион и анион являются комплексными (CuPt(NH3)4Cl4) [Cu(NH3)4][PtCl4] – фиолетовый цвет
- 52. Cd2+ + CN– = [Cd(CN)]+ K1 = [Cd(CN)+]/[Cd2+][CN–]; [Cd(CN)]+ + CN– = [Cd(CN)2] K2 = [Cd(CN)2]/[
- 53. Константа образования характеризует устойчивость комплексов (в водных растворах). Константа образования характеризует прочность связывания лиганда с металлом
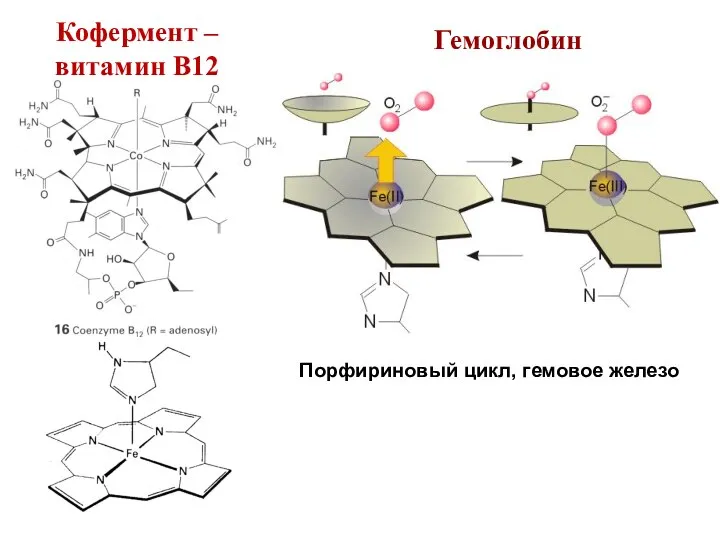
- 54. Гемоглобин Порфириновый цикл, гемовое железо Кофермент – витамин В12
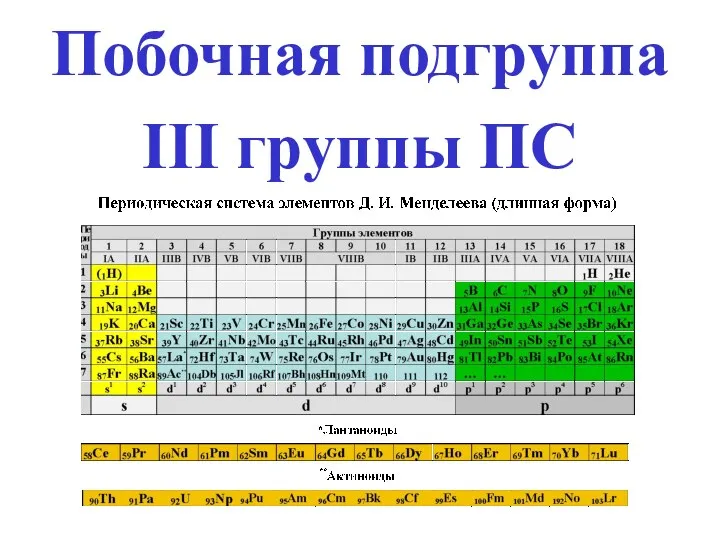
- 55. Побочная подгруппа III группы ПС
- 56. Редкоземельные элементы (РЗЭ) Редкоземельные элементы (РЗЭ) – d-элементы Sc, Y, La (скандний, иттрий, лантан) и 14
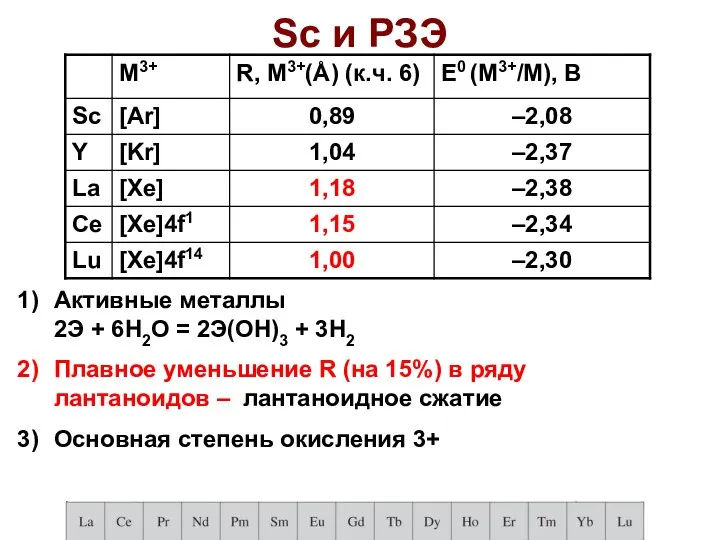
- 57. Sc и РЗЭ Активные металлы 2Э + 6H2О = 2Э(ОН)3 + 3H2 Плавное уменьшение R (на
- 58. Лантаноидное сжатие У лантаноидов (как и у актиноидов) увеличение атомного номера приводит не к повышению, а
- 59. Содержание в земной коре и минералы Sc – 36 место. Тортвейтит ((Sc,Y)2Si2O7) и стерреттит (Sc[PO4]·2H2O). Y
- 60. Открытие элементов Sc – элемент был предсказан Менделевым (как эка-бор) и открыт в 1879 году шведским
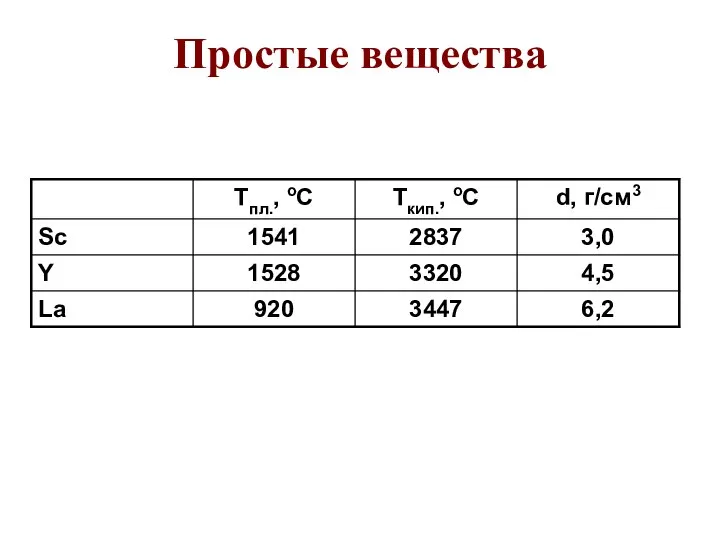
- 61. Простые вещества
- 62. Изменение свойств Sc(OH)3 ? La(OH)3 увеличение основных свойств. Примеры: 2Sc(OH)3 + 3H2SO4 = Sc2(SO4)3 + 3H2O;
- 63. Получение и свойства 1) 2MCl3 + 3Ca = 3CaCl2 + 2М – кальциетермия 2) М2O3 +
- 64. Химические свойства Ярко выражены основные свойства. Исключение – скандий (в горячей, конц. щелочи): 2Sc + 6NaOH
- 65. Основные соединения Оксиды M2O3 – тугоплавкие, плохо растворимы в воде, растворимы в кислотах Но: La2O3 +
- 66. Комплексы лантаноидов Аквакомплексы [M(H2O)9]3+ лабильны (замещение лигандов за 10–7 – 10–9 с) Предпочитают координацию по кислороду
- 67. Применение РЗЭ LaNi5 – хранение водорода в аккумуляторах; Y – в ядерных реакторах; LnBa2Cu3O7-x – сверпроводниках;
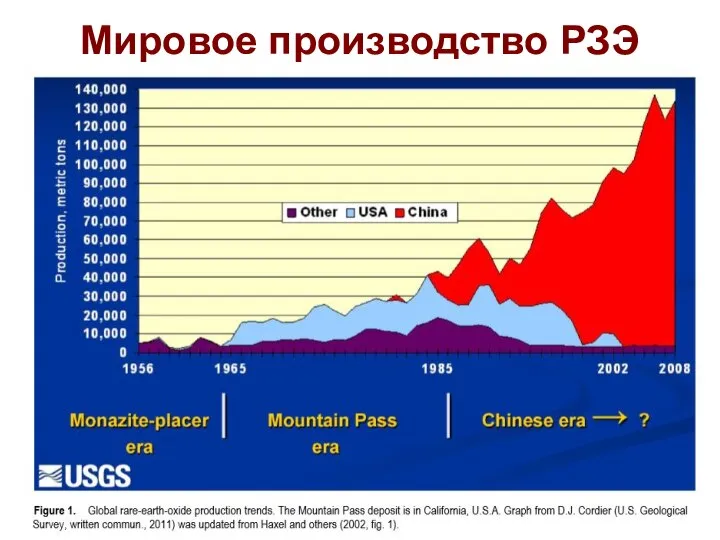
- 68. Мировое производство РЗЭ
- 69. Побочная подгруппа IV группы ПС
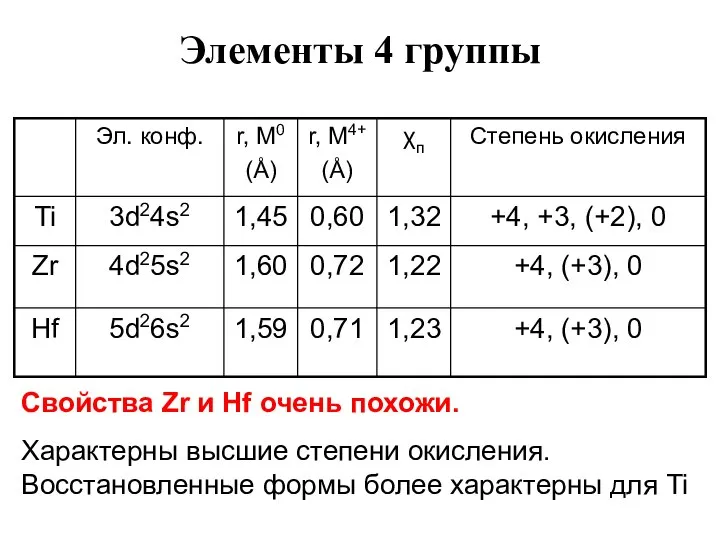
- 70. Элементы 4 группы Свойства Zr и Hf очень похожи. Характерны высшие степени окисления. Восстановленные формы более
- 71. Содержание в земной коре и минералы Ti – 9 место, рутил (TiO2), ильменит (FeTiO3), перовскит (CaTiO3)
- 72. Открытие элементов Ti – в 1791 г. англ. Грегор, в 1795 г. нем. Клапрот. Титаны –
- 73. Простые вещества Получение сложное, MO2 + 2C + 2Cl2 = MCl4 + 2CO MCl4 + 2Mg
- 74. Свойства простых веществ M+ H2 = MH2 (при выс. Т) - устойчивы M + C =
- 75. Свойства простых веществ M + O2 (или 2S) = MO2 (или MS2) (при нагревании порошков) Ti
- 76. (комплексообразование) M + 6HF = H2[MF6] + 3H2 M + 4CH3COOH + 6F– = [MF6]2– +
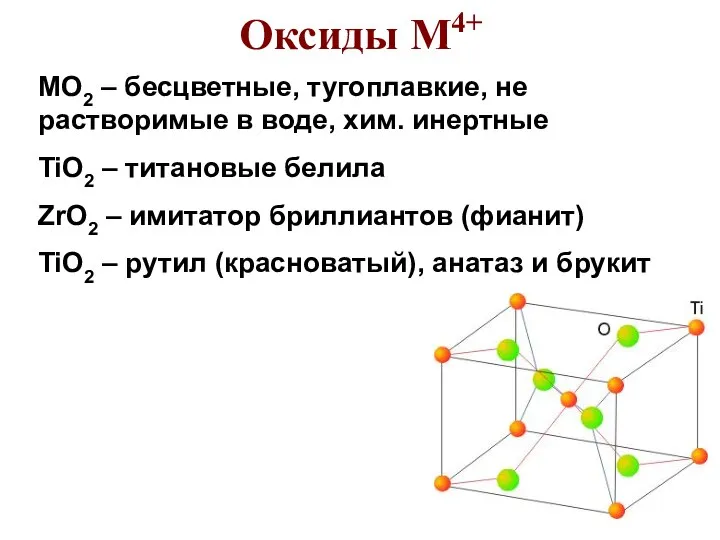
- 77. Оксиды М4+ MO2 – бесцветные, тугоплавкие, не растворимые в воде, хим. инертные TiO2 – титановые белила
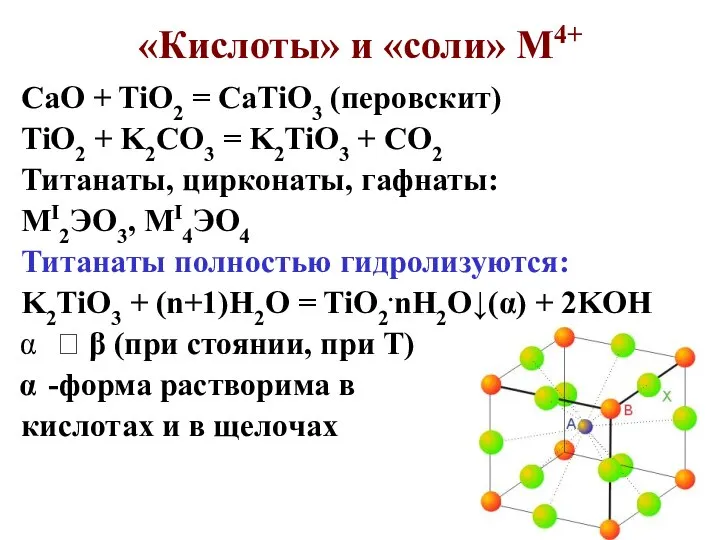
- 78. «Кислоты» и «соли» М4+ CaO + TiO2 = CaTiO3 (перовскит) TiO2 + K2CO3 = K2TiO3 +
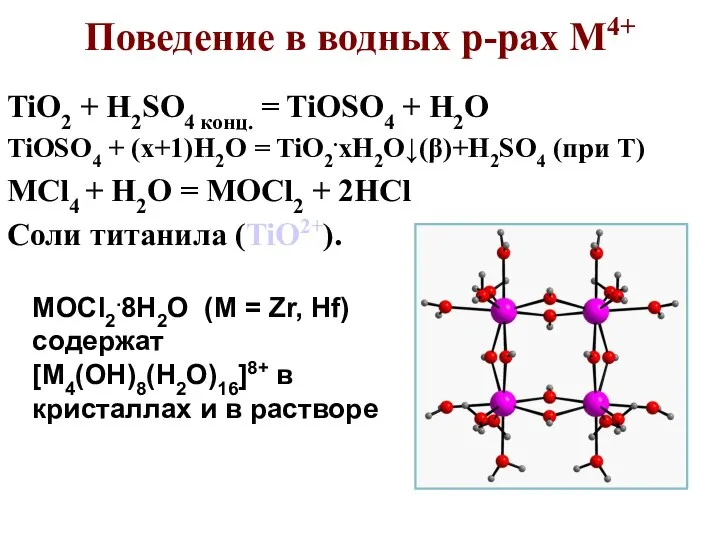
- 79. Поведение в водных р-рах M4+ TiO2 + H2SO4 конц. = TiOSO4 + H2O TiOSO4 + (x+1)H2O
- 80. Побочная подгруппа V группы ПС
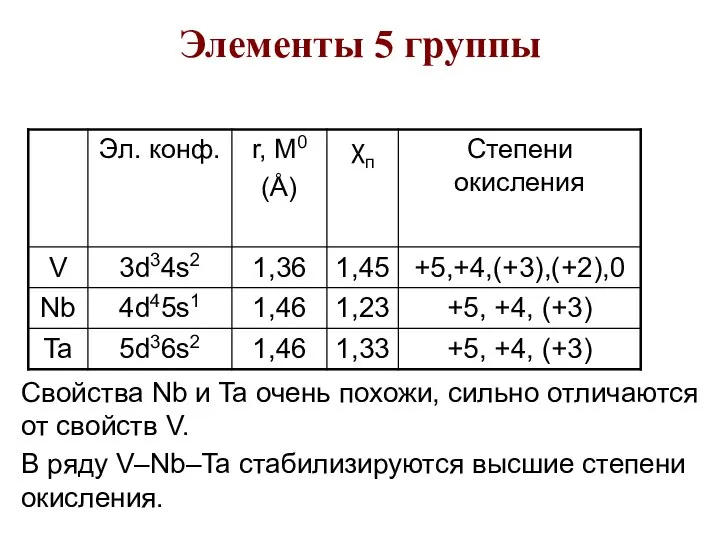
- 81. Элементы 5 группы Свойства Nb и Ta очень похожи, сильно отличаются от свойств V. В ряду
- 82. Содержание в земной коре и минералы V – 20 место, рассеян, VS2.V2S5 – патронит. Добывают из
- 83. Открытие элементов V – в 1801 г. мексиканец Дель Рио, затем в 1830 г. швед Сефстрём.
- 84. Простые вещества Получение сложное, проблема разделения Nb и Ta M2O5 + 5Ca = 5CaO + 2M
- 85. Известный "автомобильный король" Генри Форд сказал: "Если бы не было ванадия" - не было бы автомобиля".
- 86. Простые вещества Химически инертные 2V + 12HF = 2H[VF6] + 5H2 V + 6HNO3конц. = [VO2]NO3
- 87. ВАНАДИЙ 2+ VO основные VSO4 3+ V2O3 свойства V2(SO4)3 [VO]SO4 сульфат ванадила 4+ VO2 K4V4O9 ванадит
- 89. Скачать презентацию


























![[Co(NH3)6]3+ – комплекс (катионный комплекс); [Co(NH3)6]Cl3 – комплексное соединение (соль). [Fe(CO)5]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-36.jpg)
![Строение комплексного соединения K3 [Fe(CN)6] Ион-комплексообразователь (центральный атом) Лиганды от лат.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-37.jpg)
![Строение комплексного соединения Комплексное соединение состоит из: 1) внутренней сферы [комплекс]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-38.jpg)

![Цис- и транс- изомеры, для квадратных частиц. [Pt(Gly)2] – диглицинатоплатина (II)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-45.jpg)
![ос- (mer-) реберный гран- (fac-) граневой Для октаэдрических частиц [Pt(NH3)2Cl4] [Co(NH3)3Cl3]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-47.jpg)
![Лиганды во внутренней и внешней координационной сфере меняются местами. [Co(NH3)5Cl]CN –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-48.jpg)

![Cd2+ + CN– = [Cd(CN)]+ K1 = [Cd(CN)+]/[Cd2+][CN–]; [Cd(CN)]+ + CN–](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-51.jpg)









![Комплексы лантаноидов Аквакомплексы [M(H2O)9]3+ лабильны (замещение лигандов за 10–7 – 10–9](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-65.jpg)






![(комплексообразование) M + 6HF = H2[MF6] + 3H2 M + 4CH3COOH](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-75.jpg)




![Простые вещества Химически инертные 2V + 12HF = 2H[VF6] + 5H2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-85.jpg)
![ВАНАДИЙ 2+ VO основные VSO4 3+ V2O3 свойства V2(SO4)3 [VO]SO4 сульфат](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393642/slide-86.jpg)
 Металлы
Металлы Тефлон. Фенолформальдегідні смоли
Тефлон. Фенолформальдегідні смоли  Физические свойства металлов: пластичность, электропроводность, теплопроводность, металлический блеск, плотность
Физические свойства металлов: пластичность, электропроводность, теплопроводность, металлический блеск, плотность Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Расчёт равновесного состава
Расчёт равновесного состава Введение. Тренажер
Введение. Тренажер Морфологія та походження мінералів. Елементи кристалографії
Морфологія та походження мінералів. Елементи кристалографії Основания. Классификация оснований
Основания. Классификация оснований Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Азотсодержащие органические соединения
Азотсодержащие органические соединения Бинарный урок. Минеральные удобрения. (9 класс)
Бинарный урок. Минеральные удобрения. (9 класс) Сложные эфиры
Сложные эфиры Виды химической связи
Виды химической связи Электролиз Цель: изучить сущность процесса электролиза Задачи: раскрыть принцип работы электролизёра суть катодных и анодных
Электролиз Цель: изучить сущность процесса электролиза Задачи: раскрыть принцип работы электролизёра суть катодных и анодных  Тема: Серная кислота, свойства серной кислоты.
Тема: Серная кислота, свойства серной кислоты. Катаболизм жирных кислот. Метаболизм кетоновых тел. (Лекция 8)
Катаболизм жирных кислот. Метаболизм кетоновых тел. (Лекция 8) Теория строения
Теория строения Знакомство с образцами химических средств санитарии и гигиены
Знакомство с образцами химических средств санитарии и гигиены Мыс айналымы
Мыс айналымы Анионы. Группы анионов
Анионы. Группы анионов Презентация по Химии "Тема. Короткі відомості з історії хімії" - скачать смотреть бесплатно
Презентация по Химии "Тема. Короткі відомості з історії хімії" - скачать смотреть бесплатно Алканы. Предельные углеводороды. Насыщенные углеводороды. Парафины
Алканы. Предельные углеводороды. Насыщенные углеводороды. Парафины Презентация по Химии "Органічні розчинники" - скачать смотреть бесплатно
Презентация по Химии "Органічні розчинники" - скачать смотреть бесплатно Нечаев 18
Нечаев 18 Перегонка нефти в вакууме
Перегонка нефти в вакууме История чернил
История чернил Презентация по Химии "Витаминный алфавит" - скачать смотреть
Презентация по Химии "Витаминный алфавит" - скачать смотреть  Идентификация органических веществ
Идентификация органических веществ