Содержание
- 2. План 1. Загальна характеристика ферментів. 2. Властивості ферментів. 3. класифікація ферментів.
- 3. Спільність між хімічними каталізаторами і ферментами: 1. Каталізують тільки термодинамічно можливі реакції. 2. Не змінюються в
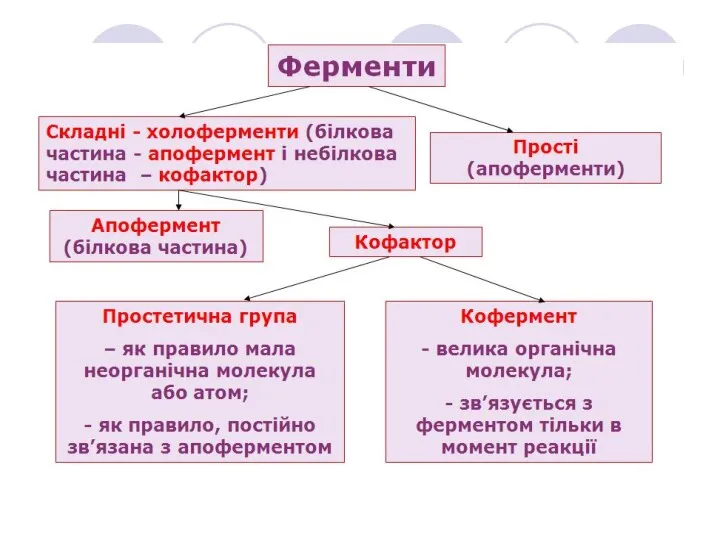
- 5. Металоферменти містять міцно зв’язані іони металів в активному центрі фермента (наприклад, залізо, цинк, мідь, кобальт). Приклади
- 6. Активні центри ферментів Активний центр – специфічна ділянка фермента до якої приєднується субстрат Субстрат, як правило,
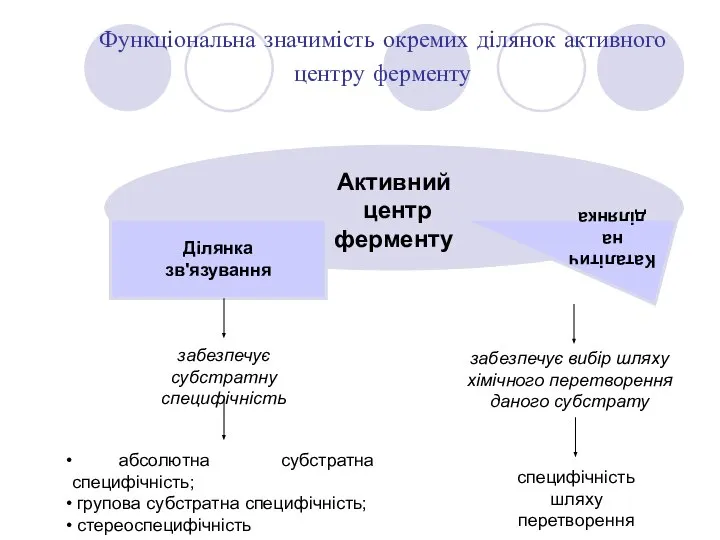
- 7. Функціональна значимість окремих ділянок активного центру ферменту Активний центр ферменту Ділянка зв'язування Каталітична ділянка забезпечує субстратну
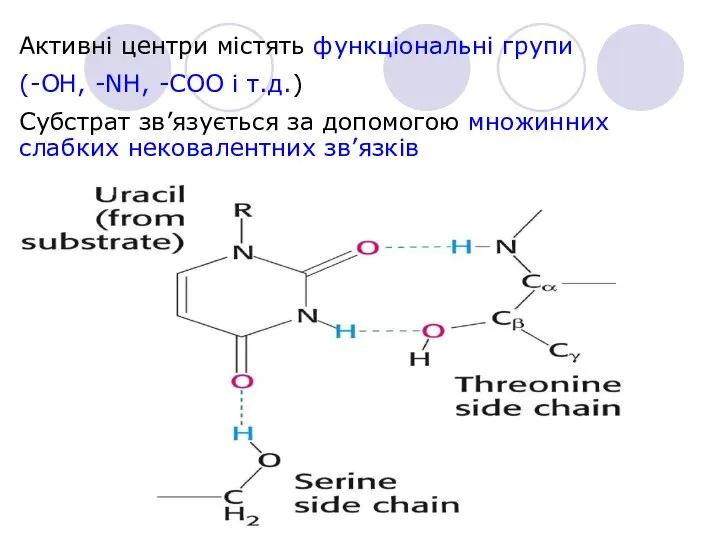
- 8. Активні центри містять функціональні групи (-OH, -NH, -COO і т.д.) Субстрат зв’язується за допомогою множинних слабких
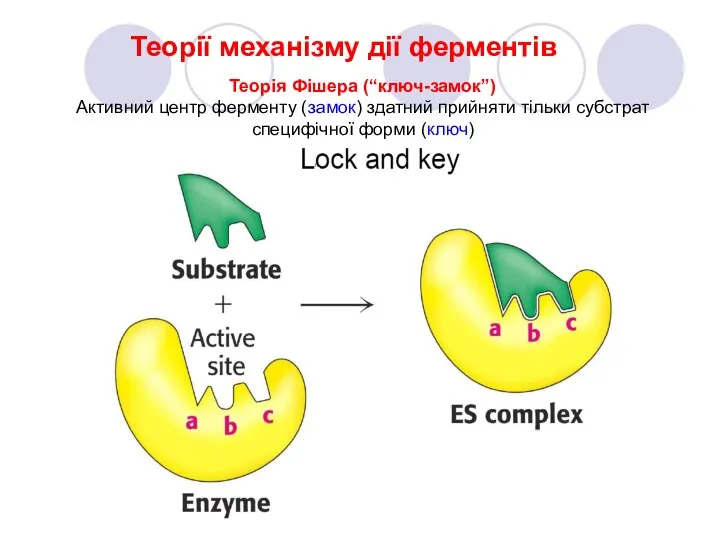
- 9. Теорії механізму дії ферментів Теорія Фішера (“ключ-замок”) Активний центр ферменту (замок) здатний прийняти тільки субстрат специфічної
- 10. Абсолютна – один фермент діє тільки на один субстрат (уреаза розщеплює тільки сечовину; аргіназа розщеплює тільки
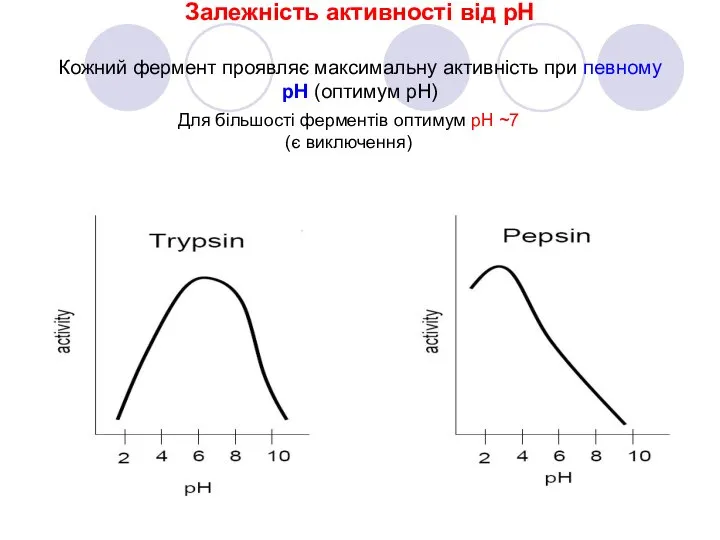
- 11. Залежність активності від рН Кожний фермент проявляє максимальну активність при певному pH (оптимум pH) Для більшості
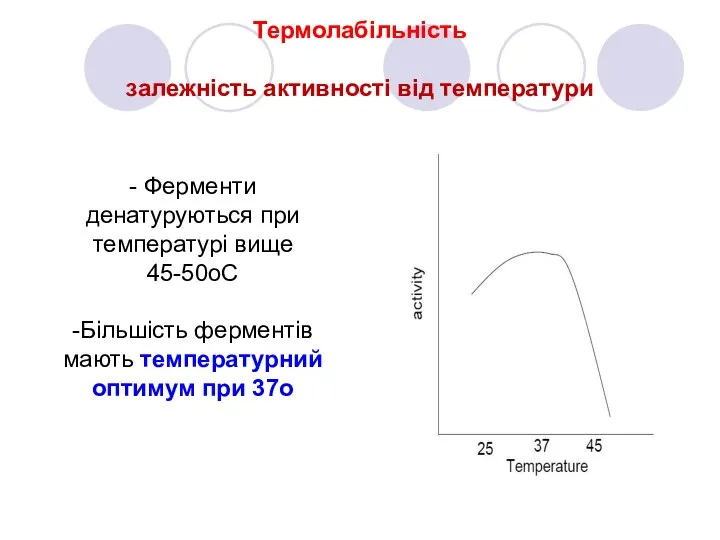
- 12. Термолабільність залежність активності від температури - Ферменти денатуруються при температурі вище 45-50oC -Більшість ферментів мають температурний
- 13. Класифікація ферментів Загальні назви Утворюються додаванням суфікса –аза до назви субстрату Приклад: - тирозиназа – окислює
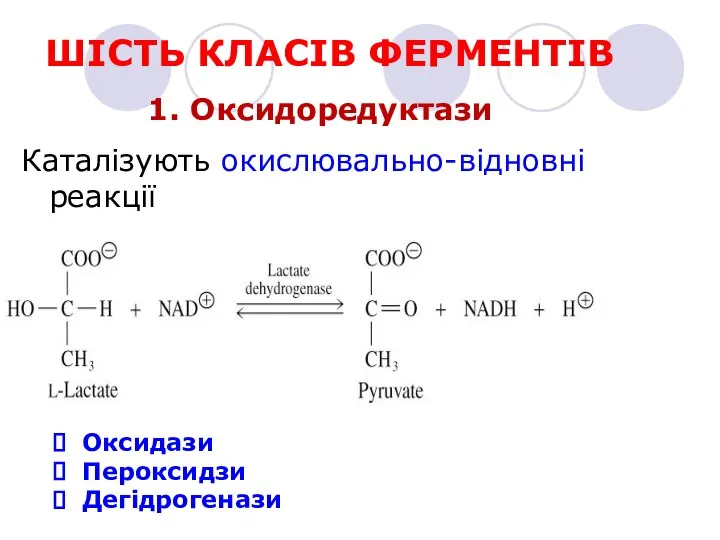
- 14. ШІСТЬ КЛАСІВ ФЕРМЕНТІВ 1. Оксидоредуктази Каталізують окислювально-відновні реакції Оксидази Пероксидзи Дегідрогенази
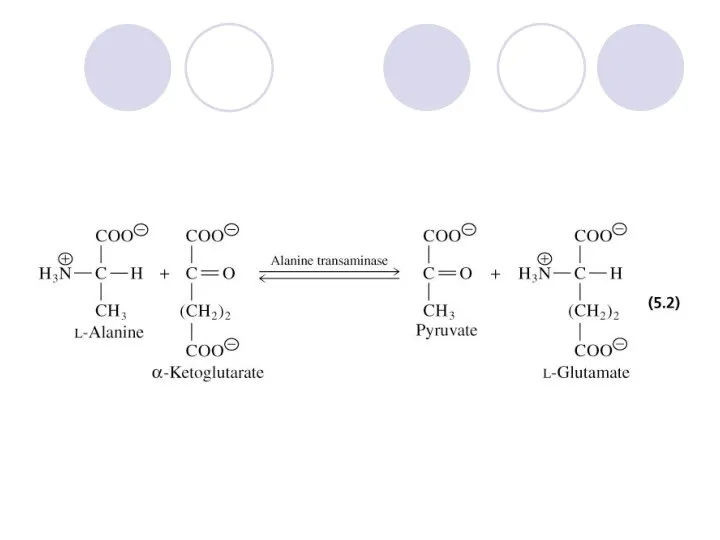
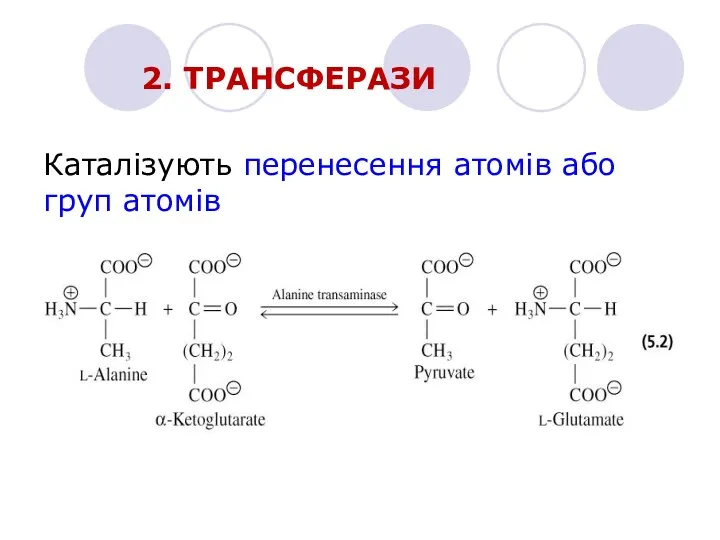
- 16. 2. ТРАНСФЕРАЗИ Каталізують перенесення атомів або груп атомів
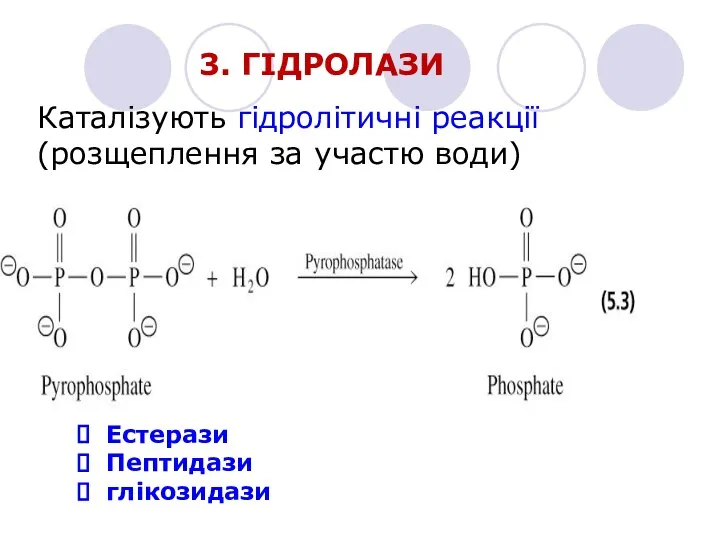
- 17. 3. ГІДРОЛАЗИ Каталізують гідролітичні реакції (розщеплення за участю води) Естерази Пептидази глікозидази
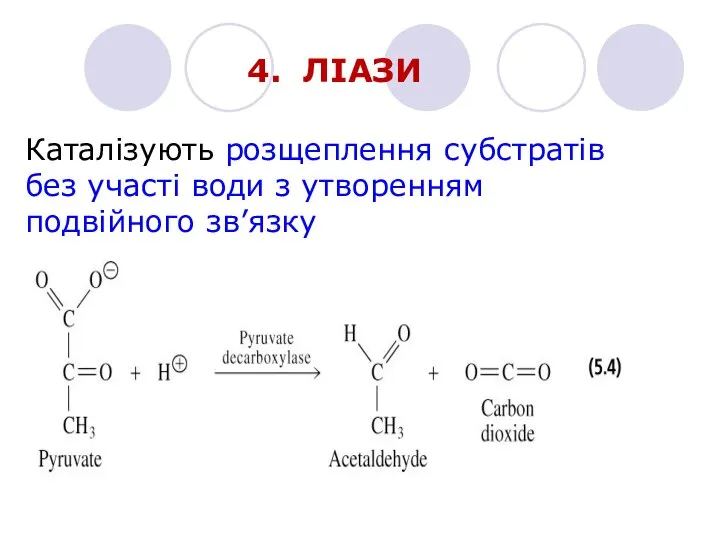
- 18. 4. ЛІАЗИ Каталізують розщеплення субстратів без участі води з утворенням подвійного зв’язку
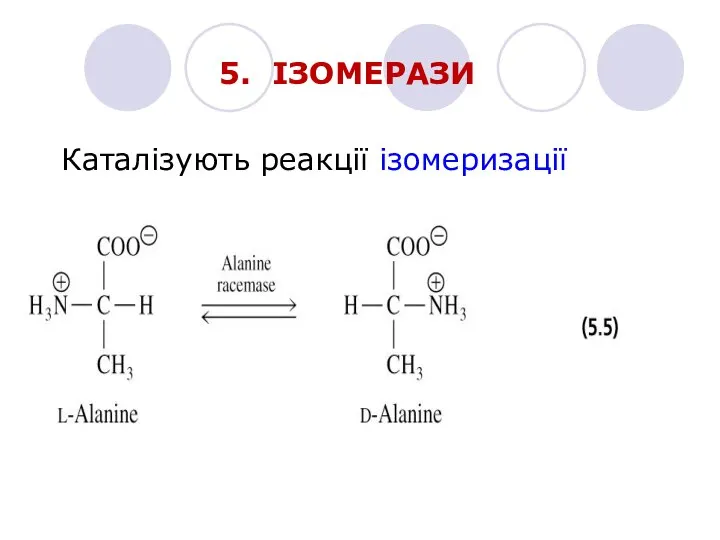
- 19. 5. ІЗОМЕРАЗИ Каталізують реакції ізомеризації
- 21. Скачать презентацию






 Презентация по Химии "Мы изучаем химию" - скачать смотреть
Презентация по Химии "Мы изучаем химию" - скачать смотреть  Поверхностные и массовые силы. Вывод уравнения неразрывности сплошной однокомпонентной среды
Поверхностные и массовые силы. Вывод уравнения неразрывности сплошной однокомпонентной среды Алкены. Состав, строение, свойства и химические превращения
Алкены. Состав, строение, свойства и химические превращения СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
СПЛАВЫ. КОРРОЗИЯ МЕТАЛЛОВ. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Мұнай эмульсиясының құрамы және фаза аралық беттерінің құрылымы. Эмульсия инверсиясы
Мұнай эмульсиясының құрамы және фаза аралық беттерінің құрылымы. Эмульсия инверсиясы Лабораторная посуда и оборудование
Лабораторная посуда и оборудование Презентация по Химии "Полезные ископаемые" - скачать смотреть
Презентация по Химии "Полезные ископаемые" - скачать смотреть  Каталитический крекинг
Каталитический крекинг Тема: Строение электронных оболочек атомов. Разработал: Учитель химии – биологии первой квалификационной категории Баженов
Тема: Строение электронных оболочек атомов. Разработал: Учитель химии – биологии первой квалификационной категории Баженов  Выращивание кристаллов в домашних условиях
Выращивание кристаллов в домашних условиях Электронные конфигурации атомов. Периодический Закон. Периодическая система Д.И. Менделеева. Химическая связь
Электронные конфигурации атомов. Периодический Закон. Периодическая система Д.И. Менделеева. Химическая связь Всероссийская олимпиада школьников по химии. Отборочный (районный) этап. Практический тур
Всероссийская олимпиада школьников по химии. Отборочный (районный) этап. Практический тур Химия и пища. Маркировка, упаковка пищевых и гигиенических продуктов, и умение их читать
Химия и пища. Маркировка, упаковка пищевых и гигиенических продуктов, и умение их читать Презентация по Химии "Увлекательные факты из жизни великого химика" - скачать смотреть
Презентация по Химии "Увлекательные факты из жизни великого химика" - скачать смотреть  Тақырыпқа байланысты білімді жүйелеу
Тақырыпқа байланысты білімді жүйелеу Общая характеристика неметаллов
Общая характеристика неметаллов Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов
Синтез новых аллильных производных семикарбазонов и тиосемикарбазонов Пиррол-2-карбальдегидов Пленки Лэнгмюра - Блоджетт
Пленки Лэнгмюра - Блоджетт Вибрационное устройство для выпуска связных, липких и слеживающихся материалов
Вибрационное устройство для выпуска связных, липких и слеживающихся материалов Хлороформ. Методы его изолирования и обнаружения
Хлороформ. Методы его изолирования и обнаружения Бүйрек зәр түзе отырып, қаннан шығатын бөлінділерді сүзетін
Бүйрек зәр түзе отырып, қаннан шығатын бөлінділерді сүзетін Решение расчетных задач по уравнениям реакций
Решение расчетных задач по уравнениям реакций Щелочи
Щелочи Супрамолекулярная химия
Супрамолекулярная химия Галогены
Галогены Натуральный и синтетический каучуки. Резина.
Натуральный и синтетический каучуки. Резина.  Chemical reactions. (Chapter 5)
Chemical reactions. (Chapter 5)